
Генная инженерия: прошлое, настоящее и будущее в изучении ДНК
Артем Елмуратов окончил мехмат МГУ, но в итоге заинтересовался генетикой — и запустил стартап Genotek. Со временем этот проект вырос до большой компании, которая занимается генетическими тестами. А сам Артем стал сооснователем еще двух стартапов, напрямую связанных с генетикой. 25 апреля, в Международный день ДНК, Артем рассказал сотрудникам BIOCAD об истории изучения наследственности и изменчивости, поделился перспективами применения современных генетических тестов, а также объяснил, что ждет генетику в будущем.
История изучения ДНК. Первые шаги: генетика от брата Дарвина
Одним из основоположников генетики, который внес свой вклад в изучение наследственности, был сэр Фрэнсис Гальтон. Этот исследователь, который всю жизнь занимался наукой — к слову, не только биологией и генетикой, — был двоюродным братом знаменитого Чарльза Дарвина. Оба брата стали талантливыми учеными, и это в чем-то соответствует выводам Гальтона о наследовании способностей и таланта: «Ровно половина из числа наиболее знаменитых людей имеет одного или нескольких выдающихся родственников». Тема наследования таланта и способностей, подобно наследованию цвета глаз и волос, живо волновала ученого. Однако не обошлось и без перегибов — Гальтон решил изучать перспективы улучшения человека при помощи искусственного отбора. Сегодня это учение известно нам под названием евгеника, а Гальтон считается его основателем и автором термина.
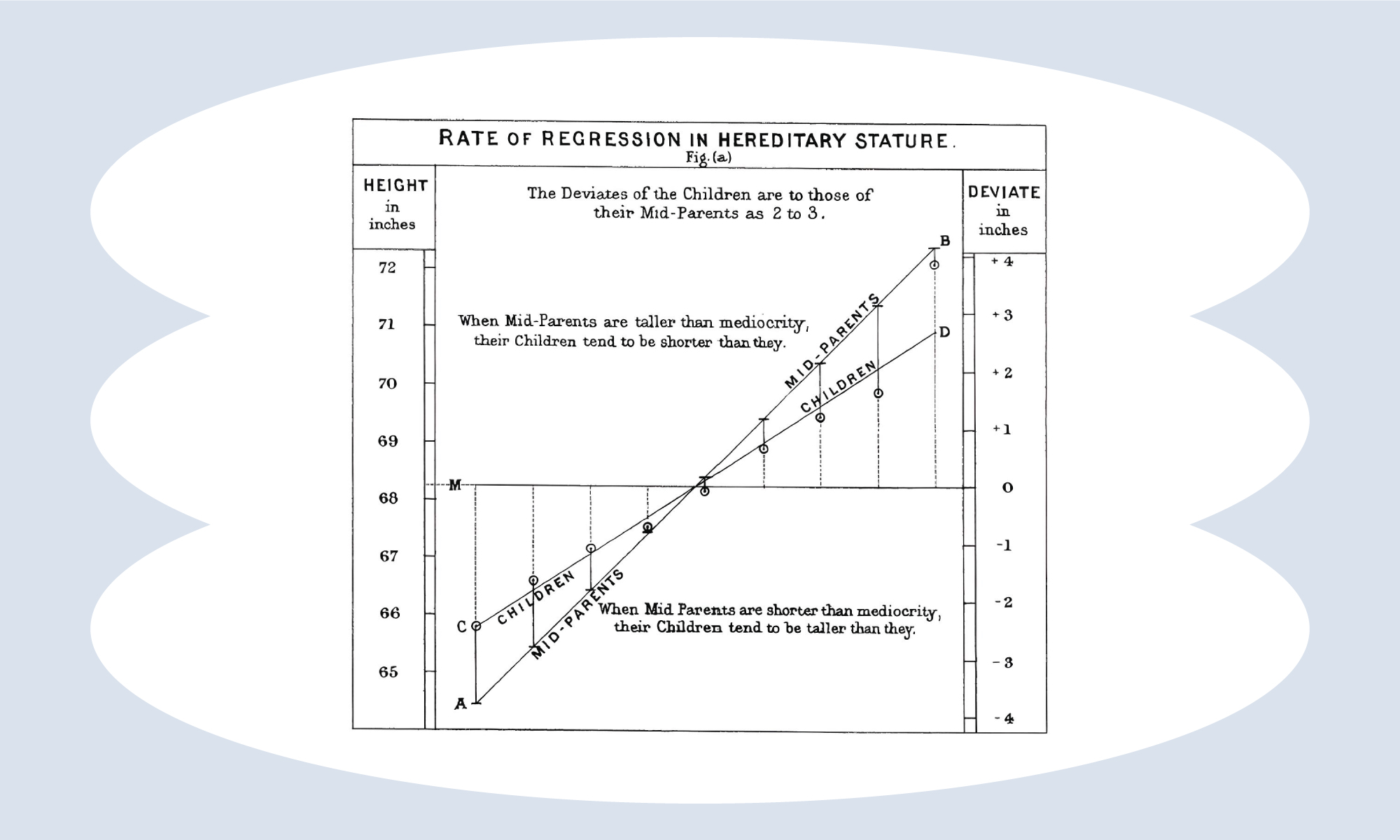
График регрессии роста у детей относительно роста родителей: исследование Гальтона
Гальтон изучал взаимосвязь между наследованием роста у отцов и детей с помощью регрессионного анализа — и показал, что в среднем у более высоких родителей более высокие дети, и наоборот. Но чисто физическими признаками дело не ограничивалось — ученый хотел доказать, что характер, поведение и ум наследуются так же, как и внешность.

«Наследственный гений»: исследование Гальтона о наследственности и родстве выдающихся людей
Неоднозначная по современным меркам, но любопытная работа Гальтона по изучению наследственности — книга «Наследственный гений». В ней он проанализировал родство около 400 «выдающихся людей», чтобы проследить взаимосвязь между родством и талантами.
Молекулярные прорывы и день ДНК
Несмотря на то что Гальтон применил математические методы к изучению наследования признаков, его выводы слабо приближают к пониманию того, как именно передается наследственная информация. А точнее — благодаря чему? Только в середине XX века удалось доказать: генетическую информацию несет молекула ДНК, та самая, которая объединяет универсальным кодом жизни всё живое на нашей планете.
Первые исследования ДНК проводили на бактериях и бактериофагах — вирусах, которые заражают бактериальные клетки. И всего за несколько лет перешли с уровня изучения микромира до человека. А дальше началась целая серия молекулярных прорывов, апофеозом которых стало открытие структуры ДНК. Это произошло 25 апреля 1953 года, а главными действующими лицами стали биолог (в начале карьеры — орнитолог) Джеймс Уотсон, физик и биолог Морис Уилкинс и физик Фрэнсис Крик, а также Розалинд Франклин, биофизик и рентгенолог. Именно они впервые показали, чем является молекула ДНК — двойной спиралью.

Уотсон, Крик и Уилкинс за свое открытие получили Нобелевскую премию по физиологии и медицине. А вот Розалинд Франклин, хоть и сыграла центральную роль в понимании структуры ДНК, не получила признания при жизни — она умерла от рака всего лишь в 37 лет.
ДНК Science: заполняем пробелы
Молекула ДНК — полимер, она состоит из множества нуклеотидов, образующих четыре типа азотистых оснований: аденин (А), тимин (Т), гуанин (Г) и цитозин (Ц). По химической природе ДНК представляет собой длинную двойную спираль, где несущая конструкция, «перила» лестницы ДНК, состоит из сахарофосфатного остова — остатков фосфата и дезоксирибозы. Два спирально закрученных витка ДНК соединяют «ступени» — азотистые основания. Эти четыре буквы составляют генетический алфавит, с их помощью записаны инструкции по сборке и действию всех белков организма.
При этом белки — это тоже полимеры, которые состоят из аминокислот. Одну аминокислоту кодируют три нуклеотида. В итоге с помощью тринуклеотидных комбинаций записана полная генетическая инструкция по устройству целого организма: какой у него цвет глаз или волос, какой окраски кожа и так далее. Различные сочетания букв генетического алфавита определяют нашу непохожесть на других. Остается понять, какие именно признаки зашифрованы под теми или иными буквами.
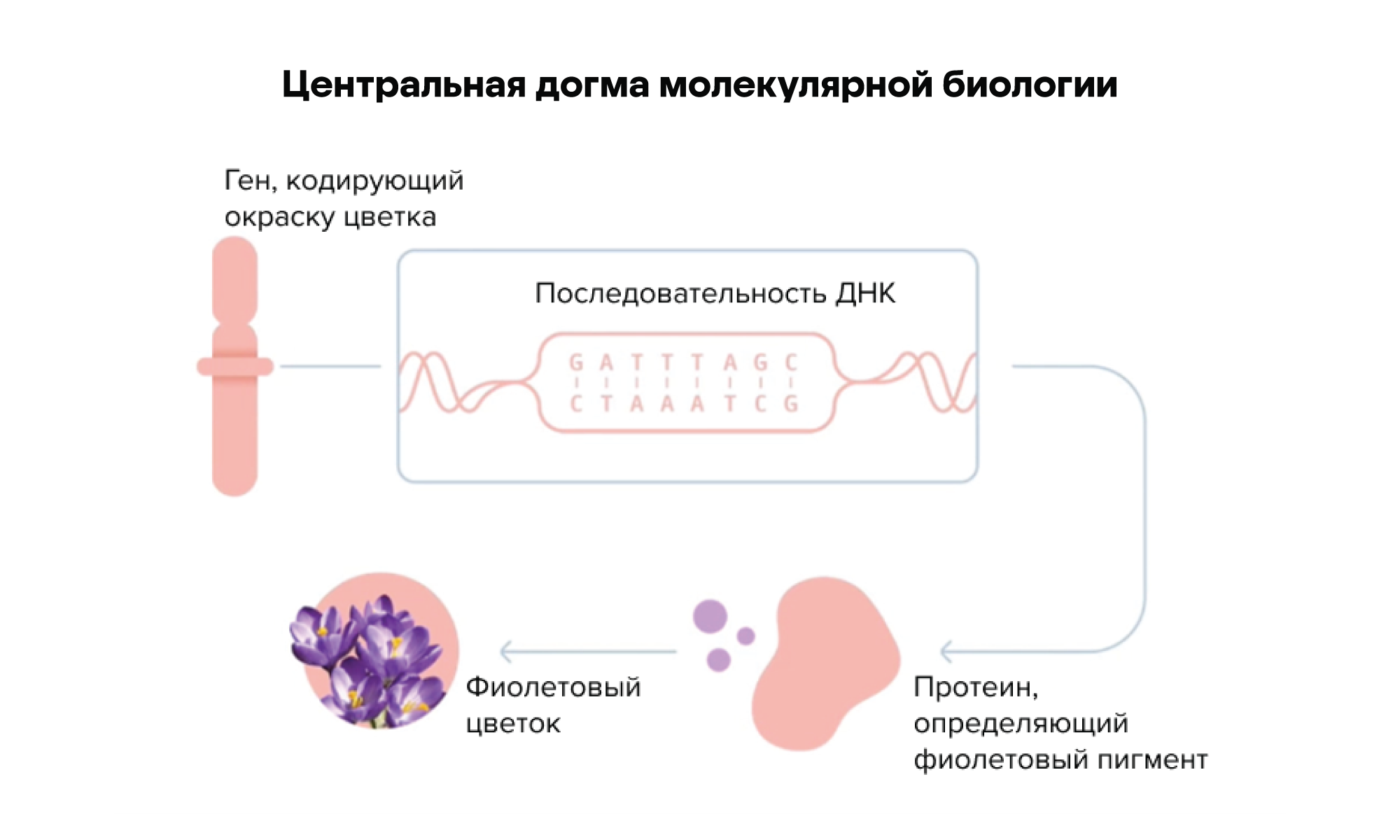
Центральная догма молекулярной биологии: один ген в молекуле ДНК кодирует один белок, который отвечает за одну химическую реакцию в клетке. Например, у растения окраска цветка определяется каким-то конкретным геном. Эта нуклеотидная последовательность сначала транслируется с двуцепочечной молекулы ДНК на одноцепочечную молекулу РНК, а затем с матрицы РНК синтезируется белок. Этот белок будет отвечать за выработку фиолетового пигмента, который придает окраску лепесткам цветка.
Несмотря на то что в 1960-70-е годы уже было известно, что из себя представляет геном, дела с его расшифровкой обстояли сложнее. Методы чтения отдельных небольших участков ДНК уже существовали, но скорость прочтения была очень низкой. И в это время работы по расшифровке генома разделились на два направления. Первый проект, который вначале курировал Джеймс Уотсон, назывался Human Genome Project и ставил своей задачей постепенно и скрупулезно, кусочек за кусочком, расшифровывать ДНК человека. А во втором проекте, лидером которого стал ученый и предприниматель Крейг Вентер, применили другой подход, автоматизируя процесс расшифровки с использованием метода молекулярного дробовика. Этот быстрый, но хаотичный метод позволяет нарезать ДНК на множество фрагментов, которые прочитывают и затем собирают снова.
Оба проекта дали свои результаты, и, наконец, в июне 2000 года представители обеих исследовательских групп объявили об успешном завершении расшифровки референсного генома человека. Впрочем, уже тогда его назвали черновым вариантом, ведь часть генома так и осталась нерасшифрованной. И только в 2022 году объявили об установлении последовательности еще 8% человеческого генома — тех самых «белых пятен», которые не вошли в изначальный проект «Геном человека».

Эволюция публикаций о проекте «Геном человека» в ведущих научных журналах
За 20 лет менялся не только дизайн обложек ведущих научных журналов. С момента объявления об успешном окончании проекта «Геном человека» до времени публикации исследований консорциума Telomere-to-Telomere удалось расшифровать сложнейшие участки человеческого генома и заполнить недостающие пропуски в генетической инструкции человека. Это стало возможным благодаря новым методам расшифровки генетического материала.
С проектом «Геном человека» связана еще одна победа, финансовая. Так, в начале 2000-х годов стоимость анализа была заоблачной: чтобы прочитать свой геном, нужно было заплатить порядка 100 млн долларов. Однако бурный рост рынка методик секвенирования позволил существенно сократить эту сумму, и уже через 10 лет стоимость одного анализа сократилась до 1 000 долларов.
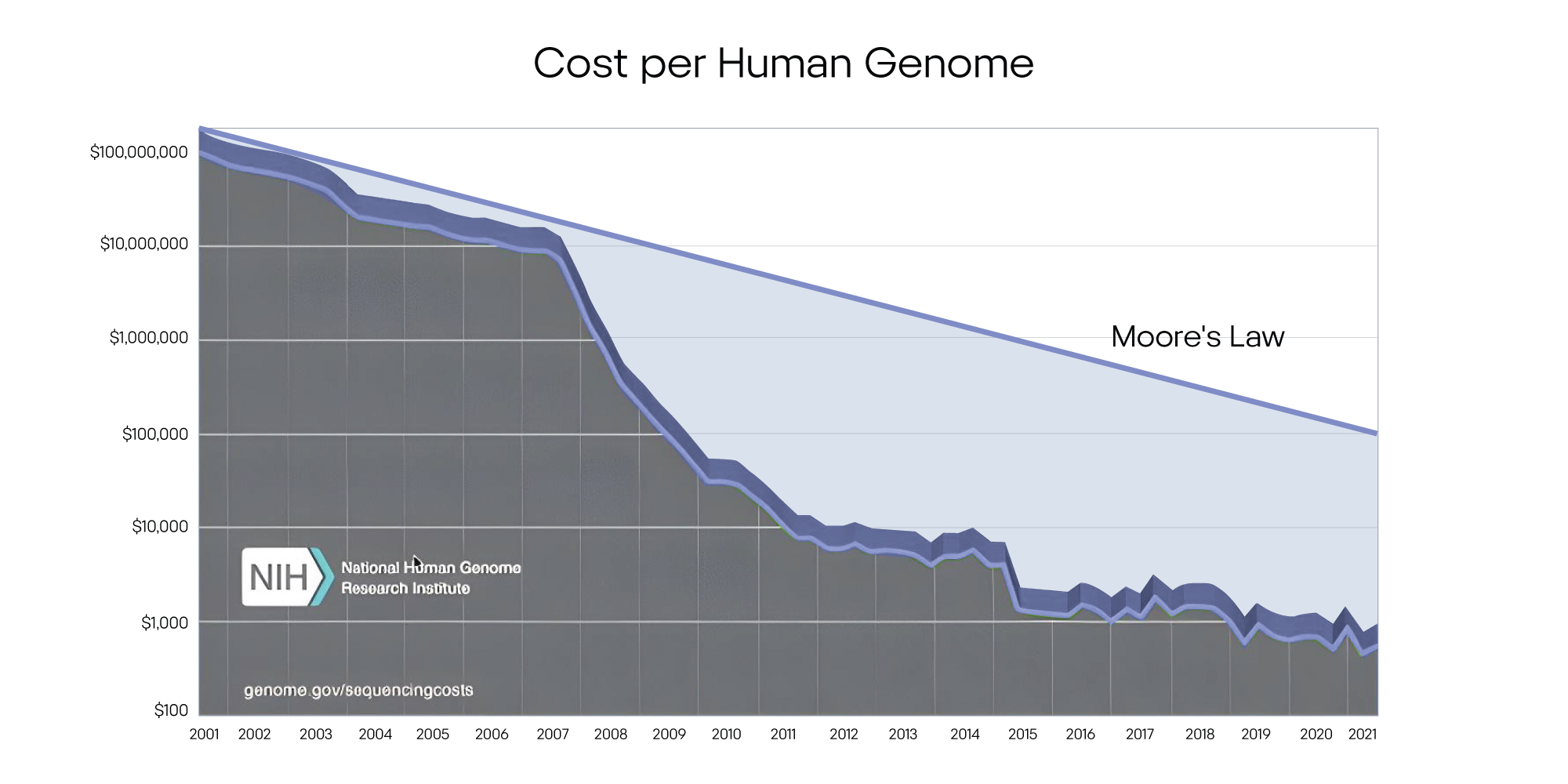
Снижение стоимости секвенирования генома человека за последние 20 лет
Стоимость секвенирования ДНК за последние 20 лет снизилась почти на порядок. Белая линия на графике иллюстрирует закон Мура. Это эмпирическое наблюдение, которое демонстрирует увеличение производительности компьютеров — она удваивается каждые 18 месяцев. Однако генетические технологии, как видно по графику, развиваются еще быстрее — и стоимость секвенирования сокращается еще больше с каждым годом. Но этот прогресс не будет бесконечным — уже сейчас мы практически вышли на плато, поэтому стоимость тестирования вряд ли существенно снизится в ближайшее время.
Зачем нужны генетические тесты
Появление технологий, которые позволяют быстро и относительно дешево читать геном человека, повлекло за собой всплеск интереса к генетике. Людям стало интересно, как они устроены и какие признаки закодированы в их ДНК. А еще — секвенирование генома стало гораздо быстрее и доступнее. Дело в том, что ДНК разных людей во многом схожа между собой, а отличия закодированы лишь в некоторых участках — полиморфизмах. В проекте «Геном человека» расшифровали общие для всех людей нуклеотидные последовательности. А сегодняшние методы исследований позволяют считывать не весь геном, а лишь конкретные участки. Благодаря этому бурно развивается рынок генетических тестов, которые решают самые разные задачи. Например, в компании Genotek работают в трех направлениях: устанавливают происхождение и генетические родословные людей, проверяют на наличие или предрасположенность к наследственным заболеваниям и занимаются вопросами молекулярной биологии и биоинформатики.
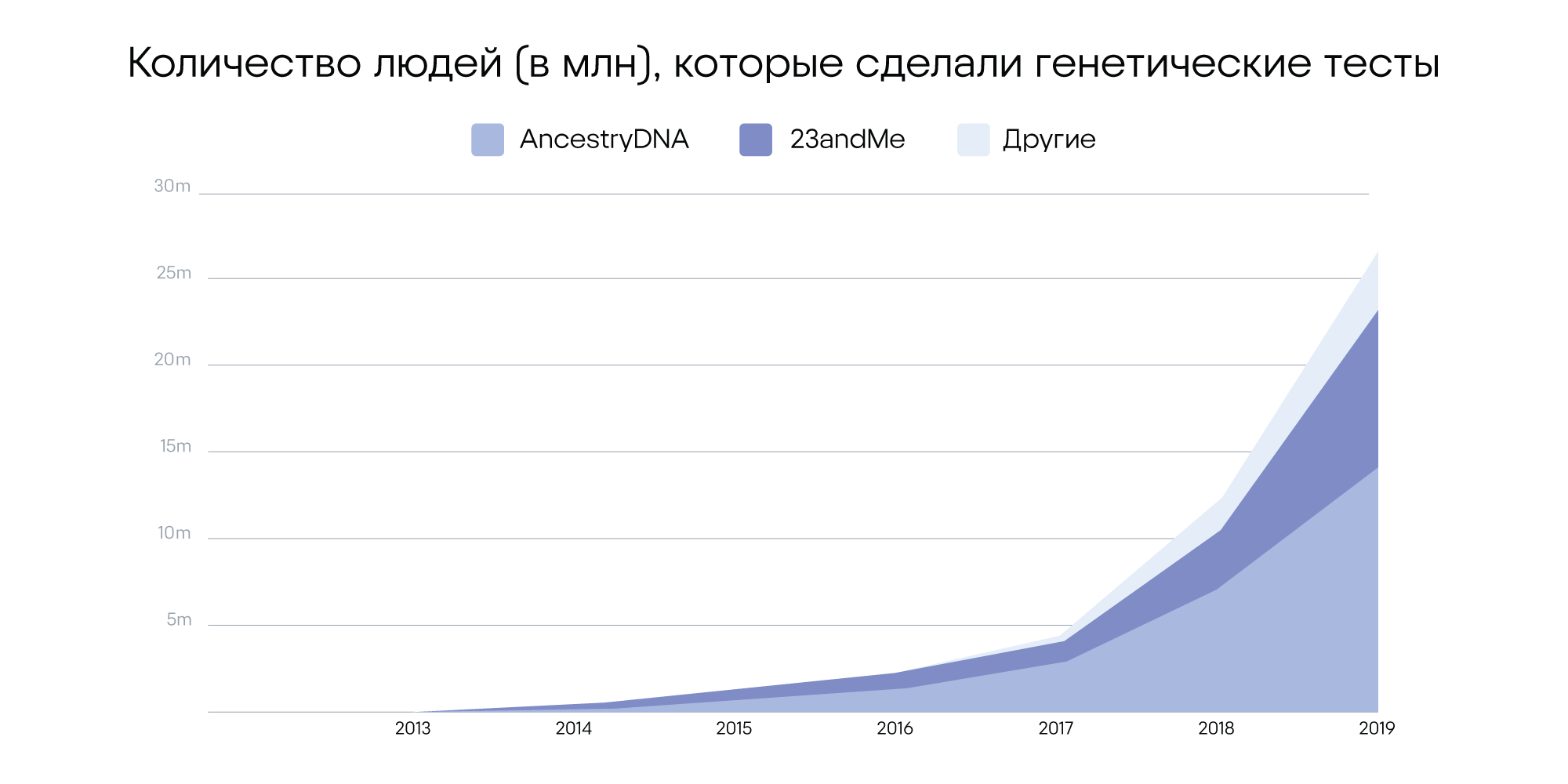
К началу 2019 года уже более 25 млн людей прошли генетическое тестирование. В числе самых популярных компаний, которые предлагают генетические тесты, — AncestryDNA и 23andMe
Генетический паспорт — как узнать себя
Один из самых популярных запросов среди людей — узнать свои персональные генетические особенности. Среди них — и происхождение, и наличие генов. Они определяют предрасположенность к различным болезням.
О чем именно говорит генетический анализ происхождения? Современные тесты позволяют заглянуть в прошлое и, например, обнаружить, сколько процентов генома неандертальца досталось конкретно вам. Еще с помощью тестов можно изучить недавнее прошлое, в пределах десятков тысяч лет, и оценить пути миграции наших предков, например куда и откуда они путешествовали. Генетические тесты также могут показать дальних родственников, которые тоже прошли тест. Это дает возможность расширить свое родословное древо и узнать больше о своей семье. Наконец, с помощью тестов удается оценить этнический состав — сколько ваших родственников и предков традиционно жили в разных регионах.
Второй важный запрос, который решают генетические тесты, — оценка своего персонального здоровья. При этом необязательно уже иметь какую-то болезнь — чаще людям интереснее, являются ли они носителями каких-то заболеваний, будучи полностью здоровыми. Здесь стоит вспомнить второй закон Менделя о расщеплении признаков: если оба родителя гетерозиготны по какому-то признаку, то есть несут в себе разные копии одного и того же гена — доминантную и рецессивную, то при воспроизведении потомства проявление этого признака происходит в определенном соотношении. Понимание того, есть ли у нас в геноме рецессивные копии генов, контролирующих развитие наследственных заболеваний, позволяет прогнозировать вероятность рождения ребенка с заболеванием.
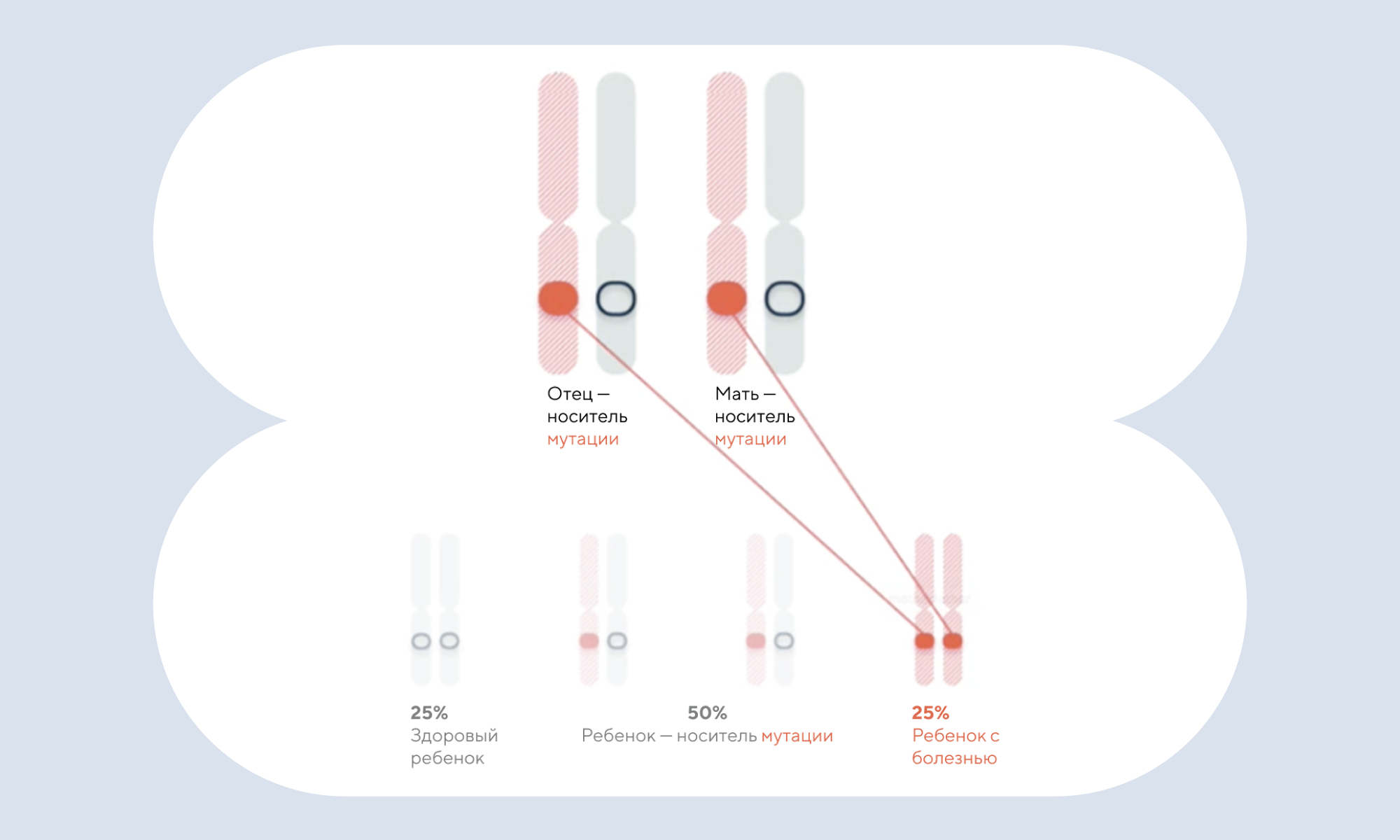
Вероятность наследования заболевания: влияние рецессивных генов
Многие люди могут являться носителями наследственных заболеваний, то есть нести в своем геноме рецессивные копии генов. В случае если у человека есть доминантная копия гена, болезнь не проявляется. Но если у потомства в хромосоме встречаются две копии рецессивных генов, то проявляется наследственное заболевание. Это может произойти, например, в том случае, если оба родителя являются носителями рецессивного гена.
Знание о наличии конкретных мутаций в генах позволяет лучше прогнозировать здоровье потомков. С этой целью применяют генетический скрининг. Один из классических примеров того, как широко распространился этот метод среди евреев ашкенази, — диагностика болезни Тея — Сакса. Так сложилось, что большинство представителей этой немногочисленной этнической группы являются носителями гена тяжелого наследственного заболевания. Чтобы снизить риск вероятности рождения ребенка с болезнью Тея — Сакса, евреи ашкенази проходят обязательный скрининг перед планированием семьи. Благодаря этой проверке за последние 20 лет удалось снизить частоту этой болезни в 10 раз.
Мультифакторные болезни — когда не во всем виноваты гены
Помимо чисто наследственных заболеваний, которые на 100% определяются генетикой и генами, существуют еще и мультифакторные болезни. Они отчасти зависят от наследственности, но также во многом определяются образом жизни и факторами окружающей среды.
Чтобы оценить, насколько заболевание зависит от генетики, используется такой признак, как наследуемость. Чем выше наследуемость, тем больше признак зависит от генетики, и наоборот. Например, цвет глаз практически полностью наследуем — мы никак не можем повлиять на то, каким он будет. Но вот, например, рост — это уже более вариативный признак. Допустим, есть два однояйцевых близнеца с идентичным набором генов. Первый занимается спортом и правильно питается, а второй недополучает витаминов и солнечного света. В итоге они, несмотря на одинаковую генетику, будут различаться по росту.
Влияние генетики на разные признаки
Изучать мультифакторные заболевания сложнее, чем чисто наследственные, так как они зависят от огромного количества разных генетических факторов, разбросанных по всему геному. Поэтому обычно при исследовании мультифакторных болезней применяют полногеномный поиск ассоциаций, когда сравнивают связь между геномом и фенотипом (внешними и внутренними признаками).

Зачем вообще изучать мультифакторные заболевания? Во-первых, понимание взаимосвязи между генетикой и образом жизни позволяет скорректировать поведение конкретного человека — например, рекомендовать ему избегать жирной пищи или реже бывать на солнце. А во-вторых, это позволяет глубже разобраться с генами, которые определяют ту или иную болезнь. Так, анализ выборки людей с высокими или низкими рисками заболеть чем-то конкретным помогает предположить, какие именно гены вовлечены в патологический процесс, приводящий к болезни. Это открывает широкие перспективы для лечения и разработки новых препаратов против генетических заболеваний. В зависимости от риска развития конкретной болезни разные группы людей могут проходить генетические скрининги с разной частотой. Чем ниже риски, тем реже необходимо проверяться.
Где еще важна генетика
Фармакогенетика — персональное лекарство для каждого
Одно из современных направлений персонализированной медицины — развитие фармакогенетики. Эта отрасль генетики позволяет понимать, как генетические особенности конкретного человека влияют на индивидуальную непереносимость лекарств. Так, даже одна вроде бы незначительная мутация может вызывать непредвиденную реакцию на какое-то химическое вещество. В результате одна и та же таблетка становится токсичной для одного человека и эффективной для другого.
Смежная область — нутригенетика, которая позволяет персонализировать питание человека. Например, вкусы и особенности восприятия пищи. Так, определенные генетические варианты кодируют нашу склонность к поеданию сладкого или к непереносимости лактозы. Изучать такие особенности не только интересно, но и полезно — понимание гастрономических вкусов может влиять на образ жизни помочь человеку избежать возможных осложнений, связанных с едой, если он просто скорректирует рацион питания.
Генетика и инфекции
Удивительно, но инфекционные заболевания могут быть вызваны генетикой. Яркий тому пример — мутация в гене CCR5, которая дает ее носителю своеобразный иммунитет против ВИЧ. Даже если человек проконтактирует с больным ВИЧ-инфекцией, заболевание не разовьется.
Еще один интересный пример, связанный с недавней пандемией COVID-19, — генетические особенности восприятия вируса SARS-CoV-2 у разных людей. В Nature было опубликовано интересное исследование, которое провел консорциум ученых со всего мира, включая Genotek. Оно было связано с выявлением генетических факторов у людей и их влиянием на терапию болезни. В результате удалось понять, как именно генетика человека связана с течением COVID-19 — с точки зрения риска заболеть и с точки зрения риска получения осложнений.
Генетическое редактирование: как изменить свои гены
После того как генетики научились читать геном, встал вопрос: а можно ли изменить гены? Например, чтобы избавить людей от наследственных заболеваний.
Само по себе направление генной инженерии, при которой производят различные манипуляции с генами, не ново. Первые опыты по синтезу инсулина с помощью трансгенных бактерий начали проводить еще в 1970-е годы. Однако редактирование генома с помощью высокотехнологичных инструментов вроде «молекулярных ножниц» — все еще новая и постоянно совершенствуемая технология. Среди таких инструментов — технология CRISPR, которая позволяет относительно точно редактировать конкретные участки в геноме. Метод заключается в том, что особая генетическая конструкция — CRISPR/Cas9 — находит нужное место в молекуле ДНК и делает в нем разрез. В результате можно удалять определенные участки генома, например те, которые несут патогенную мутацию. А еще — что сложнее — вставлять на место удаленных последовательностей новые участки и затем зашивать место разреза благодаря механизму репарации.
Будущее генетики: что нас ждет дальше
За последние 150 лет генетика пережила настоящую эволюцию, которую сейчас можно назвать революцией. Сегодня мы, как кажется, знаем про ДНК почти всё — но в то же время очень мало. В будущем спектр исследований, которые можно покрыть с помощью генетических тестов, будет расширяться, а качество и точность самих тестов — улучшаться. Чем больше людей будут участвовать в генетических скринингах и интересоваться собственным геномом, тем большую выборку для изучения генетических признаков мы получим. А дальнейшее совершенствование методов редактирования генома даст в руки врачей новые методы для лечения ранее неизлечимых заболеваний.