
Стереть из памяти: как манипулировать иммунными клетками. Дмитрий Чудаков об иммунологической памяти
Дмитрий Чудаков — один из ведущих российских иммунологов, специалист в области адаптивного иммунитета. Сейчас он руководит отделом геномики адаптивного иммунитета ИБХ РАН и исполняет обязанности директора НИИ трансляционной медицины РНИМУ им. Н. И. Пирогова. Мы пригласили Дмитрия на встречу с сотрудниками BIOCAD, на которой он рассказал о работе Т-клеточных рецепторов, B-клеток и антител и о том, как ими управлять.
Это не самая простая статья для тех, кто впервые столкнулся с этими терминами, но мы все равно советуем попробовать разобраться — это поможет понять механизм действия современных онкологических и аутоиммунных препаратов.
Иммунное вступление: как узнать врага
Наш организм подвергается постоянным атакам патогенов — вирусов и бактерий. Первым звеном защиты выступает врожденный иммунитет. На этом этапе подключаются клетки врожденного иммунитета, которые неспецифичным образом пытаются понять, кто нас атакует, и передают нужные сигналы на второй уровень — специфичным клеткам адаптивного, или приобретенного, иммунитета. При этом бывает так, что патоген уже знаком организму — его узнают особые клетки памяти, которые остались в организме со времен прошлого патогенного вторжения.
Адаптивный, или приобретенный, иммунитет — это невосприимчивость к антигену чувствительного к нему организма, приобретаемая в процессе онтогенеза в результате естественной встречи с этим антигеном организма. Примерами адаптивного иммунитета являются невосприимчивость к инфекциям после перенесенного заболевания (постинфекционный иммунитет), поствакцинальный иммунитет.
Может показаться, что перед организмом встает невыполнимая задача: как можно быть готовым к встрече с условно бесконечными видами патогенов, каждый из которых требует уникального противодействия? Но иммунитет научился справляться с этой задачей необычным способом: он случайным образом генерирует огромное разнообразие последовательностей, которые кодируют антитела и Т-клеточные рецепторы. Антитела производят В-клетки, а Т-клеточные рецепторы — уникальные белки на поверхности Т-клеток. В результате в организме образуется колоссальное разнообразие Т- и В-лимфоцитов, каждый из которых может распознать какой-то конкретный антиген, например фрагмент чужеродного белка, и запустить каскад иммунных реакций для уничтожения чужеродного патогена.
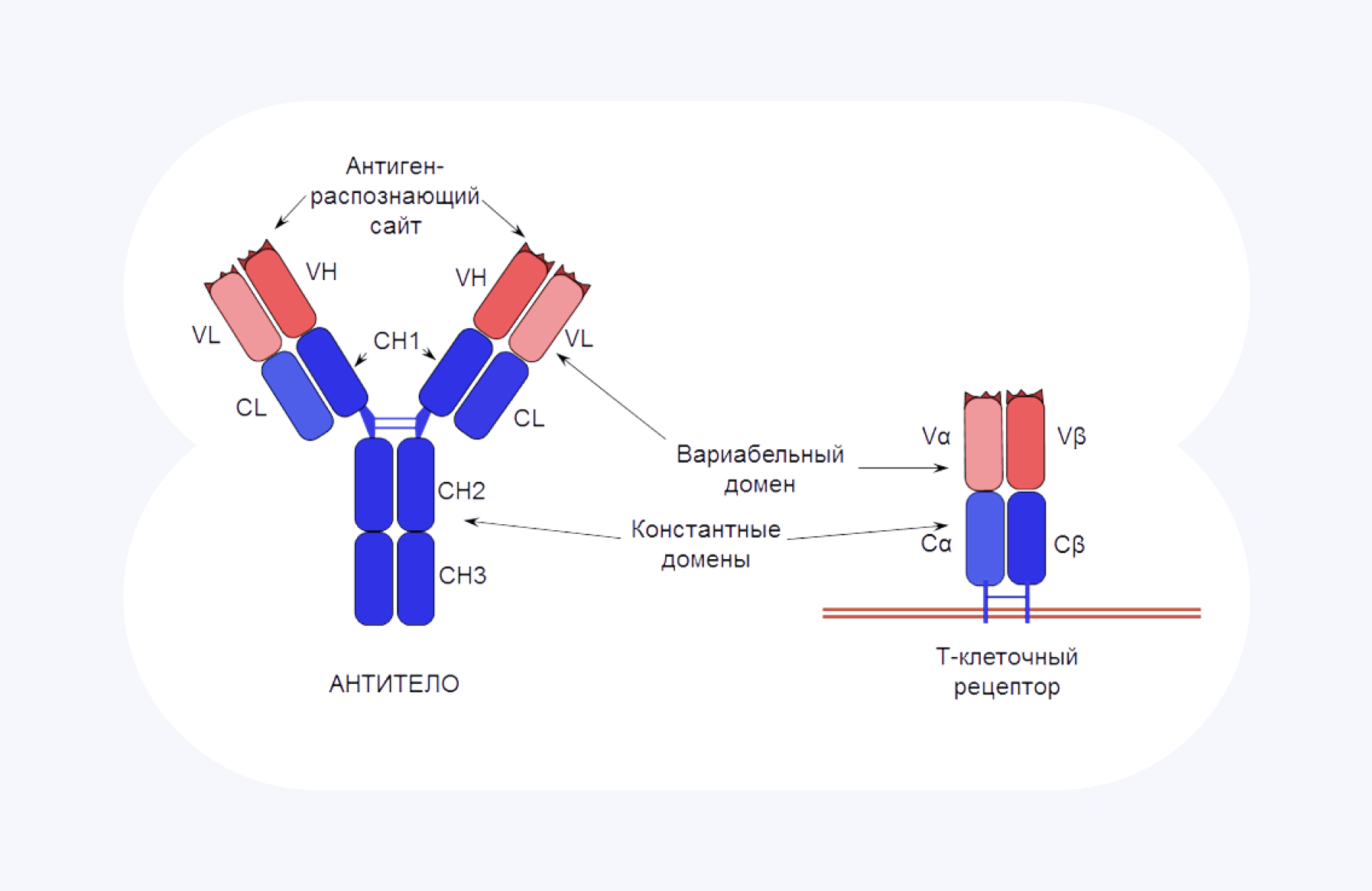
В-лимфоциты продуцируют антитела, а Т-лимфоциты — Т-клеточные рецепторы. Благодаря своим антиген-распознающим сайтам антитела и TCR (T-cell receptors) могут специфично узнавать патогены, которые оказались в организме, и запускать процесс их уничтожения
Кроме того, что иммунные клетки памяти понимают, знаком ли им тот или иной патоген и как ему противодействовать, они еще и понимают, в какой локации им необходимо действовать. Например, когда человек заражается вирусом гриппа, то в первом периоде болезни в крови падает количество Т-лимфоцитов, специфичных к патогену. Все потому, что иммунные клетки перебазируются в легкие, чтобы обеспечить необходимую защиту. Такое географическое понимание в адаптивной иммунной системе очень важно. Эти особенности иммунологической памяти позволяют организму в ускоренном режиме реагировать на повторное вторжение патогена. Более того, клетки памяти способны поддерживать высокую численность на протяжении многих лет.
Т-клеточные репертуары: как сформировать уникальность
Разнообразие Т-клеток, а точнее, Т-клеточных рецепторов (TCR), которые играют ведущую роль в распознавании патогенов, формируется в результате случайной сборки. Дело в том, что в геноме закодированы самые разные варианты нуклеотидных последовательностей, которые определяют структуру V-, D- и J-сегментов будущего TCR. Когда приходит время собирать новый рецептор, то эти три кусочка отбираются случайным образом, собираясь в новый ген. А на местах стыков дополнительно удаляются или добавляются нуклеотиды. В результате эти «швы» делают TCR еще более уникальным и в будущем позволяют специфичным образом узнавать антиген, против которого следует запустить защитную реакцию.
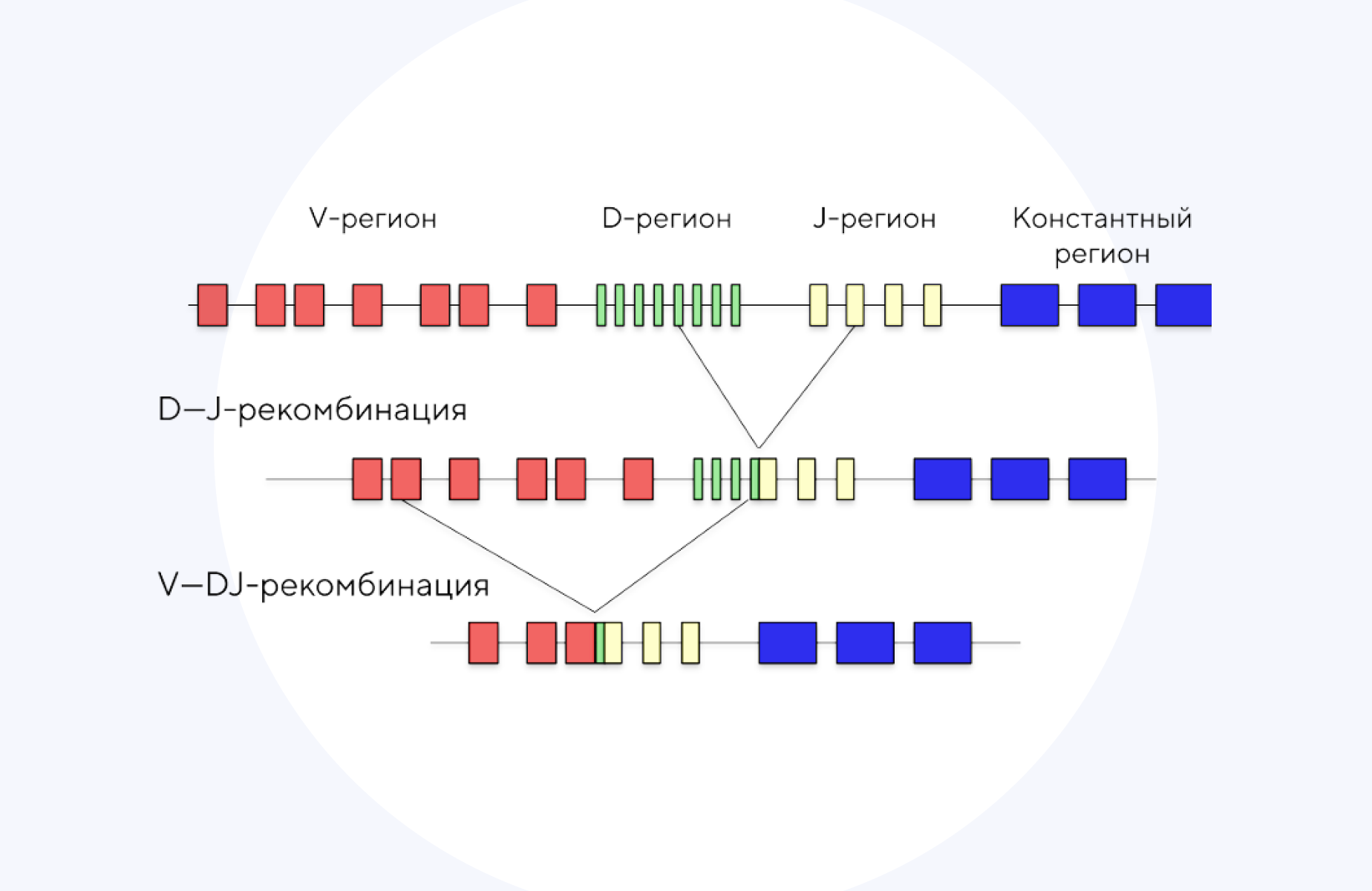
TCR состоит из двух частей — вариабельной и константной. За распознавание антигена отвечает вариабельная часть. Чтобы обеспечить большое разнообразие TCR, специфичных к различным антигенам, происходят VDJ-рекомбинации, когда последовательности трех разных регионов (V, D и J) случайным образом соединяются между собой
На этом формирование Т-клеточного репертуара с уникальным набором TCR не заканчивается. После первичной сборки Т-лимфоциты подвергаются проверке: нормально ли они работают и безопасны ли они для остальных клеток организма. На этом этапе отбора большая часть Т-клеток погибает, и в строю остаются только самые пригодные кандидаты — те, которые с большой вероятностью не вызовут аутоиммунных реакций и не будут атаковать собственные клетки. Впрочем, даже несмотря на тщательный отбор, возможны ошибки — и тогда в иммунную систему попадают Т-клетки, вышедшие из-под контроля.
Если говорить о лечении аутоиммунных патологий, то наша задача — научиться каким-то образом исправлять иммунологическую память и, например, выключить или заставить «забыть» поломанные Т-клетки о тех антигенах, от которых не нужно избавляться.
Знать последовательность репертуаров TCR важно для терапии не только аутоиммунных заболеваний. При раке вариабельные части иммунных клеток также имеют большое значение. Например, если клетки опухоли произошли от злокачественно перерожденных Т- или В-лимфоцитов, то информация об уникальной последовательности их TCR (в случае Т-клеток) или вариабельной части BCR (в случае В-клеток) может стать маркером для отслеживания других опухолевых клеток.
Наконец, TCR способны помочь в лечении пациентов, которым трансплантируют гемопоэтические клетки доноров. После переноса чужих клеток отслеживание наборов TCR позволяет понять, как восстанавливаются Т-клеточные репертуары. Оценка этой динамики и анализ возможных реакций «трансплантат против хозяина» может улучшать существующие медицинские протоколы и внедрять более персонализированный подход к лечению пациентов.
Как манипулировать Т-клетками
Чтобы управлять иммунологической памятью, важно понимать особенности формирования Т-клеточных репертуаров. Здесь важно вспомнить различия между разными популяциями Т-клеток: Т-хелперами (CD4+) и цитотоксическими Т-лимфоцитами (CD8+). Разница между ними в том, что CD8+ клетки способны самостоятельно распознать и атаковать патоген, например вирус или поломанную клетку, которой в организме в норме быть не должно. А вот CD4+ клетки мониторят организм на предмет возможных «чужаков» и в случае, если встречают кого-то не того, запускают передачу сигнала другим клеткам иммунной системы, которые будут уничтожать патоген. Но при этом оба типа Т-лимфоцитов сходны в том, что для узнавания чужеродного агента они используют те самые специфичные TCR, которые мы обсудили выше.
Что можно сделать с Т-клетками? Стоит отметить, что в норме Т-клетки не обмениваются TCR, и один Т-клеточный репертуар не может просто так взять и перейти в другой класс, клетки которого будут нести на поверхности другие уникальные TCR. Однако можно временно поменять тип Т-клеток. Например, выделить из организма CD4+ Т-клетки, произвести над ними некоторые манипуляции (например, соединить их с иммуносупрессором вроде TGF- β), и они временно превратятся в Т-регуляторные клетки. Казалось бы, это могло бы быть полезным в лечении аутоиммунных заболеваний — достаточно лишь ввести в организм пациента эти модифицированные Т-клетки, чтобы они выключили аутоиммунные реакции и избавили от болезни. Но этого не происходит, так как эффект «перепрофилирования» Т-клеток слишком недолговечен — на уровне их геномов не закреплена такая иммуносупрессивная программа.
Однако можно заставить замолчать конкретный тип CD4+ Т-клеток. Это возможно, если знать структуру TCR, а конкретно — последовательность бета-цепи (или альфа-цепи) Т-клеточного рецептора из конкретной популяции. Если разработать антитело, способное специфично связываться с конкретным участком на поверхности TCR, то можно точечно выключить конкретный Т-клеточный репертуар, не затрагивая все остальные Т-клетки. Получается, что мы удаляем лишь небольшой процент из всего спектра Т-клеточных репертуаров, не провоцируя какой-либо вред для организма.
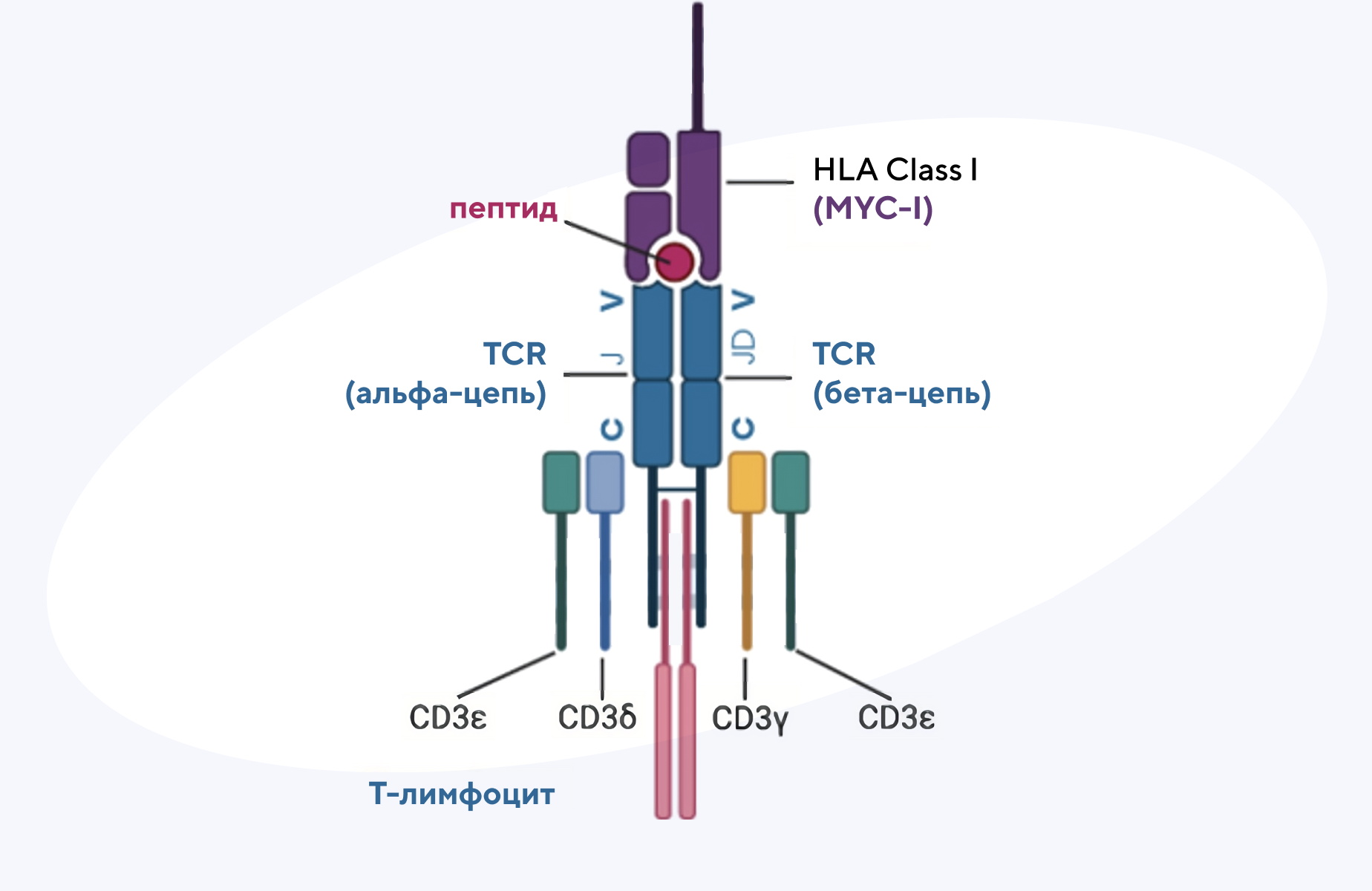
Сборка всего огромного разнообразия Т-клеточных рецепторов носит случайный характер, и состав вариабельного VDJ-участка на бета-цепи TCR также формируется случайным образом. В случае, если мы знаем конкретную последовательность на участке бета-цепи, можно синтезировать антитело, которое узнает и «выключит» этот тип Т-клеток
Перспективы управления В-клеточным иммунитетом
Обычно принято ассоциировать иммунологическую память с Т-клетками, однако В-клетки тоже остаются важными игроками на этой арене. В-лимфоциты бывают разных типов, а их В-клеточные рецепторы также несут информацию о конкретных антигенах и о том, как именно отвечать на ту или иную угрозу. И хотя В-клетка и не является профессиональной антиген-презентирующей клеткой, она способна узнавать очень специфичные антигены — те, которые она узнает с помощью рецепторов на своей поверхности.
За последние годы в онкологии выявили взаимосвязь между исходом болезни и В-клетками. Например, в случае меланомы удалось показать, что высокий уровень IgG1, продуцируемых В-лимфоцитами, связан с хорошим прогнозом. А вот IgA, наоборот, часто ассоциированы с негативным исходом, в частности с иммуносупрессией, или, иначе, иммунодепрессией.
Можно ли управлять В-клетками и тем самым влиять на течение болезни?
Если разработать анти-IgA антитело, потенциально можно удалить из популяции вообще все В-клетки с IgA, чтобы улучшить течение болезни. Либо можно воздействовать более мягко, влияя только на В-клетки памяти, благодаря чему в организме остается защита в виде наивных В-клеток.
Это лишь один из множества примеров того, как можно направить и скоординировать взаимодействие между разными ветвями иммунологической памяти и заставить клетки работать против болезней. А в целом, знания о Т-клеточных репертуарах и антителах — мощное и перспективное направление в современной иммунологии, в котором еще предстоит сделать много открытий.
