Дайджест #11. Свой против своих
Иммунотерапия пациентов применяется не так давно, но уже зарекомендовала себя как эффективный способ стимуляции иммунной системы. Но иногда этот способ лечения дает осечку и приводит к серьезным аутоиммунным нарушениям. Почему это происходит и какие именно препараты на основе биомолекул провоцируют выработку аутоантител, читайте в новом дайджесте.
Онкология
Как предотвратить распространение метастазов
Несмотря на то что только 0,02% опухолевых клеток способны образовывать метастазы, проблема метастазирования при раке остается очень актуальной. Исследователи из Швейцарии решили проанализировать возможные пути активации метастазирования, чтобы найти потенциальные ингибиторы распространения опухолей. И им это удалось — правда, пока только на примере печени мышей, для которых разработали модель колоректального и панкреатического рака, а также модель меланомы. С помощью транспозонов, содержащих систему СRISPR/Cas, и флуоресцентного окрашивания удалось изучить взаимодействия, которые возникают между гепатоцитами и метастатическими клетками. В результате получилось идентифицировать критический регулятор колонизации печени онкоклетками — им оказался плексин В2, белок из семейства семафоринов. Метастазирование печени происходит за счет того, что плексин B2 взаимодействует с семафоринами IV класса на поверхности опухолевых клеток. В результате изменяется регуляция фактора KLF4, который играет важную роль в развитии некоторых видов рака, и это способствует приобретению эпителиальных признаков у онкоклеток — они словно маскируются под обычные клетки. Если заблокировать передачу сигнала между плексином В2 и семафоринами, можно заблокировать колонизацию печени метастатическими клетками. — In vivo interaction screening reveals liver-derived constraints to metastasis.
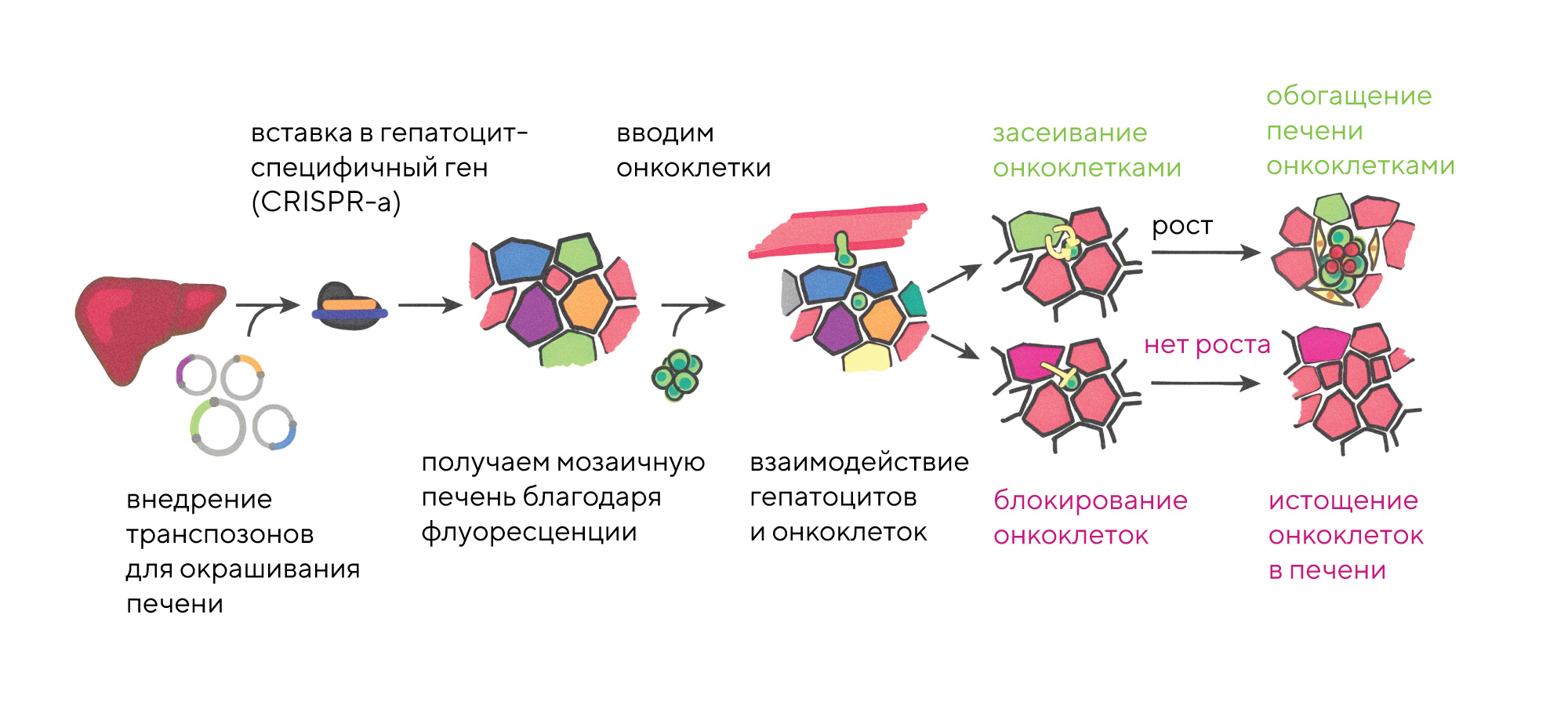
Схема эксперимента: опухолевые клетки взаимодействуют с гепатоцитами, которые способствуют или подавляют засеивание печени. В результате, в зависимости от типа взаимодействий, печень либо колонизируется онкоклетками, либо ингибирует метастазирование. Источник: адаптировано из Nature
Как изменить метаболизм для терапии меланомы
Одно из условий быстрой экспансии опухолевых клеток — быстрый метаболизм: для стремительного роста и частых делений онкоклеткам нужно настраивать свой обмен веществ. Это же свойство представляет собой потенциальную мишень: если подавить активацию метаболизма в опухоли, можно заблокировать ее рост. Китайские исследователи протестировали один из сценариев такой реактивации метаболизма на модели меланомы. Для этого к мышам с меланомой добавили специально сконструированные наномицеллы с L-тирозином и олеиламином (MTyr-OANPs). Это привело к замедлению меланогенеза — образованию меланина из тирозина — и, как результат, к значительному затруднению пролиферации клеток опухоли за счет ингибирования гликолиза: онкоклеткам просто неоткуда было брать энергию для деления. Также выяснилось, что добавление мелатонина в качестве естественного фототермического агента полностью устраняет опухоль у мышей с меланомой, которым проводили такую фототермическую терапию в сочетании с добавлением MTyr-OANPs. Эта стратегия борьбы с опухолью может стать реальной терапией меланомы. — Nutrient-delivery and metabolism reactivation therapy for melanoma.
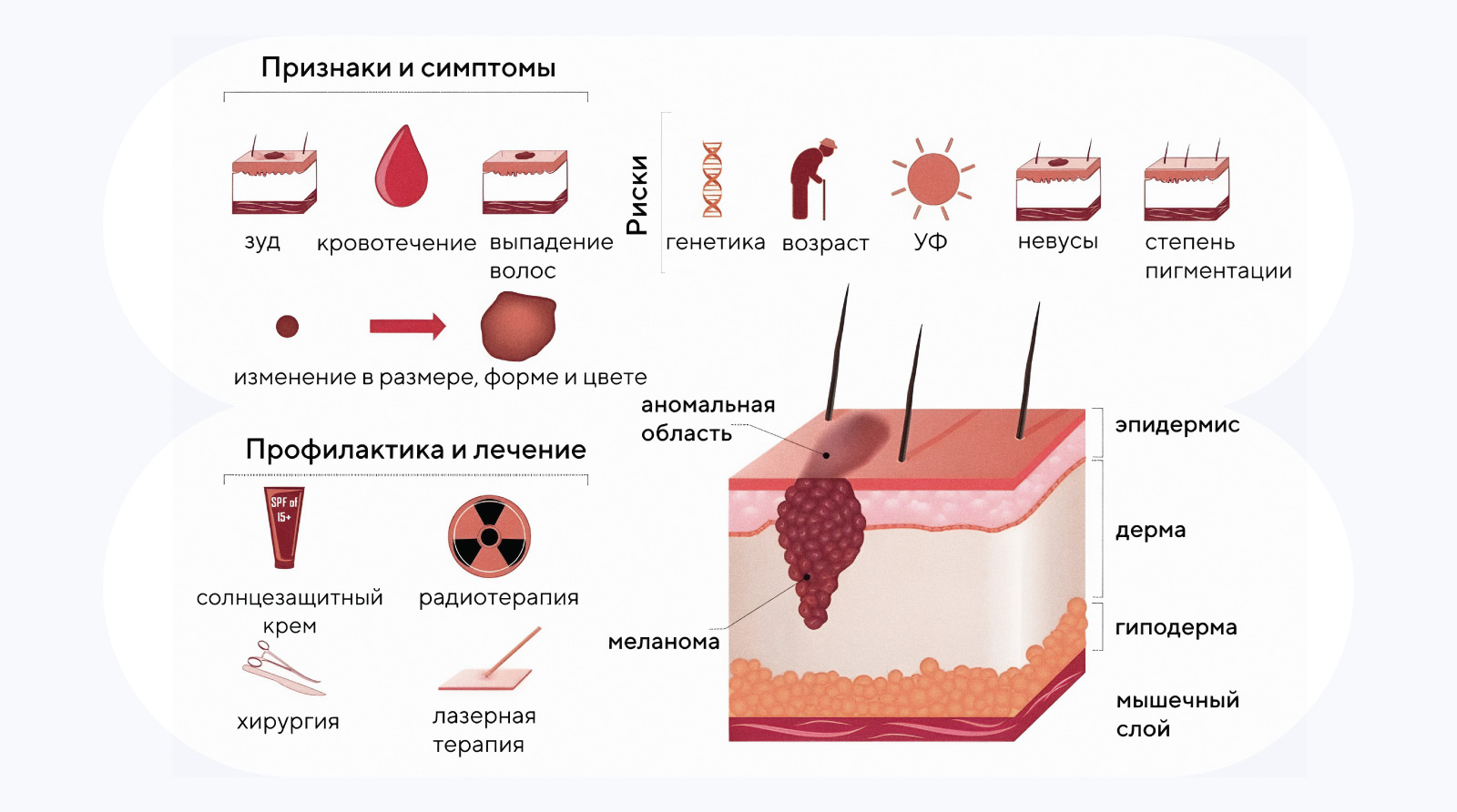
Симптомы и лечение меланомы. Источник: CD
Циркадность в генах помогает прогнозировать развитие рака легких
Аденокарцинома легких — один из наиболее распространенных типов злокачественных новообразований легочной ткани. Прогнозировать развитие этой болезни позволяют генетические маркеры, в том числе те, которые связаны с циркадными ритмами. Различные регуляторы суточных ритмов отвечают за огромное разнообразие реакций, в том числе за пролиферацию раковых клеток и их метаболизм. Чтобы оценить влияние циркадных ритмов у онкопациентов, китайские исследователи проанализировали данные об экспрессии генов из базы TCGA-LUAD (The Cancer Genome Atlas — LUng ADenocarcinoma) для построения модели, а информацию про 647 пациентов с аденокарциномой взяли из другой базы, для контрольной проверки. В результате удалось построить модель оценки риска для генов, ассоциированных с циркадными ритмами, — получилось идентифицировать восемь генов. Эта модель позволяет прогнозировать исход заболевания у пациентов с аденокарциномой легкого — в сочетании с классической терапией она может оптимизировать принятие решений при лечении. — Prediction of lung adenocarcinoma prognosis and diagnosis with a novel model anchored in circadian clock-related genes.
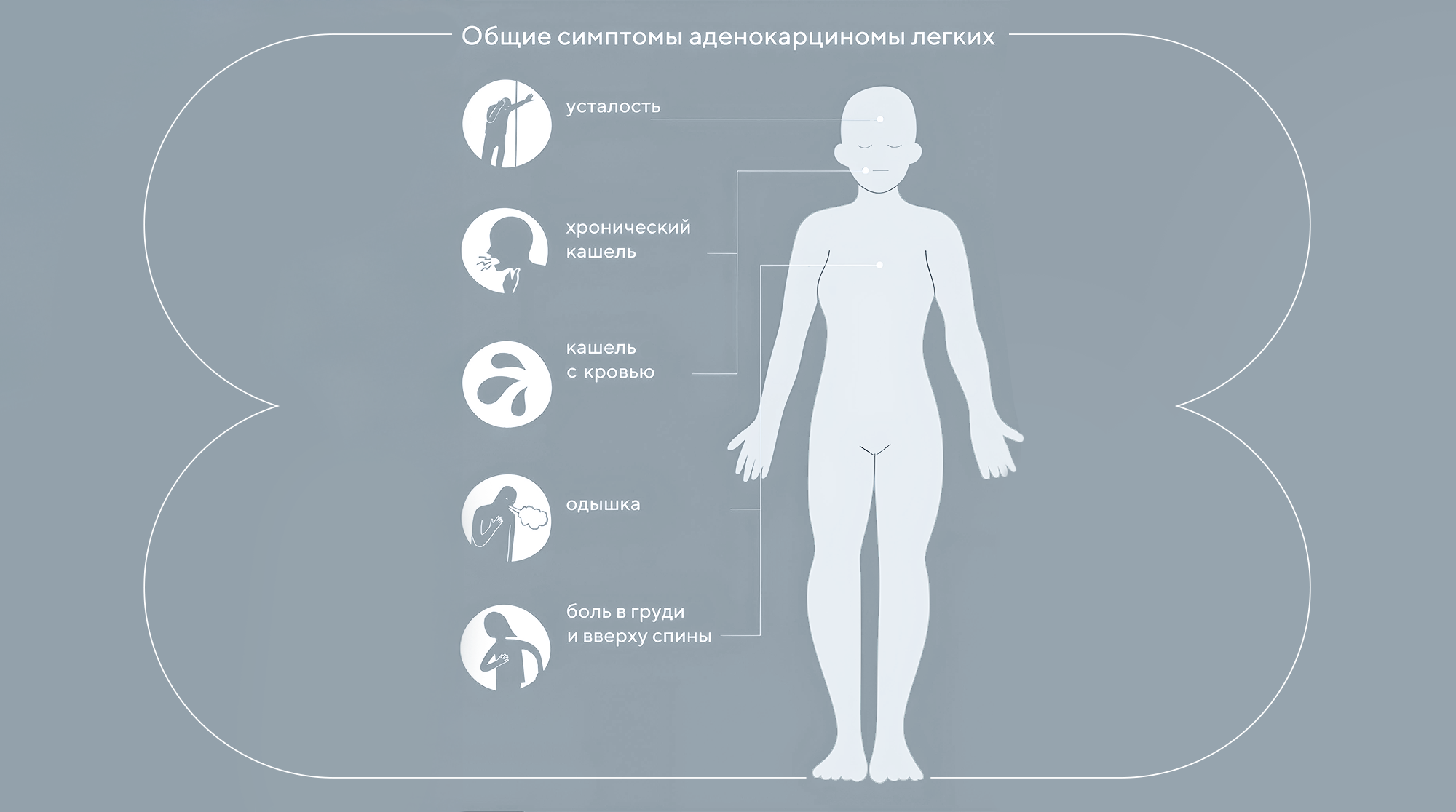
Источник: Very Well Health
Аденокарциномы легких долгое время могут не проявлять никаких симптомов. Первые признаки заболевания часто менее очевидны, чем в случае других форм рака легких. Только на поздних стадиях проявляются более заметные симптомы в виде хронического кашля и кровавых выделений при кашле.
Зачем изучать рецепторные тирозинкиназы в случае рака
Рецепторные тирозинкиназы — трансмембранные белки, которые пронизывают мембраны и участвуют в регуляции многих клеточных процессов. Но, помимо выполнения нормальных функций, также эти белки могут играть ключевую роль в развитии злокачественных опухолей. Перелом от нормы в сторону патогенеза рака происходит, когда в рецепторных тирозинкиназах случаются мутации. Именно это делает тирозинкиназы важным объектом исследования, на который можно воздействовать для таргетной терапии опухолей. За последние двадцать лет удалось разработать и проверить на практике множество ингибиторов рецепторных тирозинкиназ на основе малых молекул. В новом обзоре обобщили уже накопленные сведения об этих ингибиторах и о роли тирозинкиназ при развитии злокачественных новообразований. — Therapeutic advances of targeting receptor tyrosine kinases in cancer.
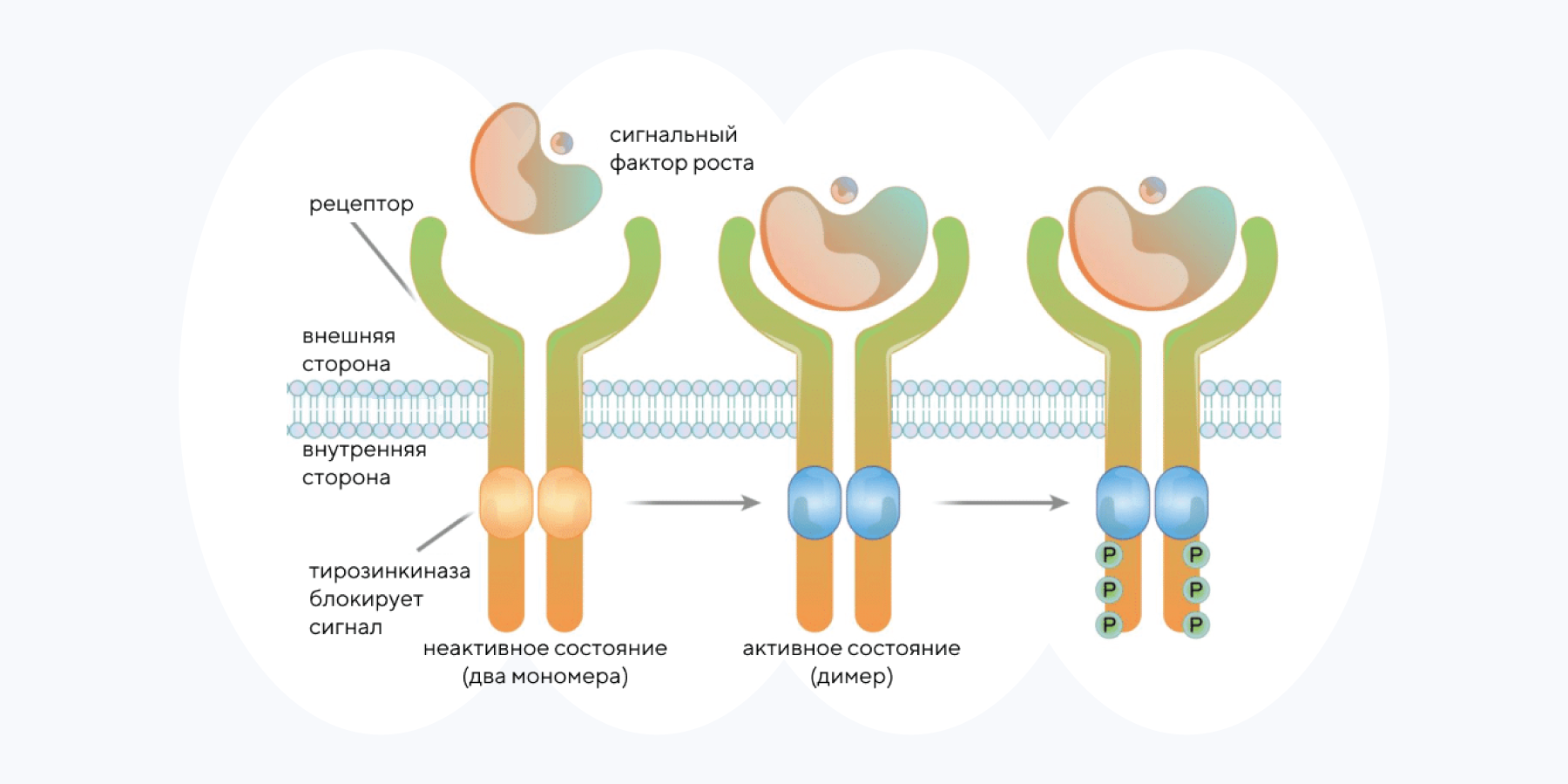
Механизм работы рецепторной тирозинкиназы. Источник: ResearchGate
При отсутствии связывания рецептора с сигнальным фактором роста тирозинкиназа блокирует связывание рецептора, который представляет собой два мономера. После связывания на мембране образуется димер, тирозинкиназа фосфорилируется, в результате чего рецептор переходит в активное состояние.
Аутоиммунные заболевания
Как предотвратить антителозависимое усиление инфекции
Обычно при проникновении вируса или другого патогена в организм происходит его связывание антителами, чтобы запустить иммунный ответ. Однако иногда этот процесс работает наоборот, и антитела, связываясь с вирусом, усиливают его проникновение в иммунные клетки и способствуют его репликации. В результате тяжесть инфекции усиливается. Однако эффект от этого феномена показан не только при вирусных, но и при бактериальных и грибковых инфекциях. В новой работе сфокусировались на механизмах, которые усиливают тяжесть инфекции, связанную с антителами, — обычно это происходит при неполной специфичности антител к патогенам. В случае когда речь идет о бактериях, антитела могут помогать их выживаемости, защищая бактериальные клетки от комплемент-зависимого уничтожения. Также в этой работе изучили роль аутоантител, которые усиливают патогенез инфекционных заболеваний. Все полученные результаты позволят разработать новые подходы к лечению инфекций и улучшить дизайн вакцин. — Mechanisms of antibody-dependent enhancement of infectious disease.
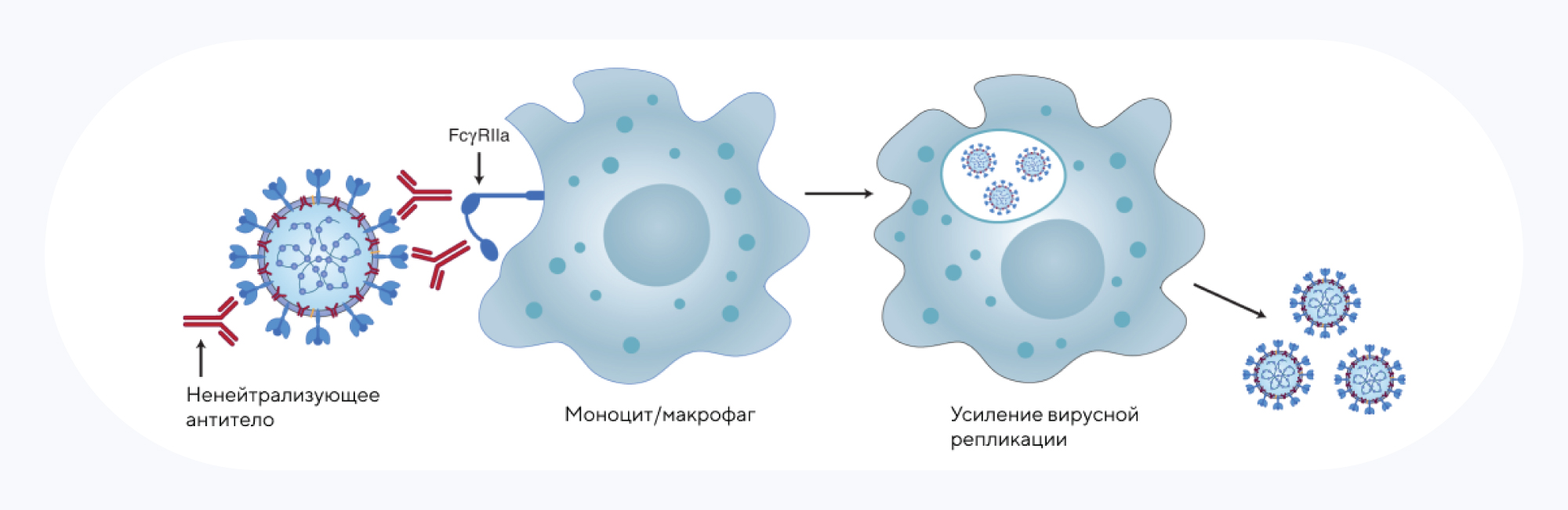
Источник: Nature Reviews Immunology
При антителозависимом усилении инфекции вирусы или другие патогены связываются с нейтрализующими или ненейтрализующими антителами, что способствует проникновению вируса в иммунную клетку и последующую вирусную репликацию.
Как укротить внеклеточные ловушки при ревматоидном артрите
ДНК надежно упакована внутри ядра клетки, но иногда ее целенаправленно выпускают наружу нейтрофилы — клетки врожденного иммунитета. Обычно это происходит в ответ на проникновение патогена, когда необходимо как можно скорее уничтожить опасность. Нейтрофилы выбрасывают сети из собственной ДНК вместе с белками — такие паутины называют NETs (neutrophil extracellular traps). Ловушка из ДНК опутывается вокруг патогена, а белки помогают в его уничтожении. Однако не всегда NETs помогают, а зачастую и осложняют ситуацию — особенно в случае избыточной активации нейтрофилов. В результате возникает воспаление и повреждение тканей организма. Недавно был обнаружен белок-ингибитор, который напрямую распознает NETs, — им оказался миелоидный лектин C (MICL, myeloid inhibitory C-type lectin-like). Эксперименты на мышах показали, что утрата или блокирование MICL запускает неконтролируемое образование NETs и развитие аутовоспалительных реакций. В случае ревматоидного артрита отсутствие MICL обостряет болезнь и вызывает патологии. Артрит — не единственное заболевание, течение которого связано с MICL, этот белок также важен при ингибировании NETs в случае волчанки и COVID-19. Получается, что активация MICL представляет собой значимый ауторегуляторный способ для контроля над внеклеточными ловушками в ряде аутоиммунных и инфекционных болезней. — Recognition and control of neutrophil extracellular trap formation by MICL.
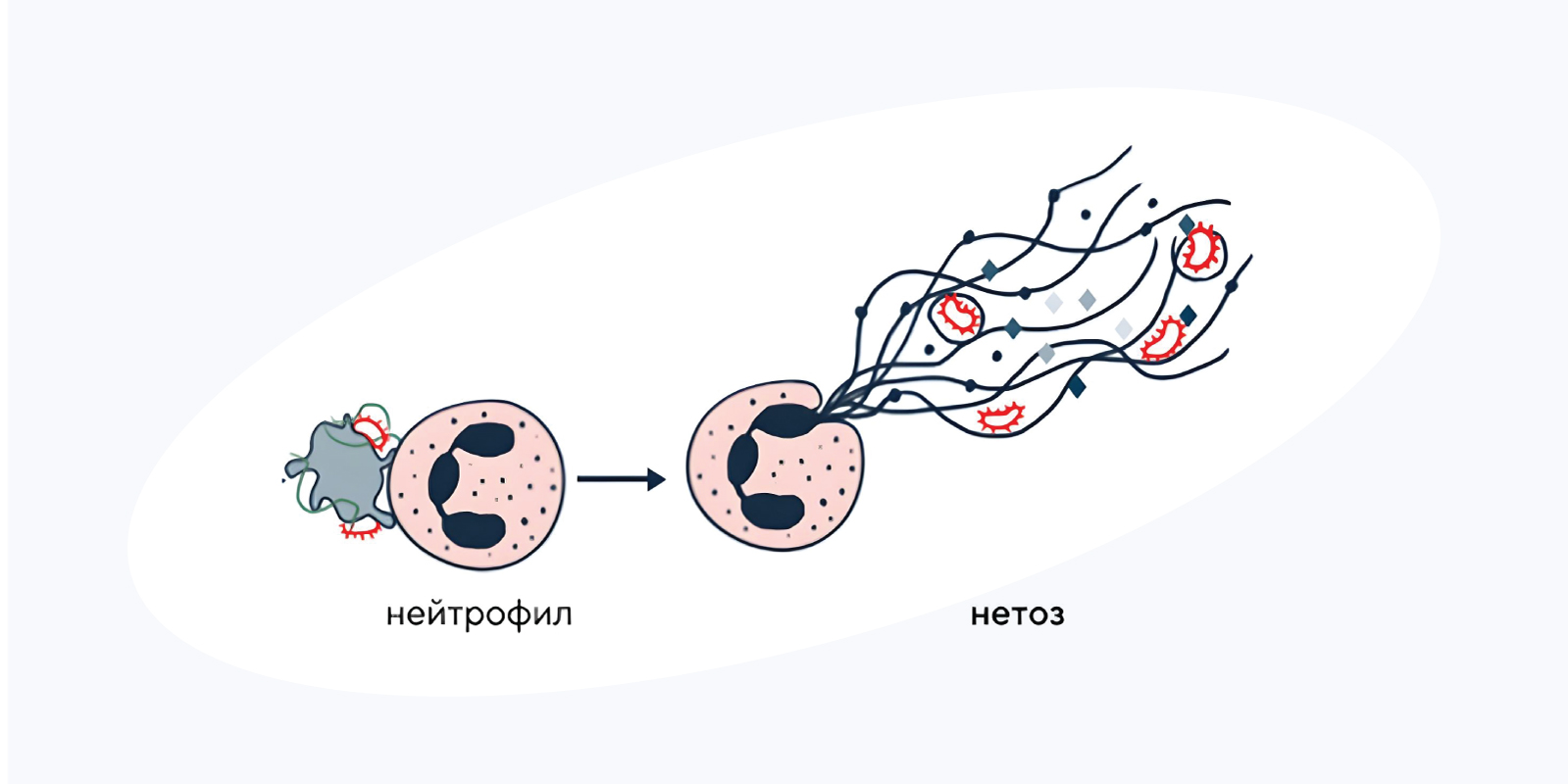
При встрече с патогеном нейтрофилы могут агрессивно отвечать на вторжение — выпускать наружу ловушки NETs из ДНК с белками. Источник: «Биомолекула»