Дайджест #19. Как одно небольшое изменение приводит к большим последствиям
Если вы считаете, что все клетки нашего организма имеют идентичный геном, вы ошибаетесь. На самом деле генетический материал, спрятанный в наших клетках, различается множеством вроде бы незаметных деталей — это явление называют мозаицизмом. К генетическому мозаицизму причастны в том числе и соматические однонуклеотидные варианты, когда на каком-то из участков ДНК происходит изменение отдельного нуклеотида на что-то иное. Но эти однонуклеотидные варианты — не просто интересный феномен: также они способны вносить свой вклад в развитие онкологических заболеваний. О том, как это происходит и что с этим делать, читайте в новом дайджесте.
Что заставляет опухоли мозга прогрессировать быстрее
Одно из наиболее распространенных злокачественных новообразований у женщин — рак шейки матки. Среди основны причин, которые провоцируют это заболевание, — инфицирование вирусом папилломы человека. Именно поэтому вакцинация от этого вируса считается одним из наиболее надежных способов профилактики. Однако не стоит забывать о том, что многие виды онкологических заболеваний связаны с генетикой, и рак шейки матки не исключение. Недавно удалось расшифровать роль одного из «генетических винтиков», способных вносить свой вклад в развитие этой болезни. Им стала кольцевая ДНК circ_ASH1L, роль которой в заживлении кожи ранее уже показали в другом исследовании. Однако на этот раз circ_ASH1L предстает с другой, негативной стороны: ее повышенная экспрессия усиливает пролиферацию, инвазию и миграцию раковых клеток в цервикальном канале, способствуя прогрессированию рака шейки матки. Исследователи из Уханьского университета (Китай) показали, что circ_ASH1L является так называемой «губкой» для микроРНК miR-1254, то есть включает в себя последовательности для распознавания и связывания с этой микроРНК. В результате miR-1254 лишается возможности реализовать свою регуляторную функцию — подавление избыточного синтеза рецептора CD36. В норме этот рецептор доставляет в клетку жизненно важные жирные кислоты, поэтому нет ничего удивительного в том, что для некоторых типов опухолей характерна повышенная экспрессия CD36 — это и приводит к усилению пролиферации и метастазирования таких опухолевых клеток. Таким образом, удалось показать, что circ_ASH1L опосредованно увеличивает количество CD36 на поверхности опухолевых клеток, повышая агрессивность рака шейки матки. Эксперименты на мышиных моделях показали, что подавление транскрипции этой кольцевой РНК в клетках рака шейки матки понижает их способность к образованию опухолей. Возможно, circ_ASH1L станет потенциальной мишенью для лечения этого вида рака. — Has_circ_ASH1L acts as a sponge for miR-1254 to promote the malignant progression of cervical cancer by targeting CD36.
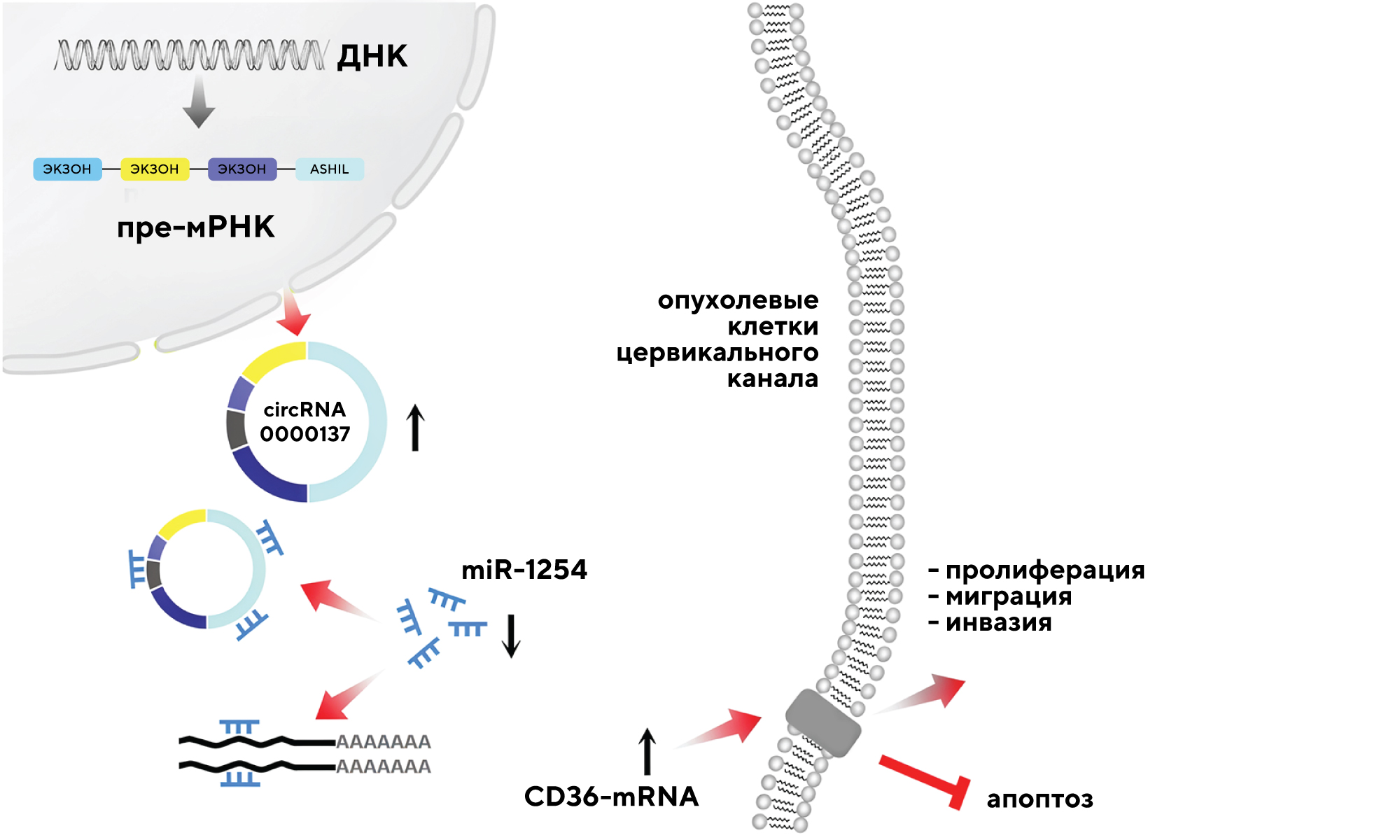
В запуске опухолевых процессов при раке шейки матки участвует кольцевая РНК circ_ASH1L, которая захватывает и связывает «полезную» микроРНК 1254 (miR-1254), не давая той достаточно эффективно ингибировать синтез рецептора CD36. Этот мембранный белок в норме доставляет в клетку жизненно важные жирные кислоты. В результате связывания miR-1254 экспрессия CD36 повышается, что способствует усилению агрессивности рака шейки матки. Источник: Nature Cancer Gene Therapy
Какие молекулярные механизмы помогают сосудистым опухолям уходить от терапии
От злокачественного перерождения не застрахована ни одна ткань организма, в том числе эндотелий кровеносных сосудов. Среди новообразований кровеносной системы встречаются как доброкачественные — гемангиомы, так и злокачественные опухоли — ангиосаркомы. Последние обычно отличаются крайне неблагоприятными прогнозами с предрасположенностью к метастазированию, из-за чего часто становятся объектом исследований. Недавно группе американских ученых удалось чуть глубже заглянуть под молекулярную изнанку онкогенеза этой группы опухолей. В фокус исследования попала мутация H1047R в хорошо известном гене PIK3CA. Благодаря этой мутации в клетках гемангиомы повышается устойчивость к одному из ингибиторов фосфатидилинозитол-3-киназы (PI3K), алпелисибу, специфично подавляющему субъединицу РI3Кα. Показано, что мутация H1047R опосредованно усиливает экспрессию генов ряда цитокинов, в числе которых IL-6, IL-8 и MCP-1 (CCL-2). Также мутация меняет метаболические пути клетки, активируя пути гликолиза и клеточного дыхания. Это характерно для многих опухолей, развивающихся в условиях гипоксии — например, для рака поджелудочной железы, о чем мы писали в прошлом дайджесте на основе статьи из Nature. Авторы статьи выражают надежду, что их открытие поможет развить новые подходы к персонализированной терапии ангиосарком с учетом индивидуальных мутаций в ключевых генах пациентов. — PIK3CA mutation fortifies molecular determinants for immune signaling in vascular cancers.
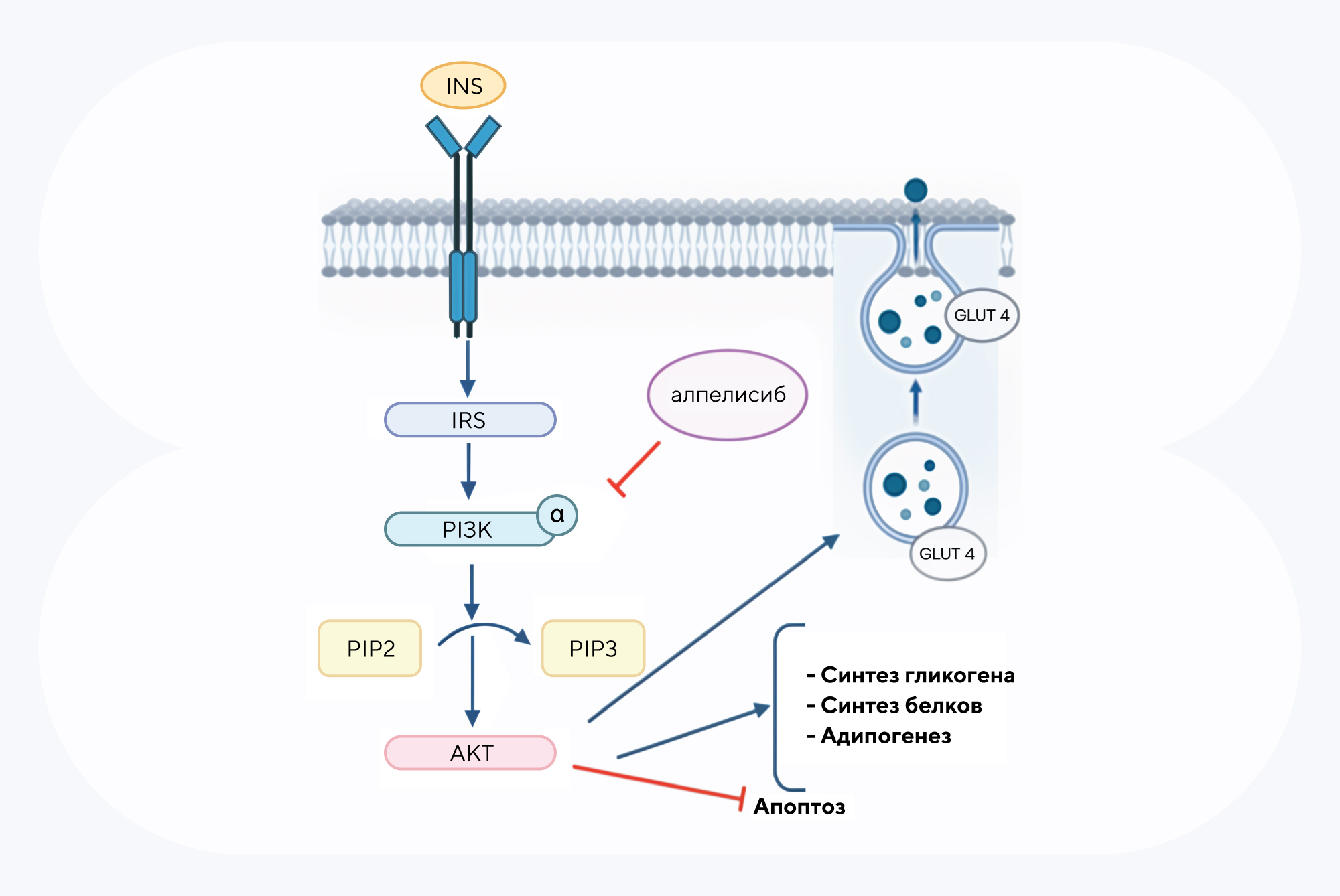
Механизм действия алпелисиба в сигнальном пути PI3K, который запускается инсулином. INS — инсулин, IRS — инсулиновый рецептор, PI3K — фосфатидилинозитол-3-киназа, PIP2 — фосфатидилинозитол 4,5-бисфосфат, PIP3 — фосфатидилинозитол (3,4,5)-трифосфат, AKT — протеинкиназа B, GLUT4 — переносчик глюкозы 4. Источник: ResearchGate
Обнаружена потенциальная мишень для лечения гепатоцеллюлярной карциномы
Белок FBXO22 — один из многочисленных участников процесса канцерогенеза. Несколько лет назад уже была описана его роль в развитии рака груди и рака легких. Но только этими опухолями дело не ограничивается — изменение экспрессии гена FBXO22 связано с многими другими злокачественными новообразованиями. Например, в недавнем исследовании изучили роль этого белка в онкогенезе гепатоцеллюлярной карциномы — самого распространенного типа рака печени. Исследования на клеточных и животных моделях показали, что повышение уровня FBXO22 тесно связано с количеством опухолей и их метастазированием. Выяснилось, что FBXO22 убиквитинирует один из белков 40S субъединицы рибосомы — RPS5, что приводит к его деградации в протеасоме. Снижение уровня RPS5, в свою очередь, активирует сигнальный путь PI3K/AKT, который повышает уровень фактора гипоксии HIF-1α и фактора роста эндотелия сосудов VEGF-A. Ожидаемо, ингибирование экспрессии FBXO22 с помощью малой «шпилечной» РНК, доставленной AAV8, привело к улучшению выживаемости мышей в модели гепатоцеллюлярной карциномы, а также повысило эффективность одного из наиболее популярных противоопухолевых препаратов — ленватиниба, ингибитора рецепторов упомянутого фактора роста эндотелия сосудов VEGF. — FBXO22 promotes HCC angiogenesis and metastasis via RPS5/AKT/HIF-1α/VEGF-A signaling axis.
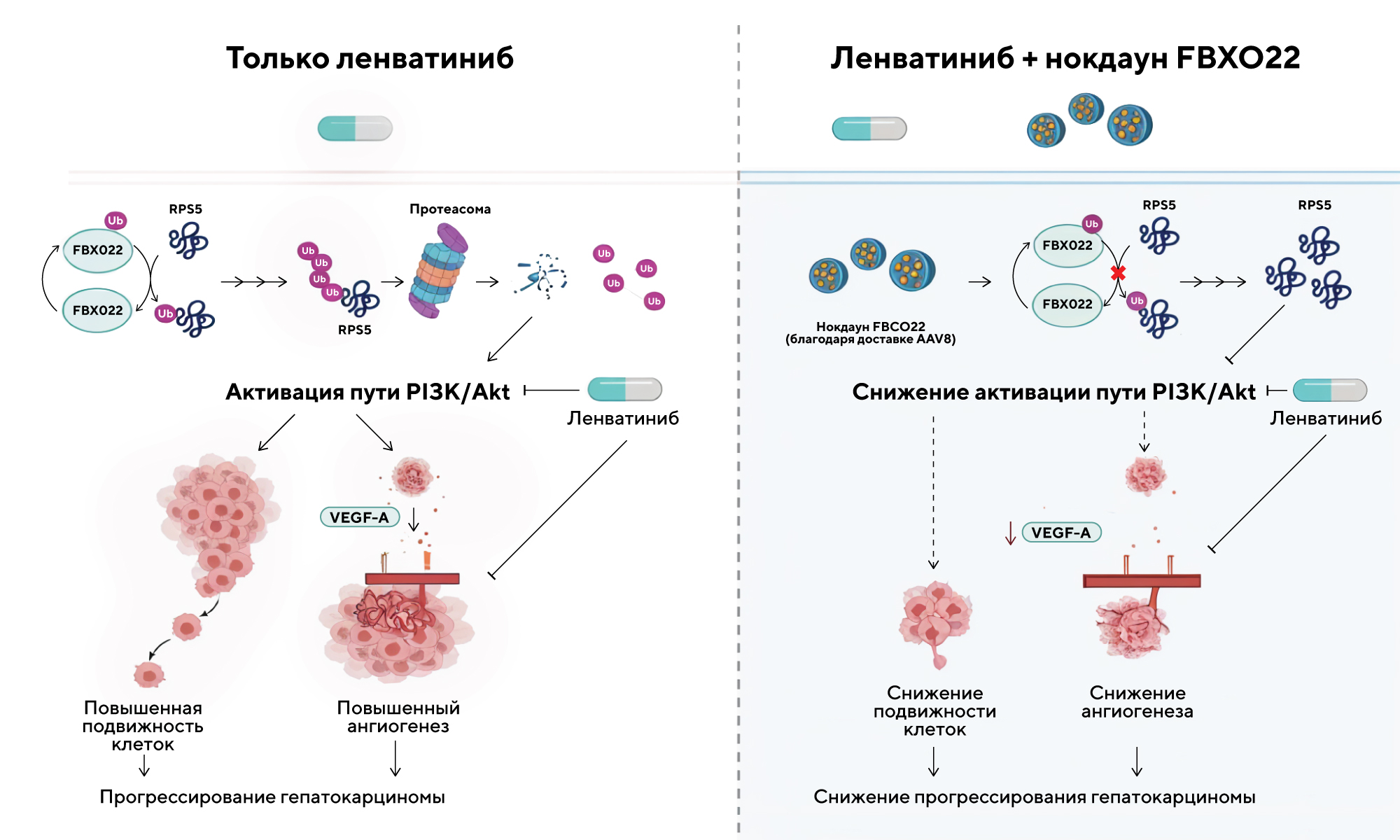
Схема каскада в сигнальном пути FBXO22/RPS5/AKT/HIF-1α/VEGF-A, который участвует в ангиогенезе и метастазировании. В случае нокдауна («выключения») гена, кодирующего белок FBXO22, повышается эффективность лечения гепатоцеллюлярной карциномы с помощью ленватиниба. Источник: Cancer Gene Therapy
Как однонуклеотидные варианты влияют на развитие нейробластомы
В случае когда на каком-то из участков ДНК меняется один нуклеотид в определенном положении — происходит вставка, удаление или какая-либо точечная перестройка — говорят о возникновении в этом месте соматического однонуклеотидного варианта (somatic single nucleotide variant, SNV). За последнее время накопились данные о том, что SNV в цис-регуляторных элементах могут быть потенциальными виновниками рака. Исследователи из Италии решили сфокусироваться на некодирующих SNVs, способных приводить к развитию нейробластомы. Эксперименты, проведенные с помощью CRISPR/Cas, показали: появление таких SNVs влияет на транскрипционную активность двух цис-регуляторных элементов, изменяя связывание сигнальных белков STAT3 и SIN3A. В результате снижается экспрессия генов CTTNBP2 и MCF2L, которые считаются супрессорами опухоли мозга. Получается, что некодирующие SNVs могут выступать в роли драйверов онкогенеза, запуская процессы перерождения клеток и дальнейшего развития нейробластомы. Эти результаты подсвечивают перспективы терапии опухоли мозга с помощью молекулярно-генетических механизмов «выключения» или блокирования SNVs. — Regulatory non-coding somatic mutations as drivers of neuroblastoma.
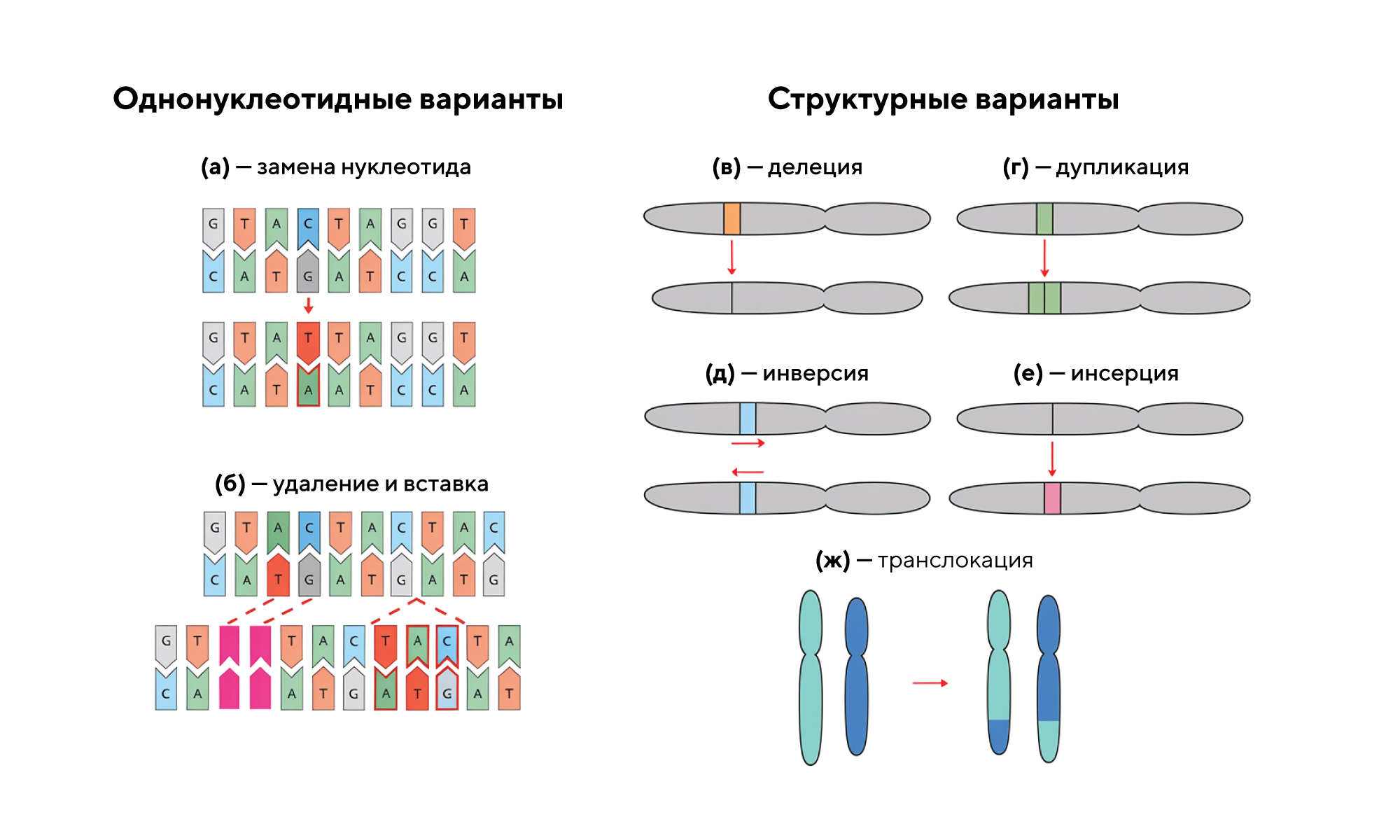
На рисунке показаны виды однонуклеотидных (SNVs) и структурных вариантов:
(а) — замена нуклеотида (цитозина на тимин); (б) — так называемые индели — Indels (от insertion or deletion) — короткие вставки или удаления в геноме; (в) — делеция, то есть потеря участка хромосомы; (г) — дупликация, то есть удвоение части хромосомы; (д) — инверсия, то есть поворот части хромосомы на 180 градусов; (е) — инсерция, то есть вставка части хромосомы; (ж) — транслокация, то есть перенос участка хромосомы на другую хромосому. Источник: ResearchGate
Как нитрит натрия связан с метастазированием
Плоскоклеточная карцинома языка — это разновидность злокачественного вида рака полости рта, который часто сопровождается ранним лимфатическим метастазированием. Накопленные данные показывают, что у пациентов с таким диагнозом проявляется плохой прогноз заболевания с низким пятилетним показателем выживаемости. Вот почему важно исследовать патогенез этого вида рака и искать возможные причины его появления. Недавно китайским исследователям удалось идентифицировать неожиданного участника, вероятно, связанного с развитием плоскоклеточной карциномы языка. Им стал нитрит натрия — более широко это соединение известно как пищевая добавка Е250, которую используют при производстве мясных полуфабрикатов.
Результаты исследования не показали прямой взаимосвязи между нитритом натрия и запуском процесса канцерогенеза, поэтому демонизировать Е250 пока рано. Однако ученым удалось проследить взаимосвязь между фенотипическими изменениями клеток языка с добавлением к клеточным культурам нитрита натрия. Изменения были связаны с активацией белка, который опосредованно блокирует другой связывающий белок, CREB1. В результате этого запускается экспрессия гена, кодирующего белок CD68 — специфичный маркёр макрофагов. В клетках опухолей CD68 способен связываться с селектинами сосудистого эндотелия и распространяться по всему организму. Получается, что в результате такой цепочки взаимодействий нитрит натрия можно косвенно считать вероятным инициатором процесса метастазирования. В этом же исследовании удалось показать, что блокирование активности CREB1 — за счет нокаута гена или путем ингибирования — снижает способность клеток плоскоклеточной аденокациномы к миграции и подавляет экспрессию CD68. — Sodium nitrite orchestrates macrophage mimicry of tongue squamous carcinoma cells to drive lymphatic metastasis.
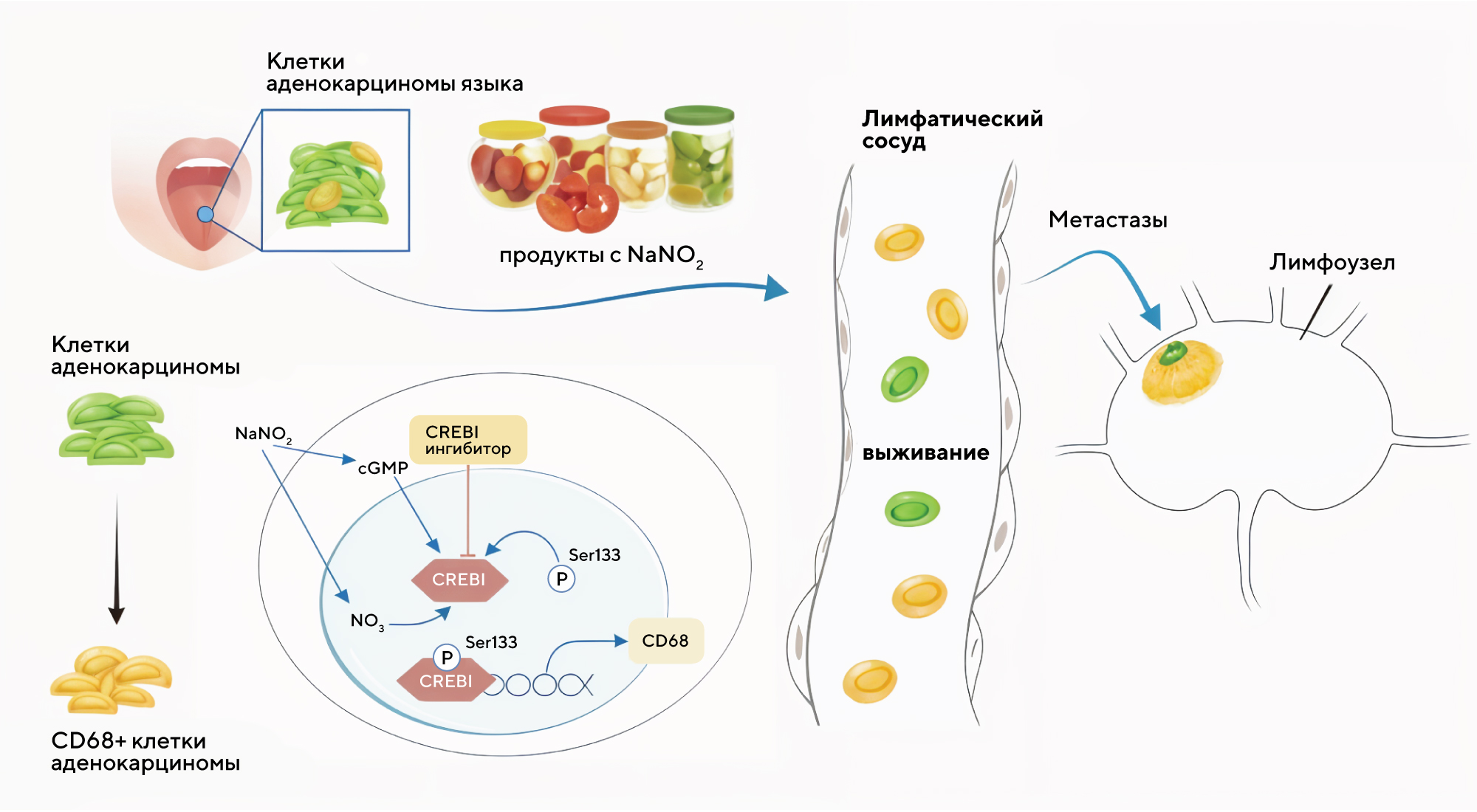
В исследовании обнаружили вероятную роль нитрита натрия в развитии метастазирования в лимфатических узлах при плоскоклеточной карциноме языка. Источник: British Journal of Cancer