
Дайджест #18. «Малые, да удалые» — как везикулы опухолевых клеток помогают в борьбе с раком
Многие клетки нашего организма производят везикулы — крошечные пузырьки, которые выполняют важные функции. Опухолевые клетки не исключение: они тоже выделяют внеклеточные везикулы с разными соединениями. До недавнего времени выделение везикул в опухолях считалось плохим признаком и свидетельствовало о росте и разрастании метастазов. Но оказалось, что всё не так однозначно: бывают случаи, когда внеклеточные везикулы, наоборот, подавляют метастазирование. Подробнее о секретном ингредиенте этих «хороших» везикул читайте в новом дайджесте.
Что заставляет опухоли мозга прогрессировать быстрее
Самой распространенной первичной опухолью мозга считается глиома. Для одной из разновидностей этого многогранного образования, связанной с мутациями в ферменте изоцитратдегидрогеназе, характерен исходно медленный рост, но неизбежное прогрессирование вплоть до летального исхода. Недавно команде исследователей из MIT удалось выяснить, что разные стадии этого заболевания характеризуются переходом от подавления экспрессии определенных генов с помощью эпигенетических механизмов к прямым модификациям генома клеток (мутациям в ДНК).
Так, в клетках медленно растущей опухоли экспрессия генов сигнальной цепи интерферона (которые в норме помогают клетке бороться с вирусами и злокачественным перерождением) подавлена с помощью избыточного метилирования ДНК, при участии той самой мутантной изоцитратдегидрогеназы или других ферментов. Переход же опухоли в агрессивное состояние часто ассоциирован с изменением последовательности самих генов, отвечающих за подавление онкогенеза: интерфероновых и многих других; при этом их метилирование часто теряется за ненадобностью. Мутации накапливаются подобно снежному кому и приводят к существенным метаболическим перестройкам. Итог неутешителен — в конце концов из относительно пассивной группы клеток возникает агрессивная опухоль. Выводы исследования могут дать толчок к развитию нового терапевтического направления, связанного с эпигенетическим изменением опухолей мозга на ранних стадиях. — Evolving cell states and oncogenic drivers during the progression of IDH-mutant gliomas.
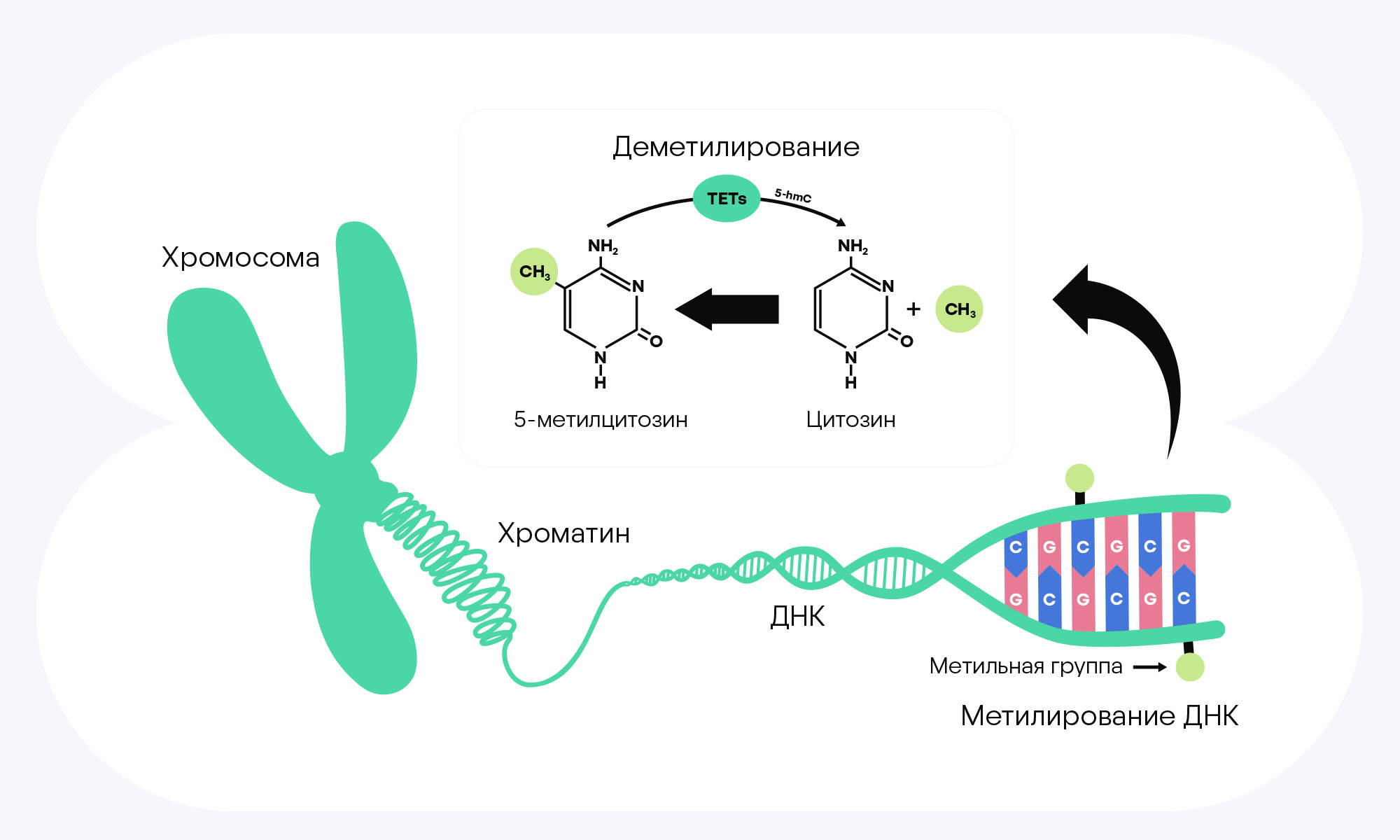
Схема молекулярных механизмов метилирования и деметилирования ДНК. В норме метилирование ДНК — это нормальный процесс, при котором изменяется модификация молекулы ДНК без изменения ее нуклеотидной последовательности. Однако в опухолевых клетках часто происходят нарушения метилирования ДНК, при которых снижается уровень метилированных цитозинов, а также происходит гиперметилирование CpG-островков внутри промотора гена ZNF154 (zinc-finger protein 154). Источник: MDPI
Как необычные везикулы подавляют метастазирование
Важную роль в передаче межклеточных сигналов играют внеклеточные везикулы. Эти крошечные пузырьки выделяются клетками и в норме, и при патологии. Традиционно считалось, что секреция внеклеточных везикул опухолевыми клетками — это плохой знак, который свидетельствует о прогрессировании заболевания и распространении метастазов. Однако недавно выяснилось, что не все так однозначно: внеклеточные везикулы опухолевых клеток, которые несут на своей поверхности фрагменты ДНК, наоборот, активируют иммунный ответ и запускают секрецию цитокинов, блокируя метастазирование. Необычной оказалась и структура этих везикул: выяснилось, что они ассоциированы с гистонами, отличающимися от привычных модификаций ядерных гистонов — они были сильно метилированы и слабо ацетилированы. Чтобы оценить влияние внеклеточных везикул с непривычной структурой ДНК, исследователи нокаутировали, то есть «выключили» гены, связанные с упаковкой фрагментов ДНК в везикулы. Выяснилось, что утрата этих везикул, обогащенных ДНК, приводила к гораздо большей степени метастазирования, по крайней мере это удалось показать на мышиных моделях рака молочной железы и колоректального рака. Также в модели колоректального рака обнаружился необычный ответ: клетки Купфера (резидентные макрофаги печени) поглощали везикулы с ДНК, в результате чего активировались реакции секреции цитокинов, образования лимфоидных структур — и все это приводило к подавлению метастазирования в печени. Все эти результаты подсвечивают важную роль внеклеточных везикул с ДНК для терапии рака, в особенности связанного с распространением метастазов. — Unique structural configuration of EV-DNA primes Kupffer cell-mediated antitumor immunity to prevent metastatic progression.
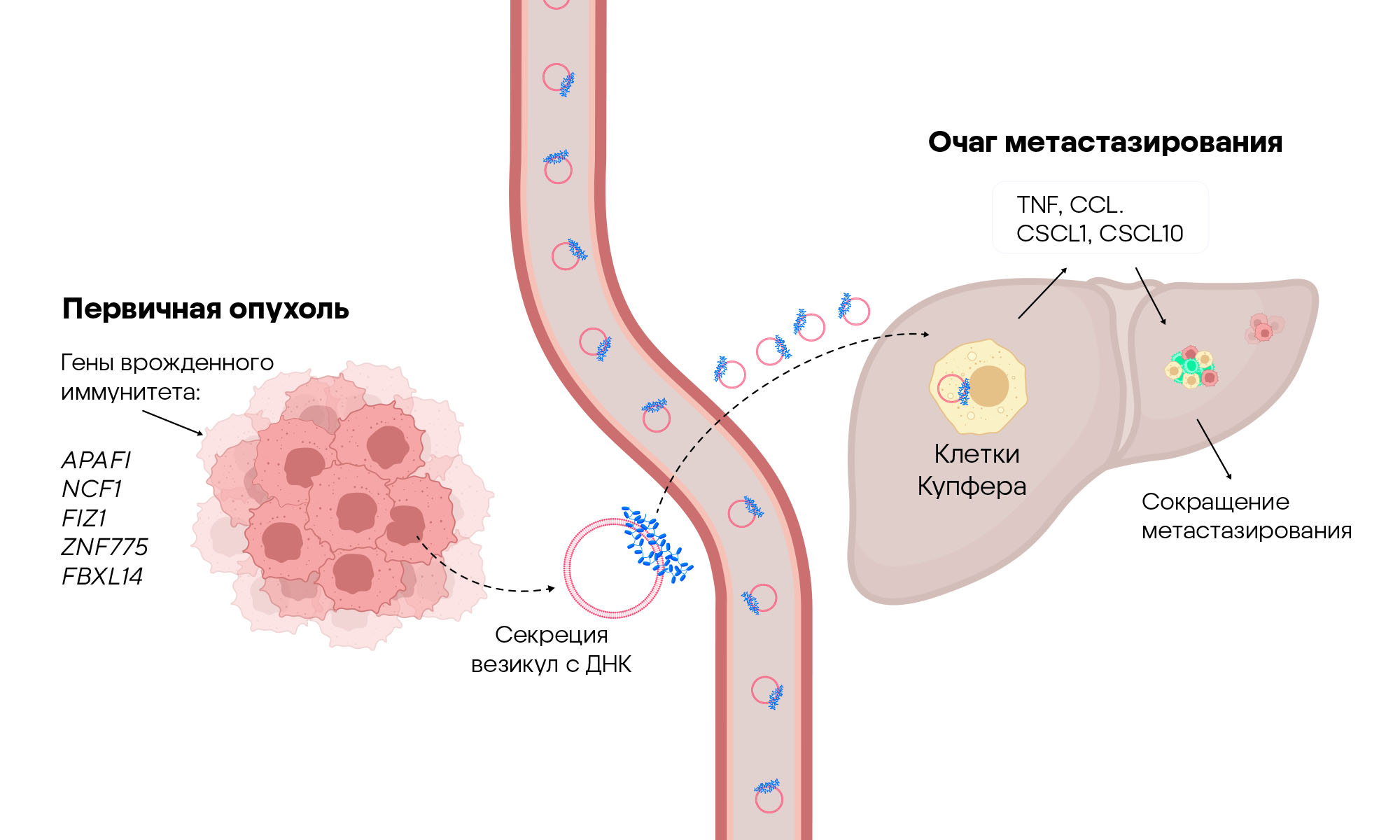
Гены врожденного иммунитета, среди которых NCF1 (цитозольный фактор нейтрофилов 1) и APAF1 (фактор активации апоптотической протеазы 1), регулируют упаковку ДНК во внеклеточные везикулы. После миграции этих везикул в печень их поглощают клетки Купфера, в результате чего запускаются реакции, которые приводят к значительному сокращению количества метастазов. Источник: адаптировано из Nature Cancer
Антитела для поддержки CAR-T-терапии при миеломе
Многие пациенты с миеломой сталкиваются с рецидивом болезни после курса лечения. Такой вид рака, который не поддается лечению, называют рефрактерным. Даже если применять клеточную CAR-T-терапию для лечения рецидивирующей и рефрактерной меланомы — а этот вид лечения уже показал значительные результаты в предыдущих исследованиях — болезнь все равно возвращается. Однако надежда на борьбу с рецидивами все же есть — ключом к спасению могут стать биспецифические антитела. Международное исследование, которое проводили при участии 139 пациентов с рефрактерной меланомой, показало положительный ответ на лечение антителами после предшествующей CAR-T-терапии. Всего оценивали влияние нескольких групп препаратов, среди которых были талкветамаб (Talvey®), теклистамаб, комбинации иммуномодуляторов, ингибиторы протеасом и антитела против CD38. Лучший ответ показали талкветамаб и теклистамаб. Однако и за этим дело не стало: продолжительность ответа на лечение после CAR-T-терапии и общую выживаемость удалось значительно улучшить при использовании биспецифических антител. Эти результаты могут способствовать тому, чтобы биспецифики включили в стандарт лечения после CAR-T-терапии при рецидивирующей и рефрактерной меланоме. — Bispecific antibodies targeting BCMA or GPRC5D are highly effective in relapsed myeloma after CAR T-cell therapy.
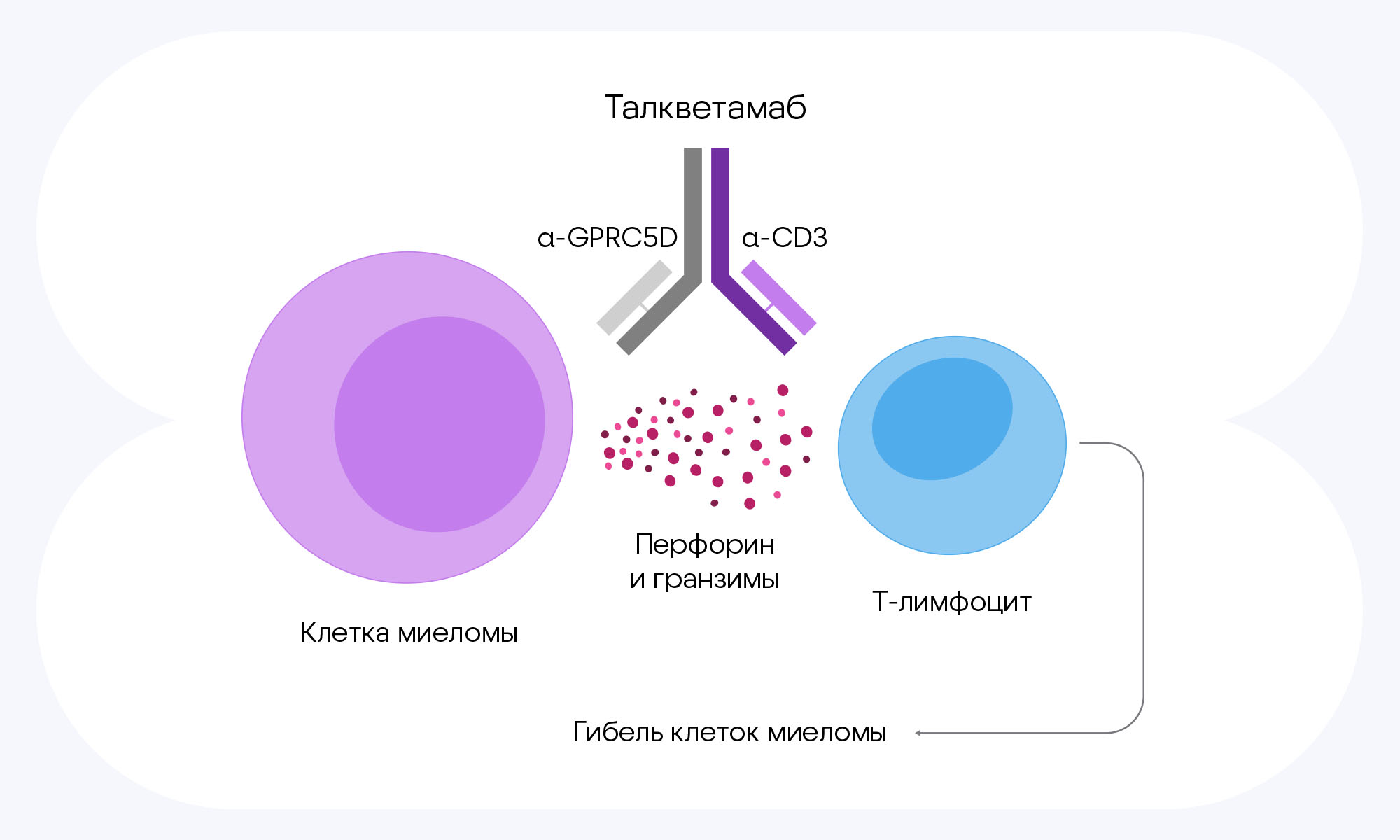
Один из препаратов для лечения рецидивирующей и рефрактерной миеломы — талкветамаб. Это гуманизированное биспецифическое моноклональное антитело (так называемый «привлекающий T-клетки биспецифический активатор», BiTE, bispecific t cell engager) против поверхностного антигена T-клеток CD3 и ассоциированного с опухолью антигена GPRC5D (член D группы 5 семейства C рецепторов, связанных с G-белками). Этот препарат назначают в качестве пятой линии терапии пациентам с рецидивирующей меланомой. Источник: адаптировано из Multiple Myeloma Hub
Блокада иммунных чекпоинтов для стимуляции Т-лимфоцитов
Разработка антител — ингибиторов контрольных точек иммунной системы является перспективным направлением в иммунотерапии рака. Часто опухоли уходят из-под иммунного контроля и, даже будучи «набиты» до отказа иммунными клетками, почему-то продолжают расти. Это происходит из-за повышенной экспрессии определенных генов, которые в норме точечно подавляют активность Т-лимфоцитов в отношении собственных клеток (для предотвращения аутоиммунных реакций). Самой известной парой таких молекул на службе у опухолей можно считать PD-1 и PD-L1 — белок «программируемой смерти», представленный на Т-лимфоцитах, и его лиганд, которые в большом количестве обнаруживаются на многих опухолевых клетках. На фармацевтическом рынке существует большое количество препаратов, нацеленных на PD-1 или PD-L1, блокирующих их связывание друг с другом, для борьбы с разными видами рака. Однако в недавнем исследовании решили изучить блокаду сразу двух иммунных чекпоинтов — PD-1 и TIGIT, еще одной хорошо известной мишени для терапии онкологических заболеваний. На мышиной модели удалось показать, что комбинированная блокада PD-1 и TIGIT приводила к клональной экспансии CD8+ Т-лимфоцитов, специфичных к опухолевым антигенам — это когда конкретная клетка многократно делится и образует многочисленную популяцию таких же клеток, в данном случае нацеленных на опухолевые клетки. При этом исходно клоны Т-лимфоцитов возникали, как и положено, из клеток-предшественников в лимфоузлах, а затем с током крови достигали опухоли и уже там дифференцировались в эффекторные Т-клетки. Таким образом, совместная блокада обоих чекпоинтов привела к изменению спектра популяции противоопухолевых Т-лимфоцитов и определению их конечного фенотипа в самой опухоли. Впрочем, несмотря на неплохие результаты относительно совместного применения антител против этих двух мишеней, называть это успехом в лечении рака пока рано: в других недавно опубликованных исследованиях обнаружились не столь радужные перспективы эффективности использования анти-TIGIT и анти-PD-1/PD-L1 на больших выборках. — TIGIT and PD-L1co-blockade promotes clonal expansion of multipotent, non-exhausted antitumor T cells by facilitating co-stimulation.
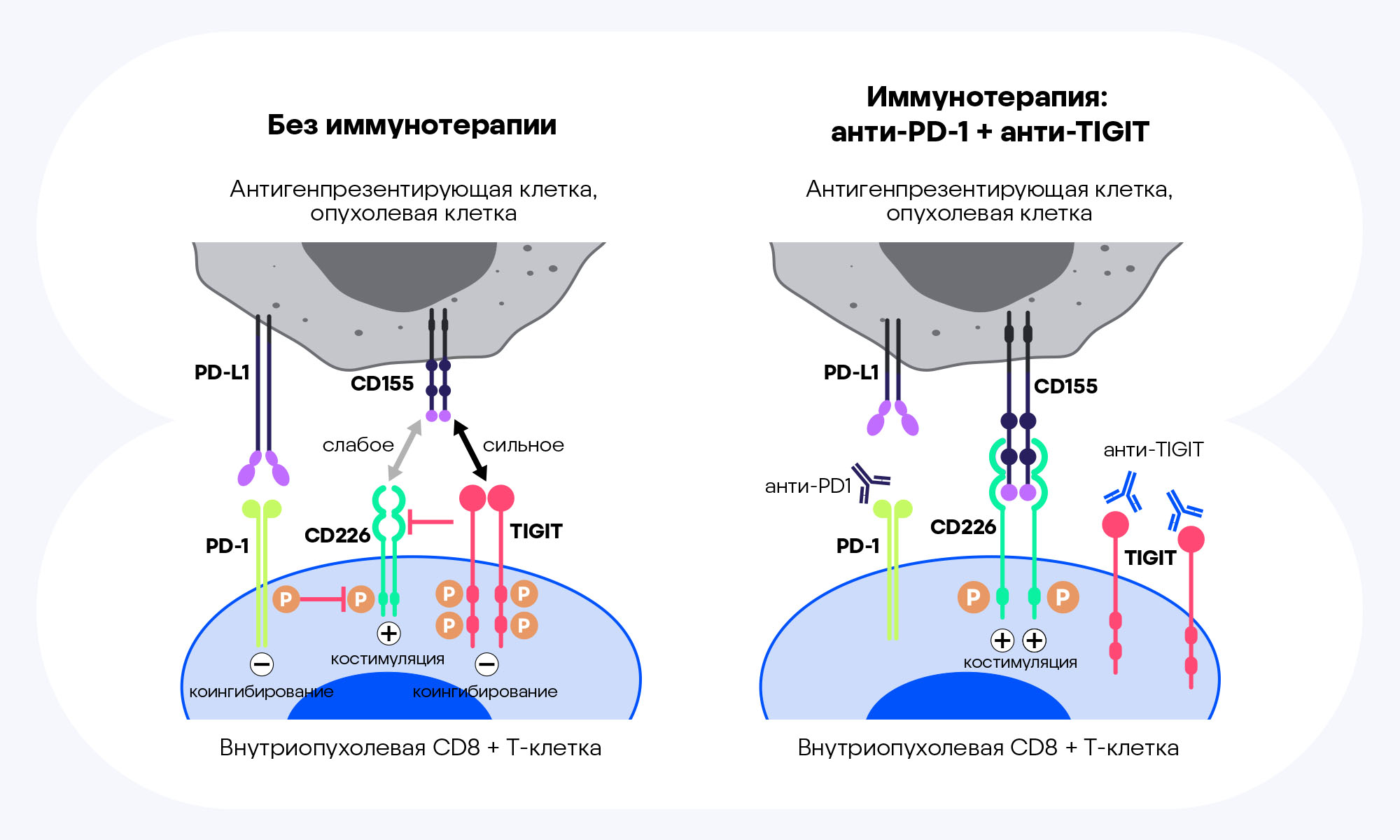
Двойная блокада TIGIT и PD-1 оказывает синергетическое действие на внутриопухолевые СD8+ Т-клетки. Слева — действие TIGIT и PD-1 в отсутствие иммунотерапии: совместная передача сигналов посредством рецептора CD226 подавляется как сигналами TIGIT, так и PD-1. Справа — блокирование TIGIT и PD-1 антителами: совместная блокада PD-1 и TIGIT синергически восстанавливает костимулирующую передачу сигналов CD226. Источник: адаптировано из ResearchGate
Как настроить иммунные клетки против рака
Твердую оболочку мозга, граничащую со спинномозговой жидкостью (ликвором), населяют различные иммунные клетки, задача которых — обеспечить периферический иммунологический барьер. В результате такой защиты удается не пропускать из кровотока в нижележащие оболочки мозга разный молекулярный мусор — это особенно важно из-за того, что мозг является иммунопривилегированным органом с ограниченной активностью иммунной системы. В недавнем исследовании ученые из Китая показали, что макрофаги твердой оболочки мозга могут мигрировать в спинномозговую жидкость с помощью матриксной металлопротеиназы MMP14 и вносить свой вклад в распространение туда же опухолевых метастаз. Более того, оказалось, что переход самих макрофагов обязательно требует наличия растворимого фосфопротеина SPP1 (также известного как остеопонтин), секретируемого опухолевыми клетками в основном очаге для подавления активности иммунных клеток микроокружения. Блокируя ось SPP1-MMP14, китайским исследователям удалось остановить рост и развитие опухоли, предотвратить переход макрофагов в ликвор и увеличить время жизни мышей в модели метастазирования в мозговые оболочки. Эти данные позволяют по-новому взглянуть на сложность и неочевидность отдаленных взаимодействий между опухолями и клетками врожденного иммунитета мозговых оболочек. — Dura immunity configures leptomeningeal metastasis immunosuppression for cerebrospinal fluid barrier invasion.
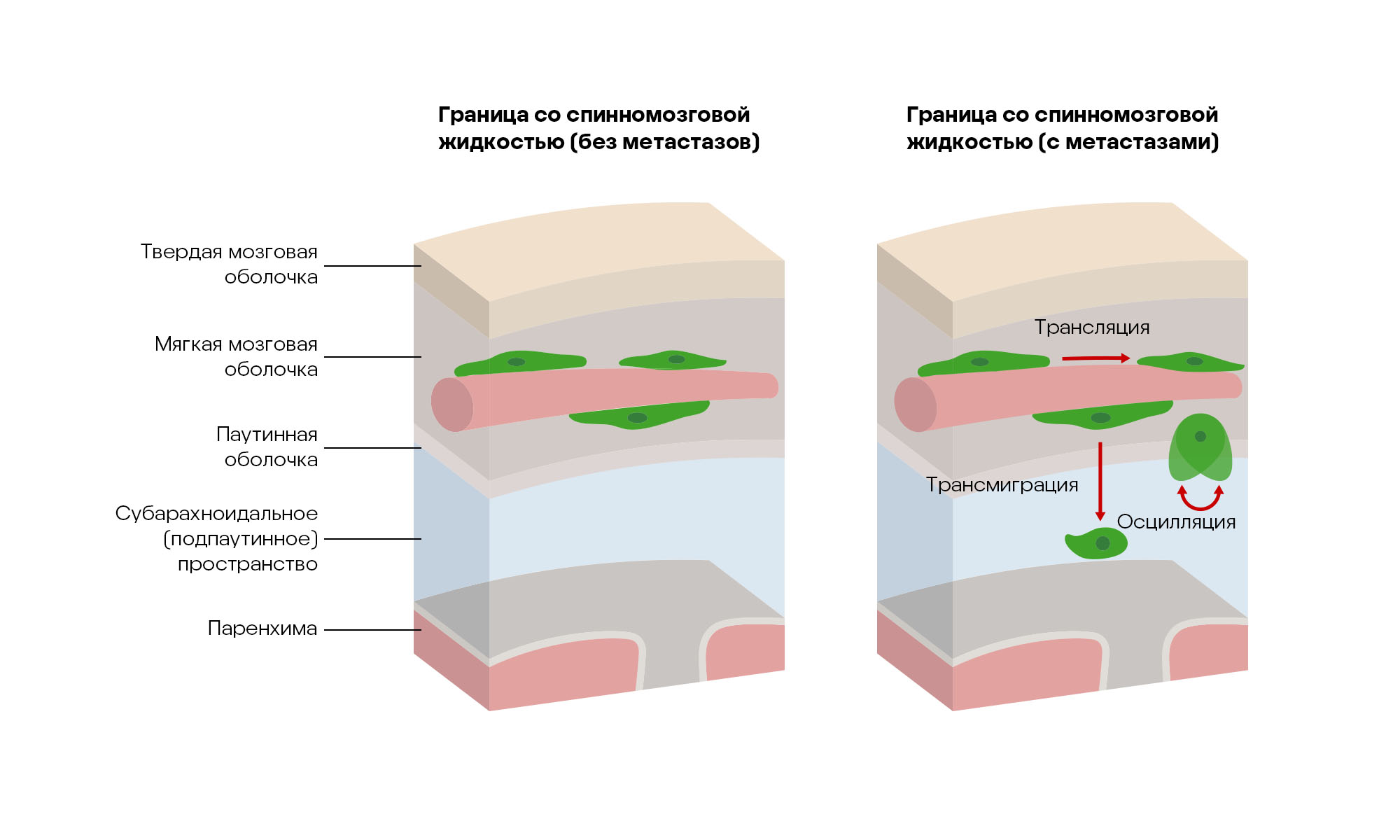
Схема миграции макрофагов твердой оболочки мозга в спинномозговую жидкость. Источник: адаптировано из Nature Cancer
Как снизить агрессивность опухоли поджелудочной железы
Злокачественные опухоли поджелудочной железы — одни из самых устойчивых к терапии видов рака на сегодняшний день, в первую очередь из-за образования «капсулы» из соединительной ткани вокруг себя и плохого насыщения кровеносными сосудами. В недавнем исследовании группа ученых из Китая показала, что опухоль обращает эти факторы себе на пользу с помощью белка ITGA3 — α3-субъединицы интегринов (белков межклеточной адгезии), ассоциированной с прогрессированием заболевания и плохим прогнозом выживаемости пациентов. Механизм состоит в аутокринной активации ITAG3 на опухолевых клетках с помощью выделяемого этими же клетками коллагена. Это запускает сигнальный путь FAK/PI3K/AKT/mTOR и приводит к экспрессии хорошо известного фактора гипоксии HIF1α, а также гена c-Myc — двух ключевых активаторов гликолитического пути клетки. С помощью переключения на этот метаболический путь опухоль повышает устойчивость к недостатку кислорода и питательных веществ, продолжает расти и в конечном итоге переходит к метастазированию в другие органы. Блокада любого из этих двух белков (коллагена или ITGA3) приводила к инактивации пути FAK/PI3K/AKT/mTOR и уменьшала агрессивность опухоли в животной модели. — ITGA3 promotes pancreatic cancer progression through HIF1α- and c-Myc-driven glycolysis in a collagen I-dependent autocrine manner.
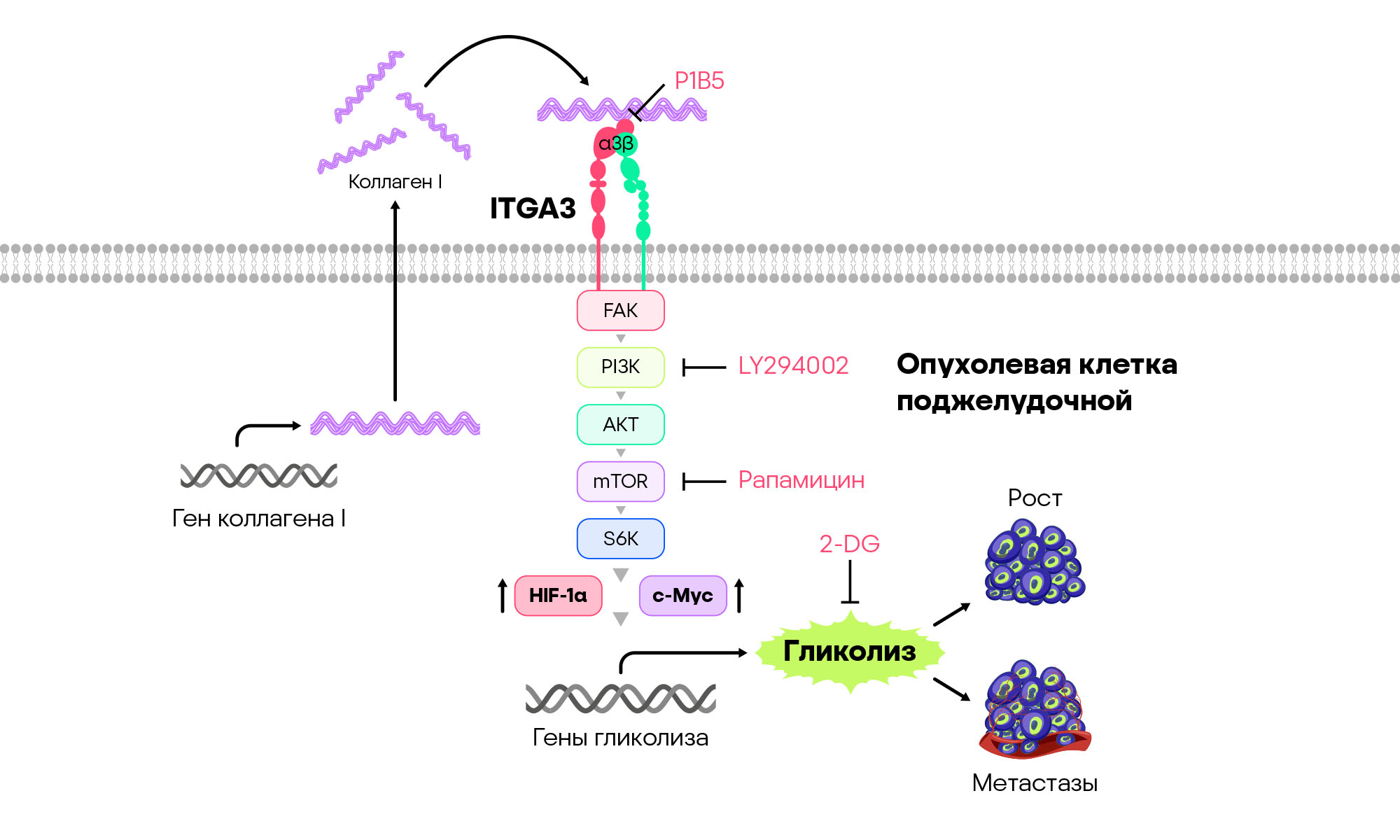
Схема сигнального пути, который запускает рост и прогрессирование опухоли поджелудочной железы. Источник: адаптировано из Nature Cancer