Научный дайджест #31: открыть путь в клетки с помощью «мини-ключа»
Использование целого ряда методов генной терапии ограничено размерами белков, которые просто не могут проникнуть внутрь целевых клеток. На помощь может прийти компактная система генетического редактирования — TnpB-ωRNA. Эта конструкция, которая состоит из белка TnpB и его «РНК-наводчика», представляет собой миниатюрный инструмент, который умеет активировать нужные гены и основания. О том, как работает эта система, а также о других прорывах в генетических технологиях и молекулярной онкологии, читайте в нашем новом дайджесте.
Как перепрограммировать Т-лимфоциты прямо в организме
Модифицированные Т-лимфоциты, перепрограммированные для экспрессии химерных антигенных рецепторов (CAR) или Т-клеточных рецепторов (TCR), в свое время произвели настоящую революцию в лечении опухолевых заболеваний. На сегодняшний день эти измененные клетки изучаются в качестве терапевтических средств для лечения некоторых заболеваний. Однако остается проблема производства модифицированных Т-лимфоцитов: их получение ex vivo — процесс довольно длительный и дорогостоящий.
Перспективным направлением для преодоления этого барьера может стать новая работа международной команды исследователей. Так, с помощью двухвекторной системы, объединяющей технологию CRISPR-Cas9 и донорную ДНК, удалось точечно встроить CAR-трансген в строго определенный локус Т-лимфоцитов in vivo, минуя этапы внешнего выращивания и модификации клеток в лаборатории. В результате у гуманизированных мышей, на которых проводили исследование, удалось получить терапевтический уровень CAR-T-клеток in vivo, которые сдерживали рост опухолей в моделях как гематологических, так и сóлидных злокачественных новообразований. Таким образом, важность этого открытия в том, что с его помощью потенциально можно преодолеть один из главных барьеров CAR-T-терапии — сложное, долгое и дорогое изготовление модифицированных клеток вне организма пациента. — In vivo site-specific engineering to reprogram T cells.
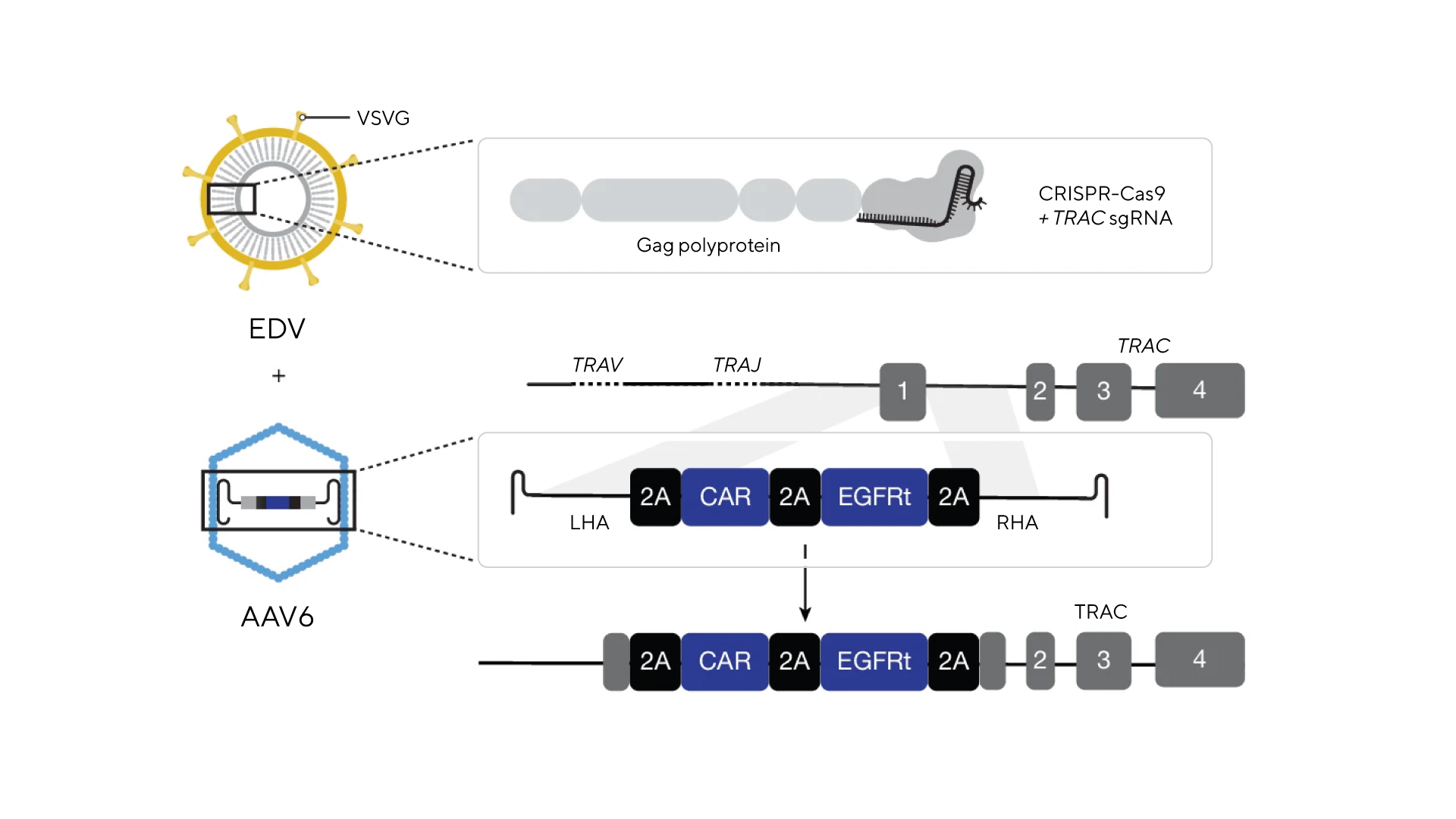
Схема эксперимента: для доставки элементов в организм использовались VSV-G WT (гликопротеины оболочки вируса везикулярного стоматита «дикого типа») и аденоассоциированные вирусы, а сама вставка происходила в локус TRAC, обеспечивающий физиологичную и контролируемую экспрессию CAR. Источник: Nature
Как метаболические рецепторы направляют NK-клетки и T-лимфоциты к сóлидным опухолям
Одна из важных ролей естественных клеток-киллеров (NK-клеток) и T-лимфоцитов — защитная: они способны распознавать сóлидные опухоли и проникать внутрь ткани для их дальнейшего уничтожения. В недавнем исследовании удалось показать, что этот процесс можно сделать более эффективным, если снабдить иммунные клетки особыми метаболит-чувствительными рецепторами. В результате NK-клетки и T-лимфоциты начинают лучше ориентироваться в опухолевом микроокружении и активнее мигрировать к очагу опухоли.
Для поиска таких рецепторов исследователи использовали CRISPR-активационные скрининги и идентифицировали несколько перспективных кандидатов, среди которых особенно выделился рецептор GPR183. После этого ученые перепрограммировали NK- и T-клетки, «заставив» их экспрессировать нужные рецепторы. В экспериментах на мышиных моделях это привело к повышению накопления иммунных клеток в опухоли и усилению противоопухолевого эффекта. В случае если подобный подход удастся подтвердить на стадии клинических исследований, такой метод лечения может повысить эффективность CAR-T- и CAR-NK-терапии для лечения труднодоступных опухолей. — Engineering NK and T cells with metabolite-sensing receptors to target solid tumors.
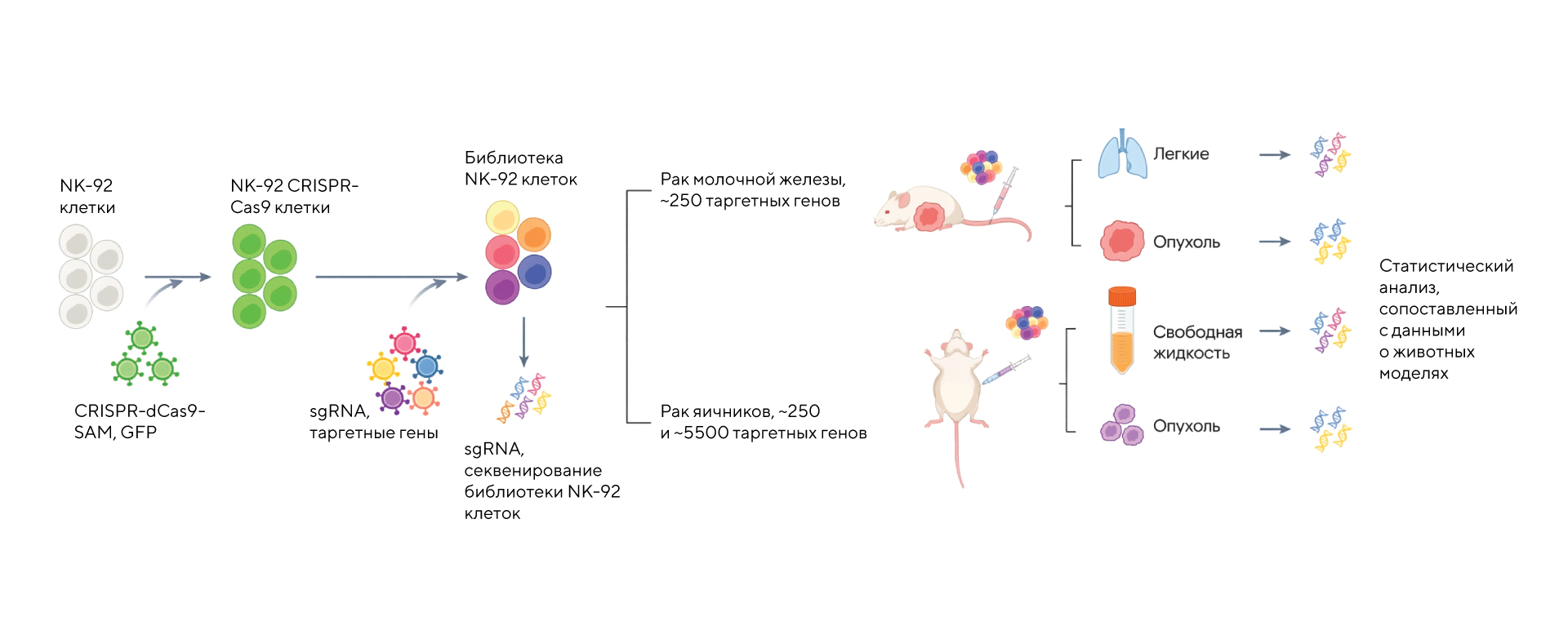
Экспериментальная схема скрининга методом CRISPR in vivo; исследователи изучали результаты на мышиных моделях, которым делали инъекции внутривенно, внутрибрюшинно и подкожно. Источник: адаптировано из Nature
Как лимфатическое метастазирование «подсвечивает» перспективную терапевтическую мишень при раке молочной железы
Обратите внимание: ниже пойдет речь об исследовании, которое опубликовано в формате неотредактированной версии статьи. Редакция журнала npj Breast Cancer размещает такие материалы до завершения окончательной проверки, чтобы читатели могли как можно раньше ознакомиться с результатами исследования. Позднее в статье могут быть выявлены ошибки, способные повлиять на ее содержание.
Рецептор эпидермального фактора роста (EGFR) считается достаточно хорошо изученным онкогенным фактором, который связан со многими видами эпителиальных злокачественных новообразований. Однако роль EGFR при раке молочной железы пока что остается неясной. В недавнем исследовании удалось продемонстрировать, что фактор EGFR способствует селективному лимфатическому распространению при трижды негативном раке молочной железы. Ключевыми участниками этого процесса являются непосредственно рецептор EGFR и его лиганд TGF-α, которые опосредуют направленную миграцию опухолевых клеток в лимфатические сосуды.
Связывание TGF-α с рецептором EGFR запускает сигнальный путь STAT3 и усиливает хемотаксис — направленное движение клеток к лимфатическим сосудам. При этом соседний фактор CTGF, наоборот, подавляет этот эффект. В эксперименте блокада TGF-α антителом фепикснебарт (Fepixnebart) заметно тормозила раннее лимфогенное метастазирование EGFR-положительных опухолевых клеток и сопровождалась изменением иммунного состава лимфоузлов, включая снижение доли CD8+ T-клеток. Важность этого открытия в том, что оно предлагает перенастроить уже известную ось EGFR-таргетной терапии: не только подавлять рост опухоли, но и мешать раннему метастазированию. Полученные результаты делают TGF-α/EGFR перспективной мишенью для биологических препаратов, особенно в контексте лечения агрессивных форм рака груди, где раннее поражение лимфоузлов сильно ухудшает прогноз для пациентов. — TGF-α/EGFR-mediated lymphatic metastasis reveals a repositionable therapeutic target in breast cancer.
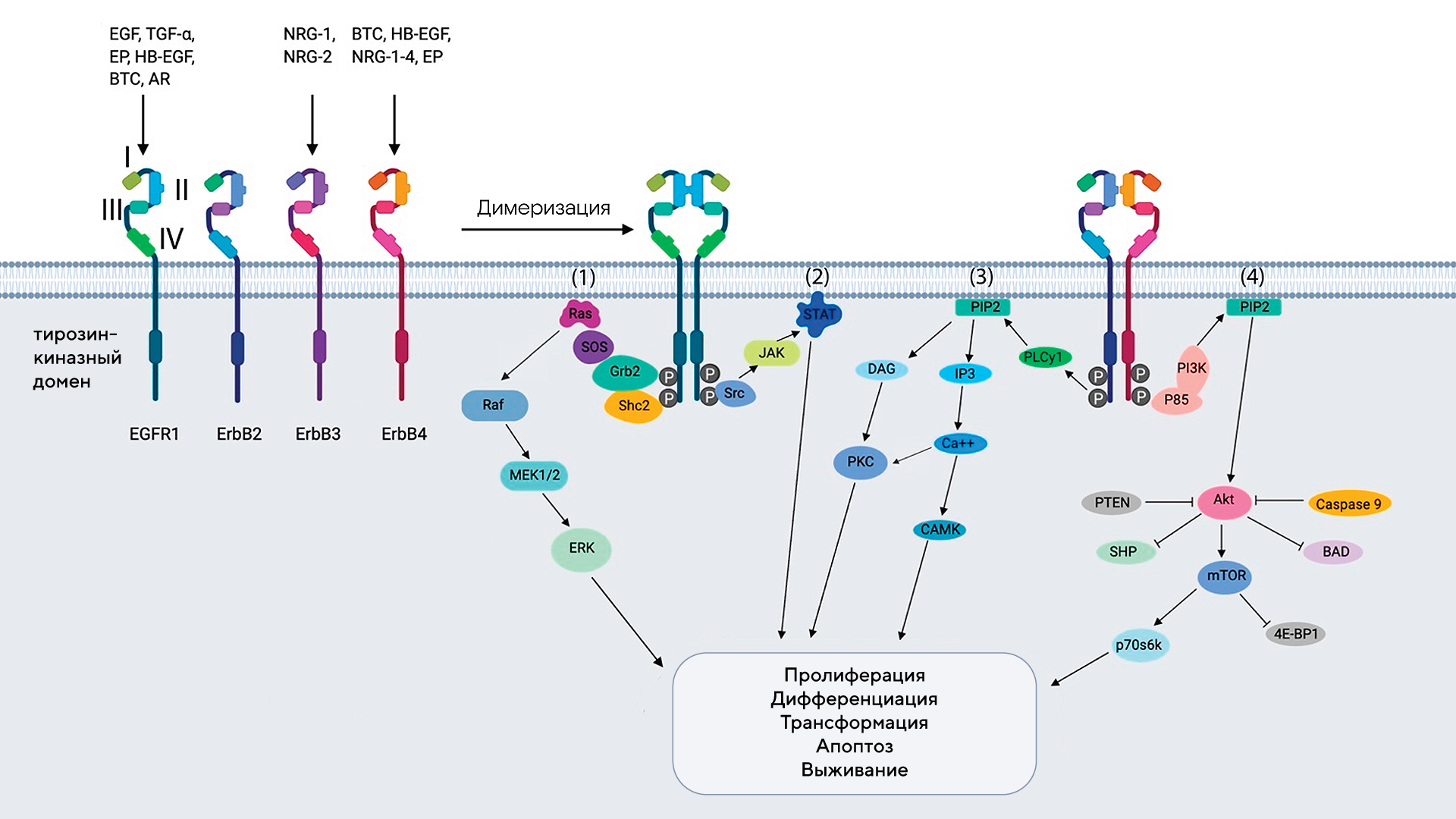
Схематическое представление четырех различных рецепторов (EGFR1, ErbB2, ErbB3, ErbB4), ассоциированных с раком молочной железы. Источник: MDPI
Миниатюрный генетический «ключ» против рака: как TnpB-ωRNA усиливает иммунотерапию
Системы CRISPR-Cas — активно изучаемые инструменты для редактирования генома. Однако у них есть ограничение, которое мешает их широкому применению в клинике, а именно большой размер белков Cas, из-за чего осложняется их эффективная доставка. Чтобы преодолеть это препятствие, исследователи из Китая разработали компактные CRISPR-подобные инструменты на основе системы TnpB-ωRNA. С их помощью можно управлять активностью генов и оснований, причем благодаря своему размеру такие конструкции доставляются в клетки проще, чем крупные Cas-белки. На практике это может быть особенно важно для иммунотерапии рака: так, с помощью AAV-системы ImmunAct исследователи активировали гены, отвечающие за синтез CXCL9, IL-15 и IFN-γ. В результате на мышиных моделях удалось продемонстрировать миграцию и активацию Т-лимфоцитов, которые способны уничтожать опухолевые клетки, особенно совместно с анти-PD-1-терапией. Таким образом, это исследование открывает перспективы для более гибкой доставки иммуномодулирующих конструкций и создания новых схем противоопухолевой терапии, которые можно комбинировать с уже существующими иммунопрепаратами. — Miniature and versatile genome regulation TnpB-ωRNA toolkits facilitate cancer immunotherapy.
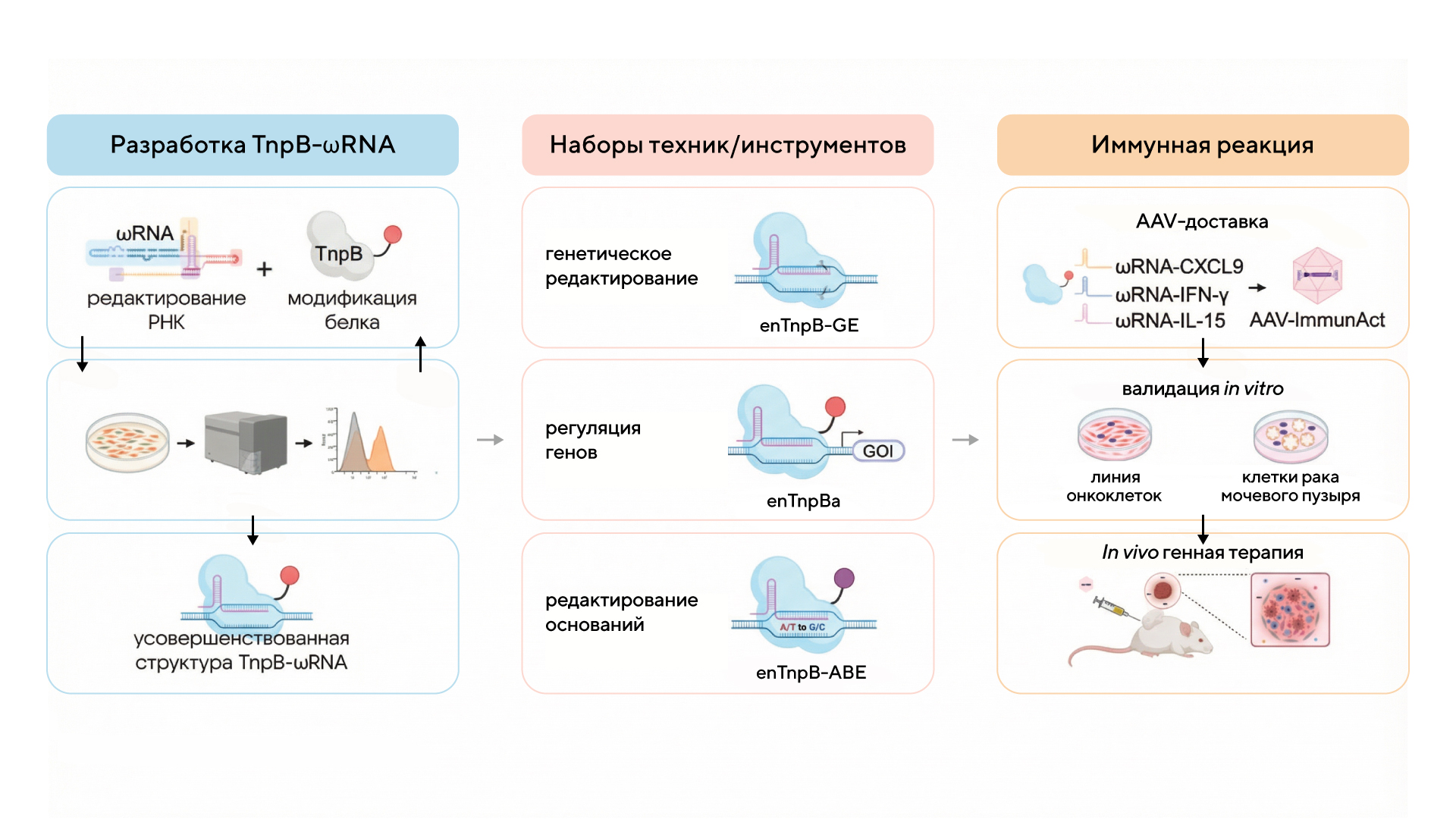
Схема получения конструкции TnpB-ωRNA. Источник: Nature Communications
Наночастицы против рака яичников: как siRNA учат опухоль «молчать»
Рак яичников — один из самых сложных для лечения видов опухолей, что во многом связано с устойчивостью этого вида заболевания к терапии, а также с высокой частотой рецидивов. Одним из перспективных направлений лечения этого вида злокачественных новообразований может стать генная терапия, в том числе технология интерференции малых интерферирующих РНК (siRNA). В недавнем обзоре подробно описан терапевтический подход с использованием наночастиц как своеобразных «курьеров» для доставки siRNA, которые способны избирательно выключать активность генов, связанных с ростом опухоли и ее выживанием. Этот подход помогает решить основную проблему siRNA-терапии: без защиты такие молекулы быстро разрушаются в организме и просто не успевают попасть в нужное место. Наночастицы способны повысить стабильность siRNA, улучшить доставку в опухоль и снизить системные побочные эффекты, а значит, сделать генное «молчание» более точным и эффективным. — The application of nanoparticle-mediated siRNA delivery systems in ovarian cancer.
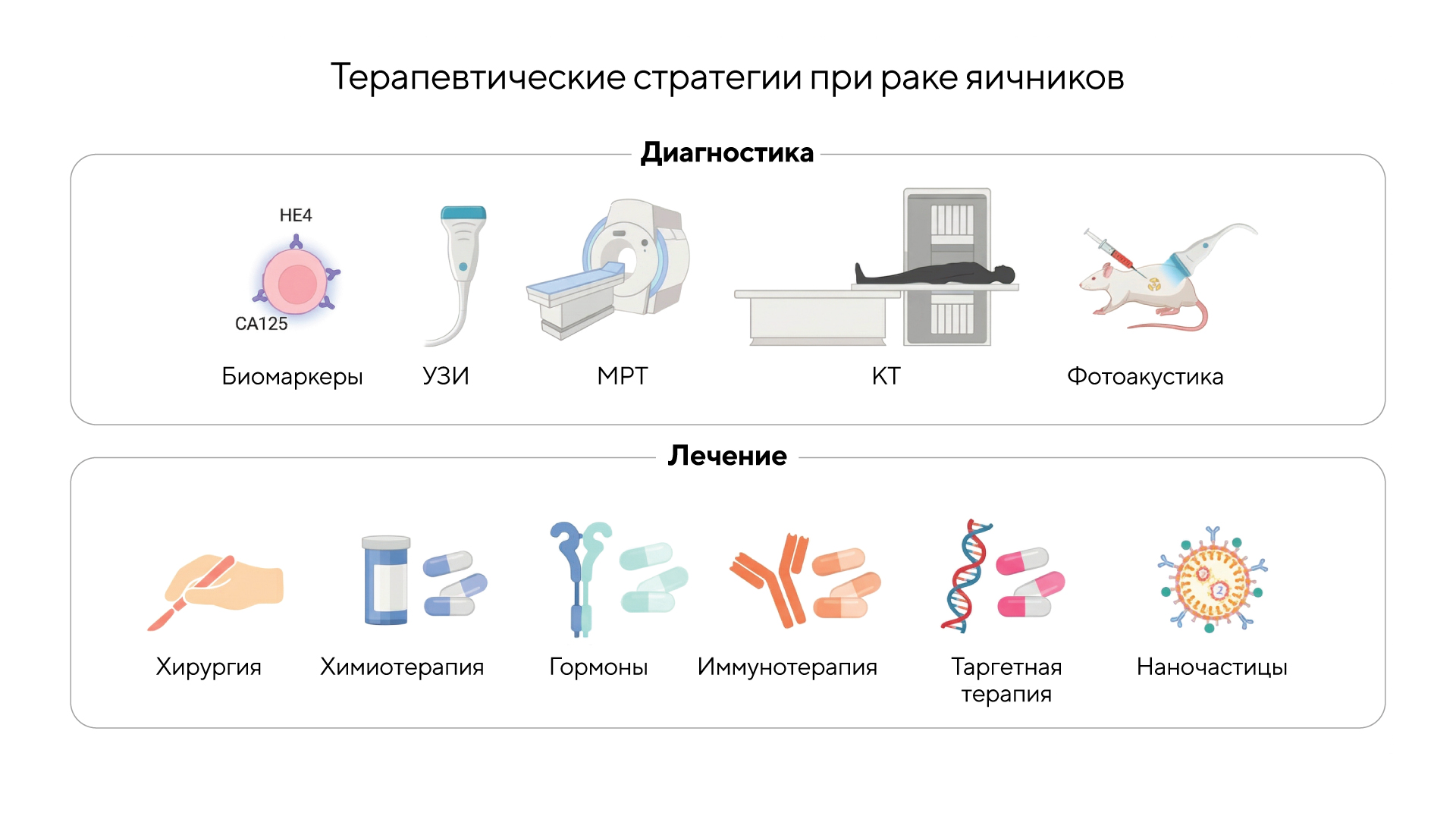
Существующие стратегии диагностики и лечения рака яичников. Источник: Cancer Gene Therapy