
Дайджест #7. Какой вирус виновен в развитии рассеянного склероза
Новость о том, что вирус Эпштейна — Барр повышает шансы на развитие рассеянного склероза, недавно получила новые подтверждения. Заражение людей этим вирусом можно назвать бомбой замедленного действия: после инфицирования вирус может годами дремать внутри В-лимфоцитов, пока не выстрелит — и запустит патологические процессы поражения миелиновых оболочек нейронов. О том, как это происходит, а также о других новостях из мира онкологических и аутоиммунных заболеваний читайте в новом дайджесте.
Онкология
Как везикулы влияют на опухоли и что с этим делать
В онкологии выделяют горячие и холодные опухоли: первые лучше поддаются лечению благодаря своей «видимости» для иммунных клеток, а вторые замаскированы от иммунного ответа и обычно связаны с негативным прогнозом. Механизмы «неуязвимости» холодных опухолей все еще изучены недостаточно, и любое новое исследование в этой области может дать ключ к пониманию их лечения. Недавно биологам удалось выявить одного из возможных виновников, которые связаны с подавлением иммунного ответа через PD-1. Вспомним о роли белка PD-1: он связывается с лигандом PD-L1 опухолей и подавляет иммунные Т-клетки. Выяснилось, что в этом участвуют малые внеклеточные везикулы — они переносят PD-1 и другой мембранный белок, CD80, которые производят стимулированные Т-клетки. Из-за этого происходит адаптивное перераспределение PD-1 и CD80 на поверхности опухолевых клеток. В результате развивается системная иммуносупрессия, подавляются молекулы, связанные с презентацией антигена, а сами опухоли приобретают холодный фенотип. Результаты исследования подсвечивают один из возможных способов лечения таких опухолей — удар по везикулам с целью ингибирования иммунных «тормозов». — PD-1/CD80+ small extracellular vesicles from immunocytes induce cold tumours featured with enhanced adaptive immunosuppression.
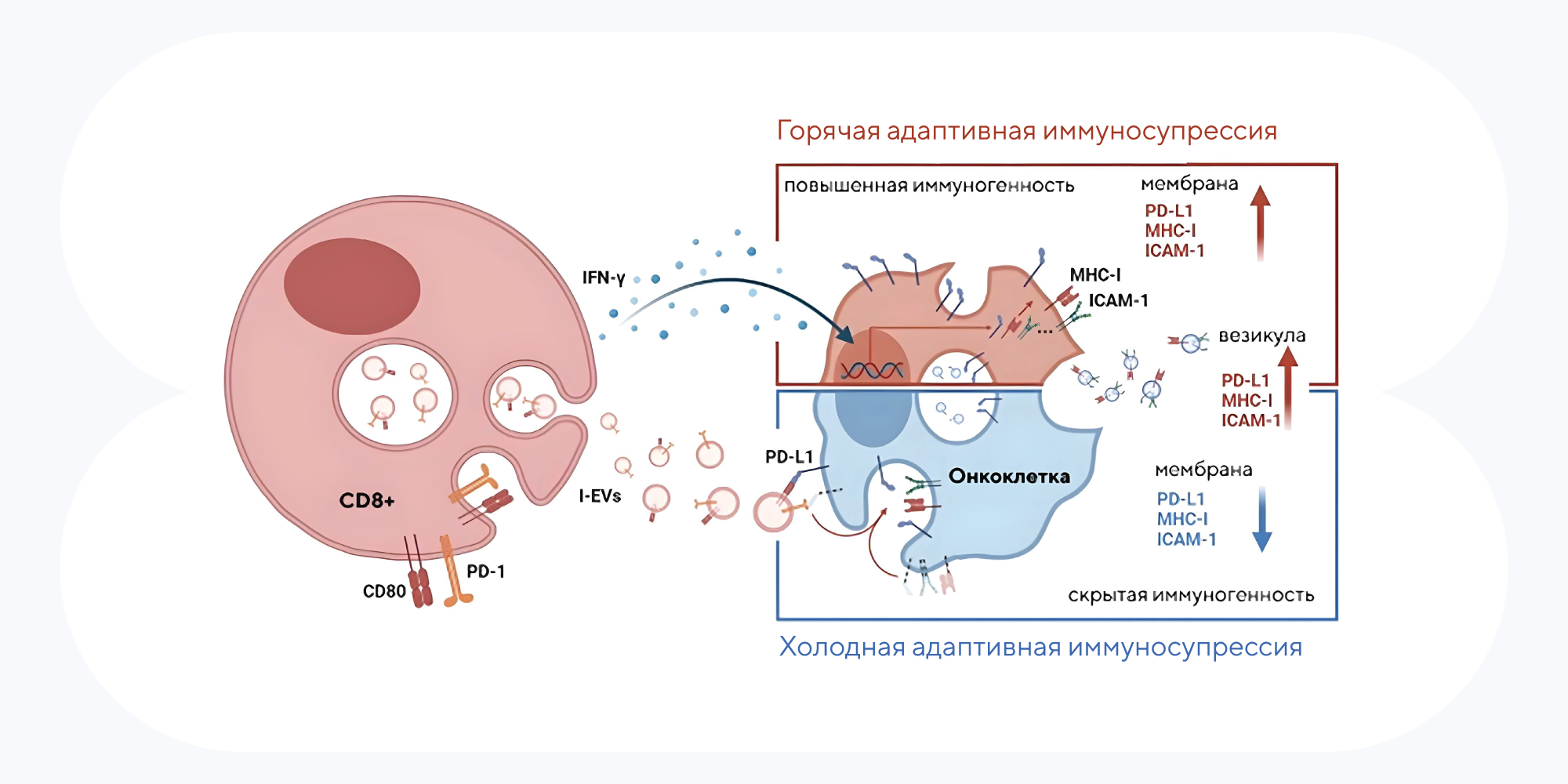
Источник: адаптировано из Nature Cancer
Более ранние исследования показали, что секреция PD-L1 и малых внеклеточных везикул может быть связана с IFN-γ. В новой работе решили сравнить эффекты IFN-γ и PD-1/CF-80, которые производятся стимулированными CD8+ Т-клетками. Выяснилось, что в случае IFN-γ наблюдается повышенная регуляция белков, из-за чего на мембране увеличивается количество PD-L1, а в случае переноса PD-1 в составе везикул, наоборот, снижается. Это приводит к формированию холодного типа опухоли.
Совместное действие химио- и иммунотерапии улучшает терапию рака
Комбинация химио- и иммунотерапии считается одним из действенных способов улучшить ответ на лечение у пациентов с онкологией, однако обширных количественных данных этого эффекта пока что накоплено недостаточно. Недавнее исследование устраняет этот пробел: в нем суммированы известные на сегодняшний день данные о транскриптомике опухолей, на которые воздействовали анти-PD-1, а также о линиях раковых клеток, которых подвергали действию химиопрепаратов. Целью этой работы было изучить возможность изменения устойчивости опухолей к анти-PD-1 под воздействием и химических веществ, и низкомолекулярных ингибиторов. В результате удалось подтвердить митохондриальный РНК-зависимый механизм иммунной активации в опухоли. — Systematic investigation of chemo-immunotherapy synergism to shift anti-PD-1 resistance in cancer.
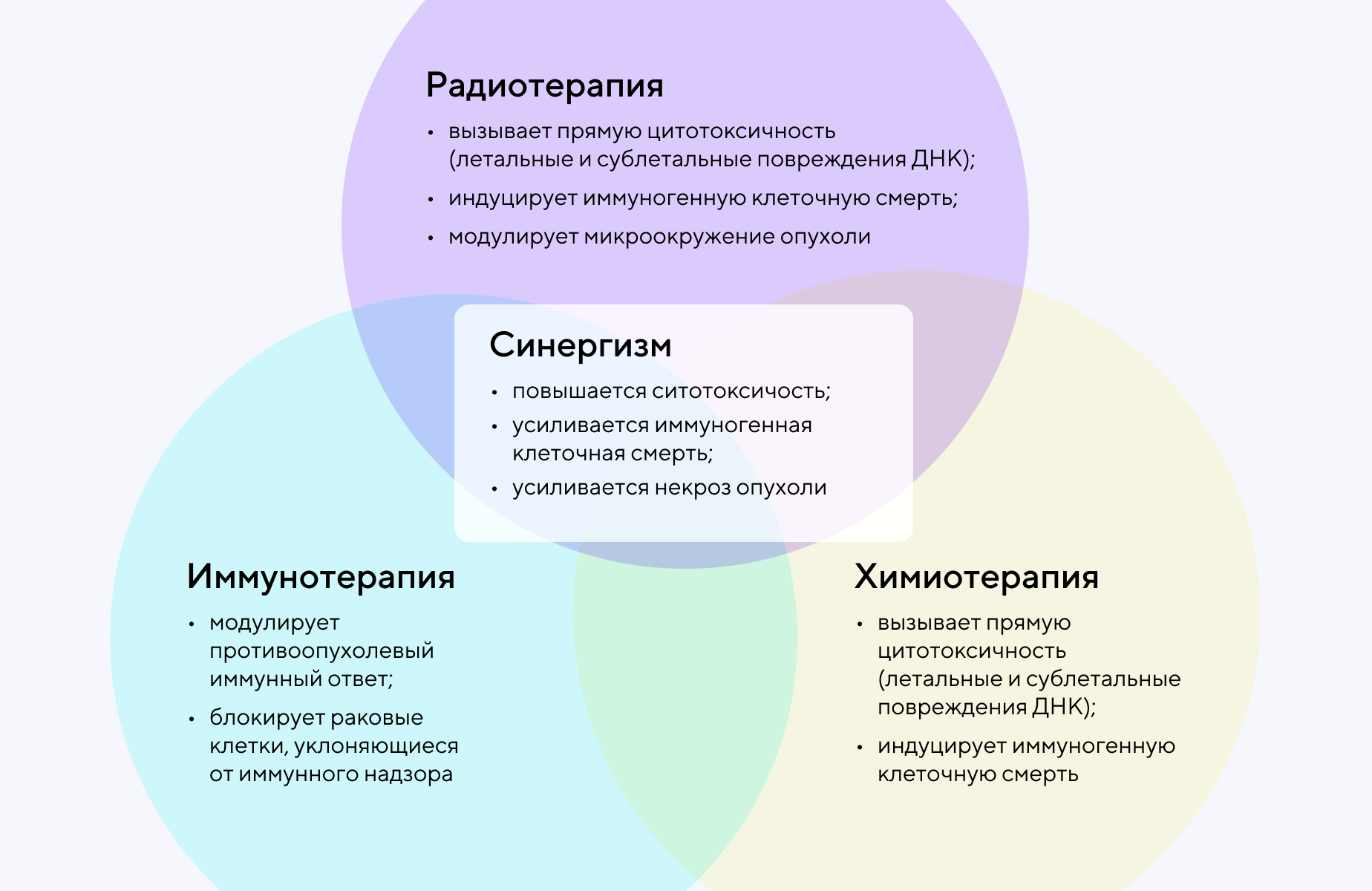
Потенциальные синергические эффекты, которые возникают при комбинации химио-, иммуно- и лучевой терапии. Адаптировано из ResearchGate
Обнаружена потенциальная уязвимость в резистентных меланомах
Один из ключевых регуляторов развития меланомы — сигнальный путь МАРК: большинство мутаций в генах белков этого пути связаны с развитием опухолей. Эта особенность делает МАРК-путь важной терапевтической мишенью для борьбы со злокачественными образованиями кожи. Продвинуться в понимании особенностей сигнального пути МАРК стало возможным благодаря совместной работе бельгийских и американских биологов. Им удалось обнаружить важного игрока МАРК-пути, ответственного за устойчивость меланомы к лечению — им оказалась валин-аминоацил-тРНК-синтетаза, VARS (valine aminoacyl-tRNA synthetase). Так, перестройка белкового профиля в резистентных меланомах смещена в сторону использования валина, а значит, связана с усилением экспрессии VARS. Данные, полученные в результате экспериментов in vitro и in vivo, показывают, что VARS может стать привлекательной мишенью для терапии резистентных меланом. — Valine aminoacyl-tRNA synthetase promotes therapy resistance in melanoma.
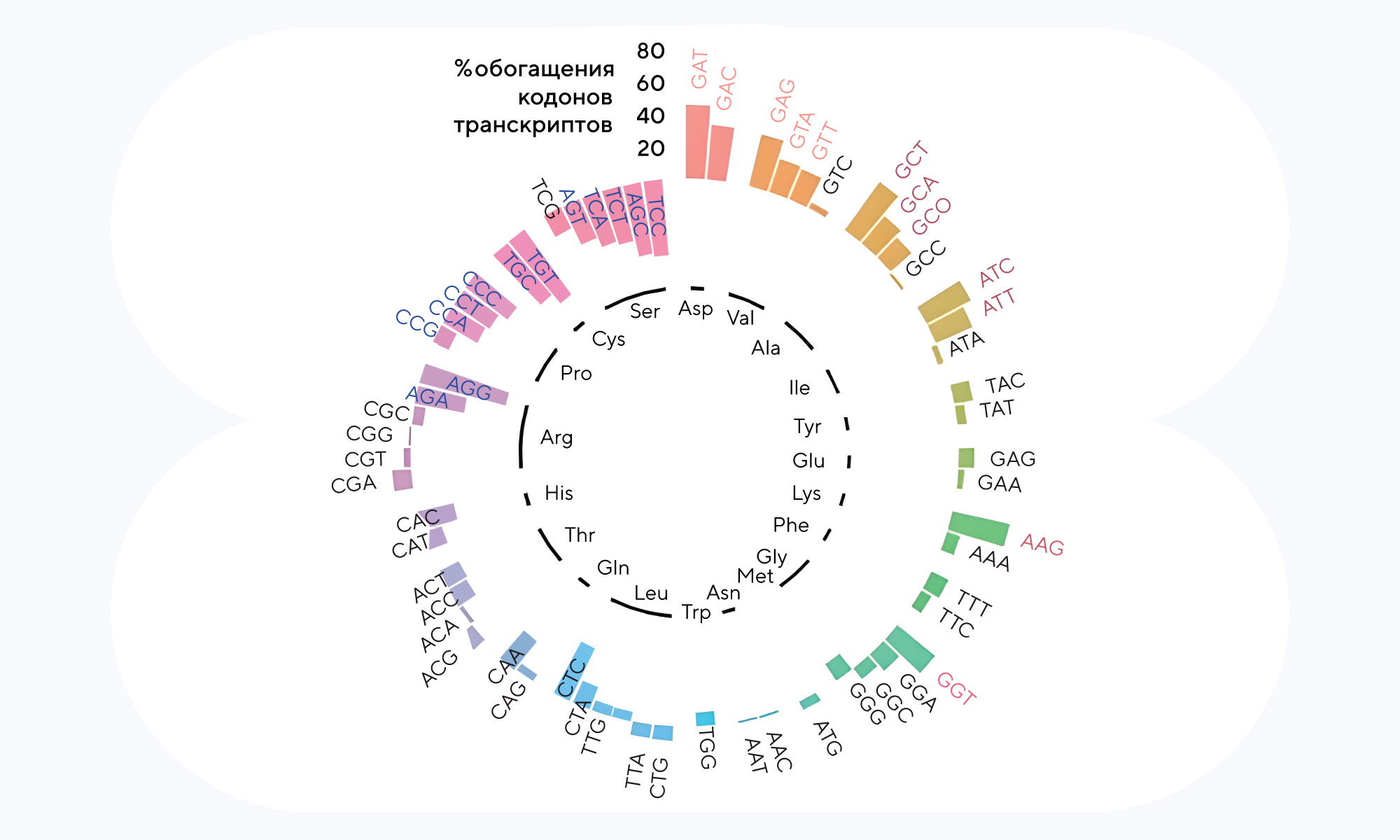
Активность белков МАРК-пути, обогащенных валином, повышается в случае резистентных к лечению меланом. На графике представлены процентные содержания кодонов в транскриптах таких меланом. Источник: Nature Cell Biology
Как изменить микроокружение опухоли для улучшения лечения рака
Глиобластома — одна из наиболее агрессивных форм опухоли мозга, лечение которой осложняется непроницаемостью гематоэнцефалического барьера (ГЭБ) для большинства лекарственных препаратов. Наблюдения за пациентами с глиобластомами дикого типа показали низкую пятилетнюю выживаемость. Эффективность существующего лечения ограничивается инфильтрацией иммунных клеток — микроглией и ассоциированными с опухолью макрофагами, в результате чего глиобластома разрастается и становится более устойчивой к терапии. Чтобы снять это ограничение, в новом исследовании решили нацелить на опухоль комплекс РНК-РНК-связывающего белка LOC-DHX15. Считается, что этот комплекс играет ключевую роль в стимулировании инфильтрации иммунных клеток и росте опухоли, приводя к развитию более агрессивных видов рака мозга. В серии экспериментов на комплекс LOC-DHX15 нацелили малые молекулы, проницаемые через ГЭБ. В результате удалось повысить уязвимость глиобластомы для терапии благодаря нарушению связей между клетками и снижению выживаемости онкоклеток. Этот терапевтический подход обещает большие перспективы не только в лечении опухолей мозга, но и других видов рака. — Tumour microenvironment programming by an RNA-RNA-binding protein complex creates a druggable vulnerability in IDH-wild-type glioblastoma.
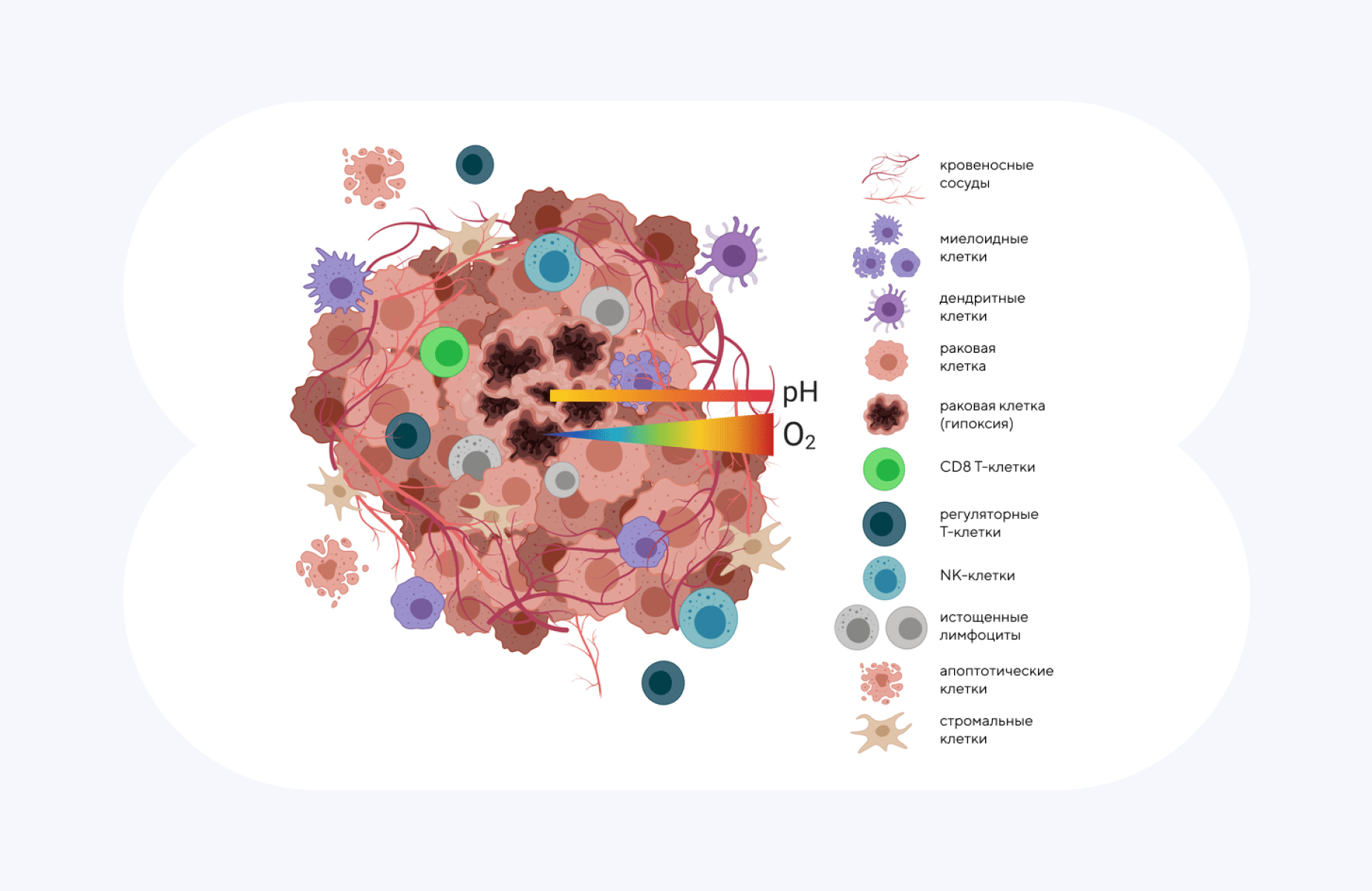
Микроокружение опухоли — целая система из различных клеток, кровеносных сосудов и продуктов метаболизма. Источник: Wikipedia
Аутоиммунные заболевания
Как вирус Эпштейна — Барр связан с рассеянным склерозом
Один из триггеров, который повышает риск развития рассеянного склероза, — вирус Эпштейна — Барр. Коварность этого вируса в том, что после проникновения в организм он способен годами оставаться в В-лимфоцитах, но в какой-то момент активируется и запускает хроническое воспаление. До недавнего времени роль В-клеток, инфицированных вирусом Эпштейна — Барр, в развитии рассеянного склероза оставалась непонятной. Приблизиться к пониманию механизмов патогенеза болезни удалось исследователям из США. Для этого они сравнили лимфобластоидные клеточные линии, выделенные у пациентов с рассеянным склерозом и у здоровых людей. Выяснилось, что В-клетки пациентов с рассеянным склерозом в активной фазе заболевания сильнее экспрессируют литический ген вируса Эпштейна — Барр. Если снизить репликацию вируса в В-клетках с помощью таргетных подходов, можно снизить выработку цитокинов и аутологичные ответы CD4+ Т-клеток — а значит, ослабить аутоиммунное воспаление при рассеянном склерозе. — Multiple sclerosis patient-derived spontaneous B cells have distinct EBV and host gene expression profiles in active disease.
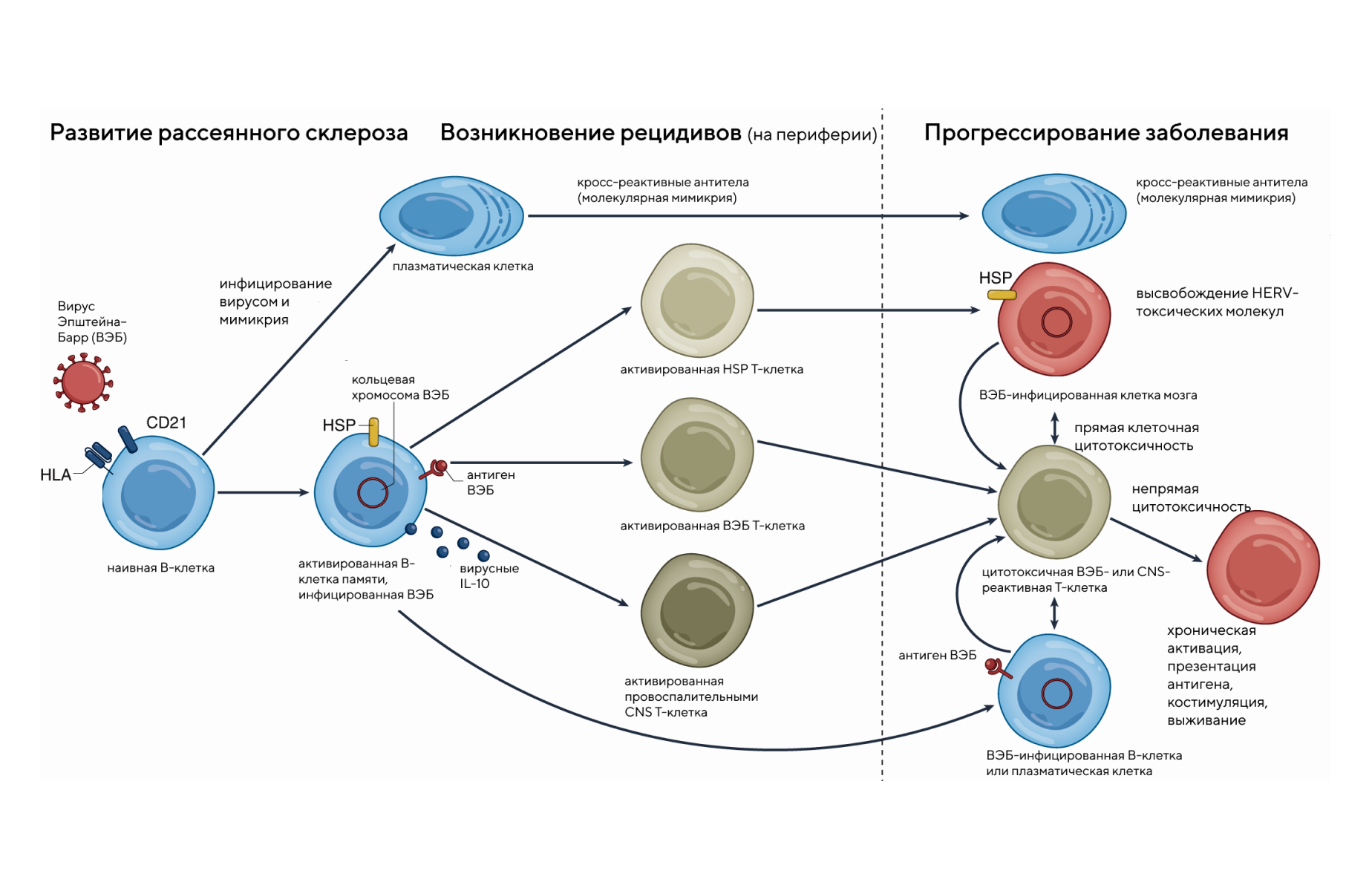
Роль вируса Эпштейна — Барр в развитии рассеянного склероза. Источник: Nature Medicine
Связи между популяциями иммунных клеток определяют течение ревматоидного артрита
В развитии ревматоидного артрита участвуют различные антиген-специфические Т- и В-клетки. Чтобы разобраться в обилии ассоциаций между ними при болезни, исследователи выделили из синовиальной оболочки суставов пациентов различные популяции Т- и В-лимфоцитов. Так, CD4+ Т-клетки, в числе которых CCL5+ и периферические Т-хелперы, продемонстрировали выраженную транскриптомную подпись (то есть изменения в активности), связанную с их эффекторной функцией. В отличие от CD4+, CD8+ Т-клетки показали более высокую олигоклональность, а их самые многочисленные клоны были обогащены клетками GZMK+. Среди В-клеток наибольшую клональную экспансию продемонстрировали NR4A1+ и плазматические клетки. Также ученым удалось идентифицировать плазматические клетки, которые несли на себе В-клеточные рецепторы, общие для ABC-клеток, клеток памяти и активированных В-клеток. Все эти результаты демонстрируют разнообразие и различные типы взаимоотношений между субпопуляциями синовиальных клеток у пациентов с ревматоидным артритом. — Clonal associations between lymphocyte subsets and functional states in rheumatoid arthritis synovium.
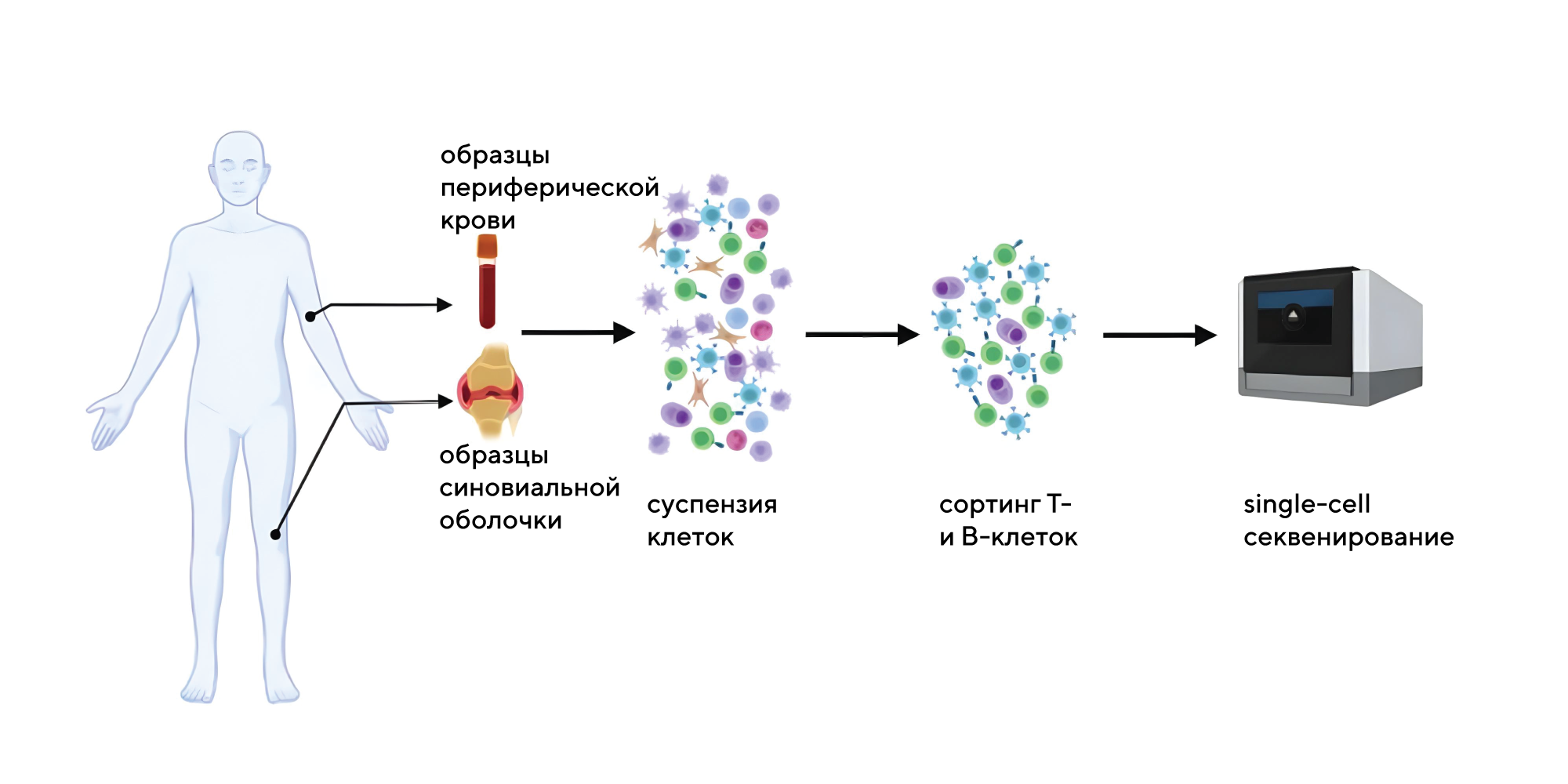
Схема дизайна исследования: Т- и В-клетки выделяли методом биопсии из синовиальной оболочки и периферической крови; секвенирование клеток проводили с использованием платформы 10X Genomics. Источник: Nature Communications