
МикроРНК для макрозадач: за что вручили Нобелевскую премию — 2024
Когда-то считалось, что экспрессию генов регулируют преимущественно белки. Но в 1993 году впервые была опубликована статья, которая изменила представление о регуляции генов и вывела на биологическую арену маленького, но важного участника — микроРНК. С тех пор выяснилась роль этих маленьких молекул в развитии множества болезней — от вирусных инфекций до аутоиммунных заболеваний. А еще микроРНК нашли свое применение в медицине, в особенности — в терапии рака. Попробуем разобраться, почему эти молекулы так важны в нормальном развитии организма и как исследователи используют их для своих задач.
Маленькие молекулы с историей в миллионы лет
МикроРНК получили свое название из-за размеров: их длина обычно составляет 18–25 нуклеотидов — в отличие от сотен и тысяч нуклеотидов в обычной мРНК. Более того, эти микроРНК еще и некодирующие, то есть на их матрице нельзя собрать полноценный белок. Долгое время считалось, что они не выполняют каких-либо важных функций в организме, а лишь достались нам в наследство от более примитивных организмов. На заре эволюции много миллионов лет назад эти молекулы появились у губок и кишечнополостных, в организме которых начали выполнять защитную роль.
Привлечь к себе интерес этим молекулам удалось с помощью червя Caenorhabditis elegans. Этот классический модельный организм активно используют в своих исследованиях многие ученые. Один из будущих нобелевских лауреатов, Виктор Эмброс, пытался разобраться с вопросом: почему у некоторых нематод С. elegans не развиваются органы. Выяснилось, что причина — в мутации в гене lin-4, который нарушает нормальное течение сразу нескольких программ развития. Примерно в это же время другой биолог — и второй будущий лауреат 2024 года, Гэри Равкун, — тоже изучал нематод, но уже с другой проблемой: тех, которые почему-то перескакивали через этап личинки и не вырастали до взрослых размеров. Причина тоже была в мутации, но уже в другом гене — lin-14. И здесь завязывается история будущего открытия: выяснилось, что элементы lin-4 были комплементарны фрагментам lin-14. Более того, эти комплементарные участки были некодирующими и, как казалось, никак не могли влиять на организм — но тем не менее нарушали нормальную программу развития нематоды. Дальнейшие исследования подтвердили эту странность: действительно, участок гена lin-4 (который совпадает с частью гена lin-14) не кодирует белок, однако на его матрице синтезируется РНК, хотя и очень маленькая. Эту РНК длиной всего в 21 нуклеотид назвали микроРНК, написали об открытии в журнале Cell — и на какое-то время забыли об этом странном некодирующем феномене.
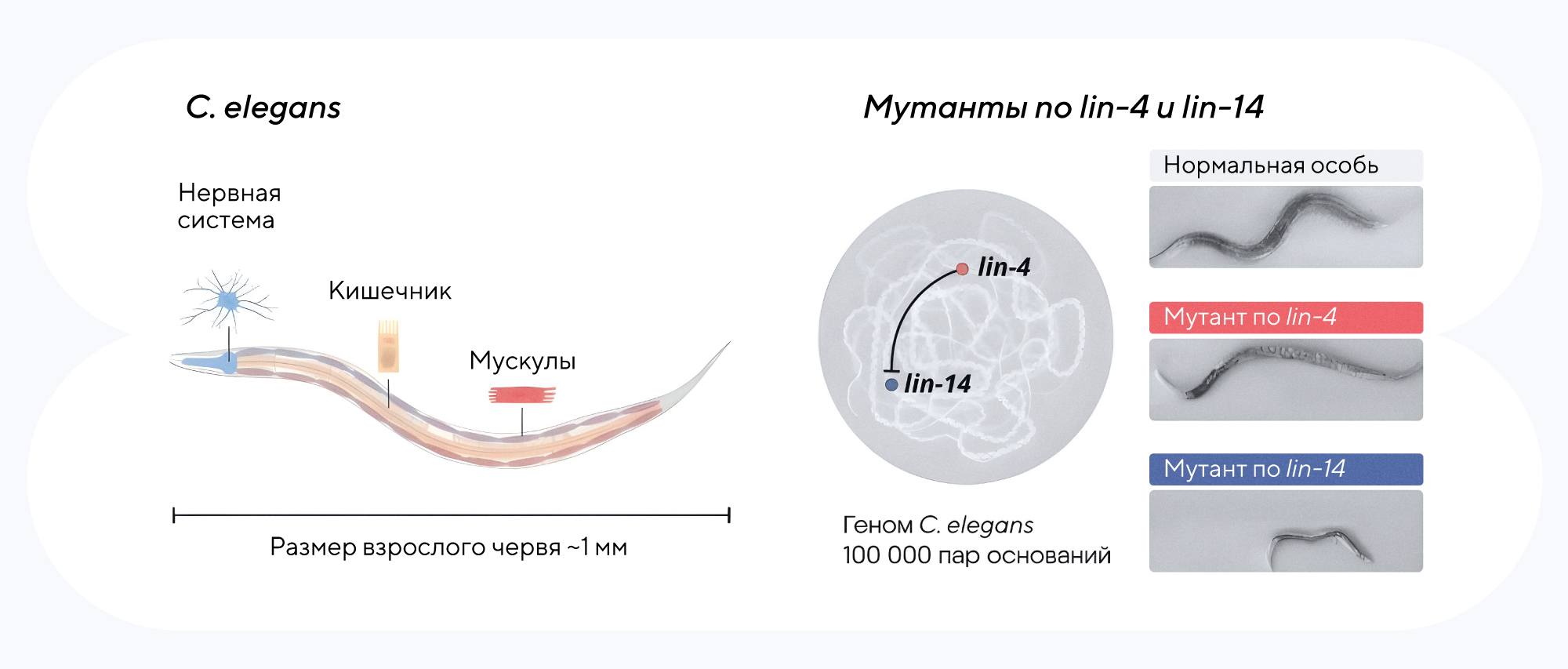
Нематода C. elegans — популярный модельный организм для изучения того, как развиваются разные типы клеток. Именно с этим организмом работали будущие нобелевские лауреаты: Виктор Эмброс обнаружил связь между дефектами развития и мутацией в гене lin-4, а Гэри Равкун выявил нарушения скорости развития у нематоды, мутантной по гену lin-14. Расшифровка генома червя показала, что за эти нарушения отвечают аномально короткие некодирующие РНК — микроРНК
Зачем нужны микроРНК
После первой публикации про микроРНК нематод казалось, что эти экзотические некодирующие последовательности есть только у примитивных животных, поэтому их дальнейшее исследование не будет иметь практической значимости. Однако спустя время выяснилось, что микроРНК играет очень важную роль в организме человека — эти небольшие некодирующие молекулы контролируют экспрессию более 60% генов. Обычно микроРНК выступают в роли переключателей генома: активируя или выключая те или иные гены, микроРНК координируют дифференцировку клеток. В результате в каждой клетке реализуется своя программа развития, которая наделяет клетку своими особенностями и делает ее непохожей на других.
Как работают микроРНК
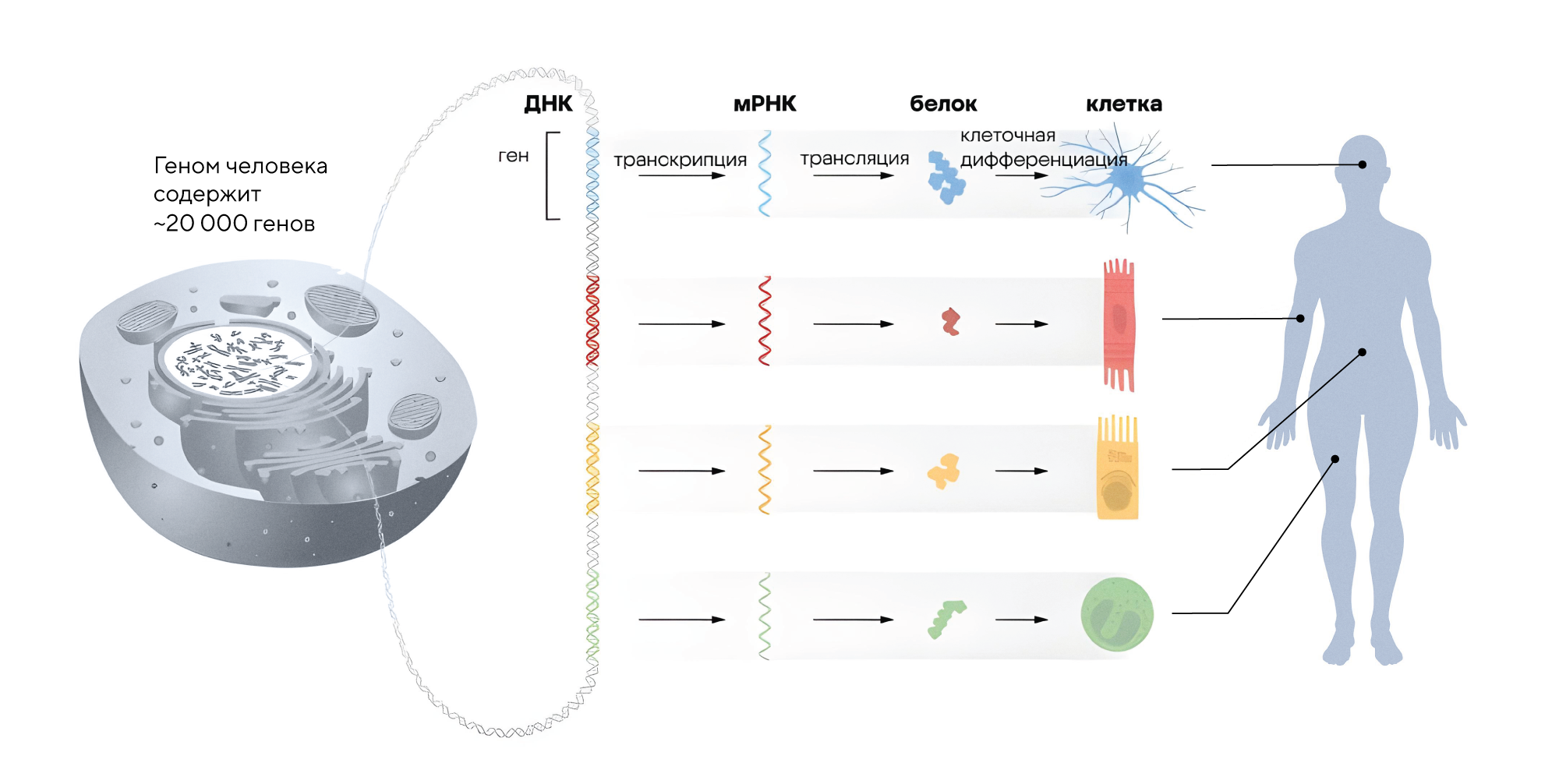
Источник: пресс-релиз Нобелевского комитета
Все клетки нашего организма несут один и тот же набор генов с одинаковой генетической информацией, закодированной в ДНК. Однако разные клетки реализуют эту информацию по-разному: нервные клетки передают сигналы, мышечные — сокращаются и удлиняются, а эпителиальные выполняют барьерную функцию. Это возможно за счет точной регуляции активности генов: в каждом конкретном типе клеток активен только определенный набор генов. При этом активность генов постоянно перенастраивается, чтобы приспосабливаться к изменяющимся условиям среды. Но если регуляция генов идет не так, это может приводить к серьезным нарушениям и заболеваниям. Почему это происходит?
В организме человека содержится почти 20 тысяч генов, информация с которых переводится в молекулы РНК — этот процесс называется транскрипцией. А уже на основе матрицы РНК строятся белки — это процесс трансляции. Чтобы понимать, какие конкретно участки ДНК нужно скопировать на РНК и на ее основе создать белок, нужны микроРНК. Разные микроРНК связываются с ДНК, отключая или, наоборот, активируя конкретные гены, а значит, запускают те или иные клеточные процессы. Если микроРНК воздействует на ген не так, как нужно, это приводит к сбою запрограммированной генетической программы.
Роль микроРНК в развитии и лечении рака
Конечно, микроРНК не определяет все многообразие типов клеток. Однако исследования подтверждают: клетки и ткани не могут нормально развиваться без этих некодирующих молекул. Так, аномальная регуляция микроРНК может запускать онкогенные процессы. Например, мутации в одном из белков, который необходим для сборки микроРНК, приводит к DICER1-синдрому — эта генетическая мутация повышает риск развития рака. А поломки в двух микроРНК, которые в норме блокируют рост онкоклеток, приводят к развитию хронического лимфоцитарного лейкоза.
При раке микроРНК выполняют двойственную роль: с одной стороны, в организме вследствие мутаций могут возникать онкогенные микроРНК, которые запускают процесс образования опухолей, с другой стороны — некоторые онкосупрессорные микроРНК подавляют развитие онкоклеток. Функции конкретной микроРНК как «плохого» или «хорошего» игрока определяются уровнем ее экспрессии в разных тканях: в одном месте организма микроРНК подавляет опухолевые процессы, а в другом эта же микроРНК запускает онкогенный процесс. Задача исследователей — научиться определять, при каких условиях те или иные микроРНК блокируют или провоцируют рак.
Получается, что восстановление нормальных функций микроРНК или их доставка в составе вектора в нужное место — перспективный способ терапии рака и других болезней, связанных с регуляцией микроРНК. Однако этот способ лечения пока еще сыроват: на сегодняшний день нет ни одного примера успешно завершенных клинических исследований препаратов на основе микроРНК. Во многом это связано со сложностью работы и недостаточной изученностью этих молекул: микроРНК очень быстро разрушаются, их тяжело направлять в нужные места в организме, а еще они могут вызывать опасные иммунные реакции. Однако эти сложности преодолимы: чем больше мы узнаем об этих небольших молекулах, тем скорее получится создавать на их основе безопасные и эффективные лекарства. Именно поэтому во многих исследовательских лабораториях, в том числе и в BIOCAD, продолжают исследовать микроРНК для их дальнейшего выхода на биотехнологическую арену.