
Дайджест #6. Рассеянный склероз: большая роль малой молекулы. И маленькой мыши
Как справляются с рассеянным склерозом, при котором разрушаются оболочки собственных нейронов? Обычно используют препараты, которые снимают воспаление и препятствуют дальнейшей деградации. Но что, если не просто остановить этот процесс, но и запустить его вспять? В недавнем исследовании удалось показать, как с помощью одной молекулы, PIPE-791, удалось не просто снизить нейровоспаление, но и восстановить процесс миелинизации нейронов — правда, пока этот эффект продемонстрирован только на мышах. О том, как это происходит в мозге, читайте в новом дайджесте.
Онкология
Перспективные союзники для иммунотерапии рака
Опухоль-специфические Т-клетки — важные участники противоопухолевого иммунитета, так как часто служат своеобразными мишенями при иммунотерапии рака. Однако в микроокружении опухолей этих клеток может быть недостаточно, из-за чего эффективность иммунотерапии у пациентов снижается. Недавно выяснилось, что исправить эту ситуацию могут так называемые «клетки-свидетели» (TBYS, tumor-irrelevant bystander T cells), не имеющие непосредственного отношения к опухоли и не несущие специфичных маркеров для их распознавания при иммунотерапии. В отличие от опухоль-специфических клеток, TBYS достаточно многочисленны в микроокружении опухоли и сохраняют свойства функциональной памяти. Чтобы нацелиться на TBYS и сделать их заметными для дальнейшего уничтожения самой опухоли, использовали онколитический вирус, кодирующий эпитопы TBYS (OV-BYTE). В результате удалось перенаправить антигенную специфичность опухолевых клеток на многочисленные, но ранее незаметные клетки TBYS, благодаря чему получилось эффективно ингибировать опухоли у животных моделей при проведении доклинических исследований. — An oncolytic virus delivering tumor-irrelevant bystander T cell epitopes induces anti-tumor immunity and potentiates cancer immunotherapy.
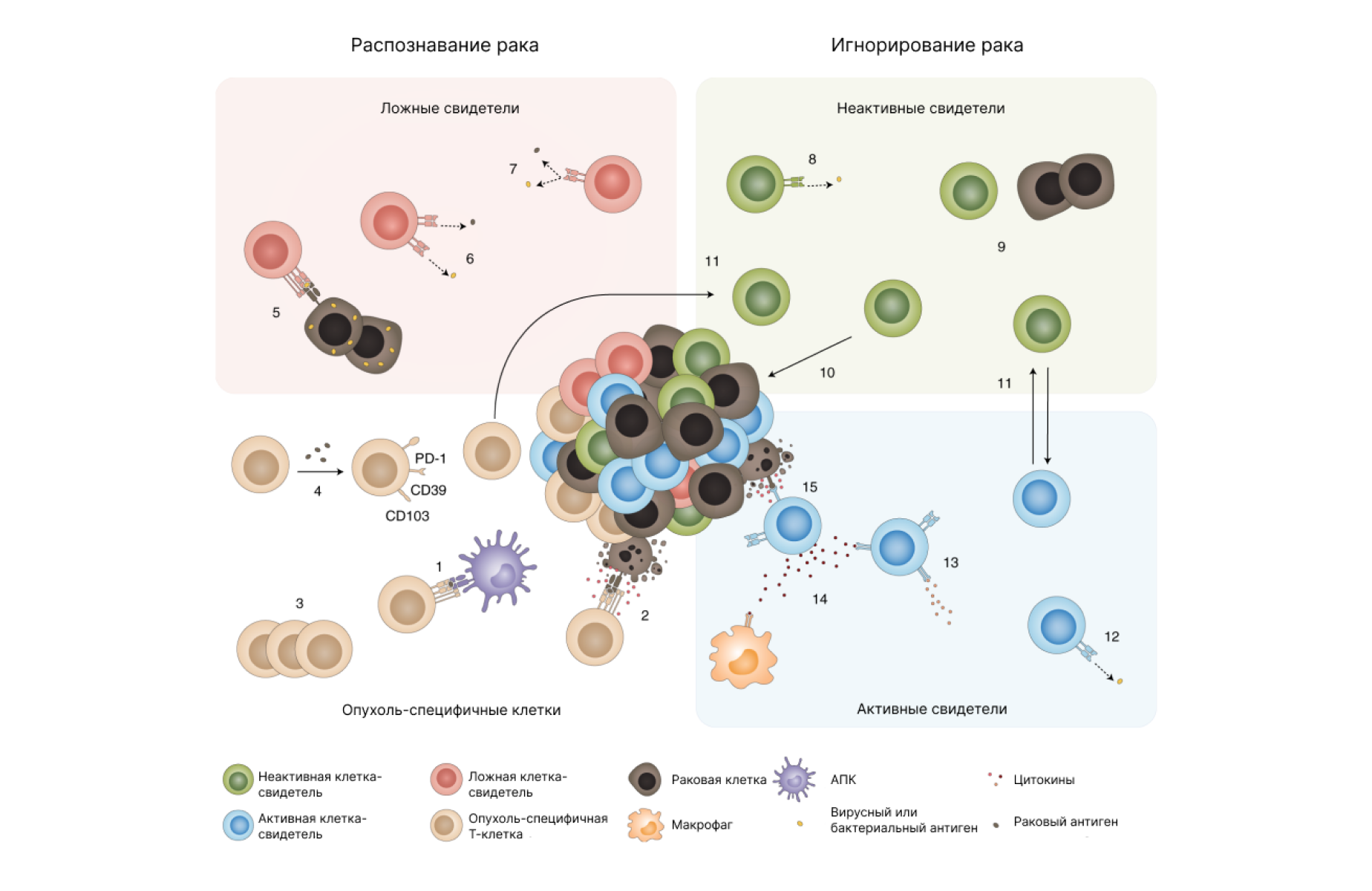
Разнообразие клеток в микроокружении опухоли. Источник: адаптировано из Nature Cancer
Как связаны показатели мутационной нагрузки и прогноз терапии с помощью анти-PD-1/PD-L1
Одним из наиболее важных прорывов в иммунотерапии рака стало открытие иммунных чекпоинтов, нацеленных на фактор запрограммированной клеточной смерти PD-1 или его лиганд PD-L1. Однако этот метод лечения эффективен не у всех пациентов. Ученые предполагают, что одной из возможных причин неуспеха терапии, связанной с PD-1/PD-L1, является высокая опухолевая мутационная нагрузка, или бремя опухоли (TMB, Tumor mutation burden). С помощью этого параметра измеряют общее количество мутаций в опухоли, чтобы оценить степень отторжения иммунных чекпоинтов и ответ опухоли на терапию. В недавнем исследовании оценили связь между TMB и результатами выживаемости среди 70 тысяч пациентов с устойчивыми видами рака. В результате удалось связать показатели TMB со степенью выживаемости, а также выявить восемь разновидностей рака, которые продемонстрировали специфическую связь между уровнем TMB и улучшением результатов при терапии с помощью анти-PD-1/PL–L1. — Tissue-specific thresholds of mutation burden associated with anti-PD-1/L1 therapy benefit and prognosis in microsatellite-stable cancers.
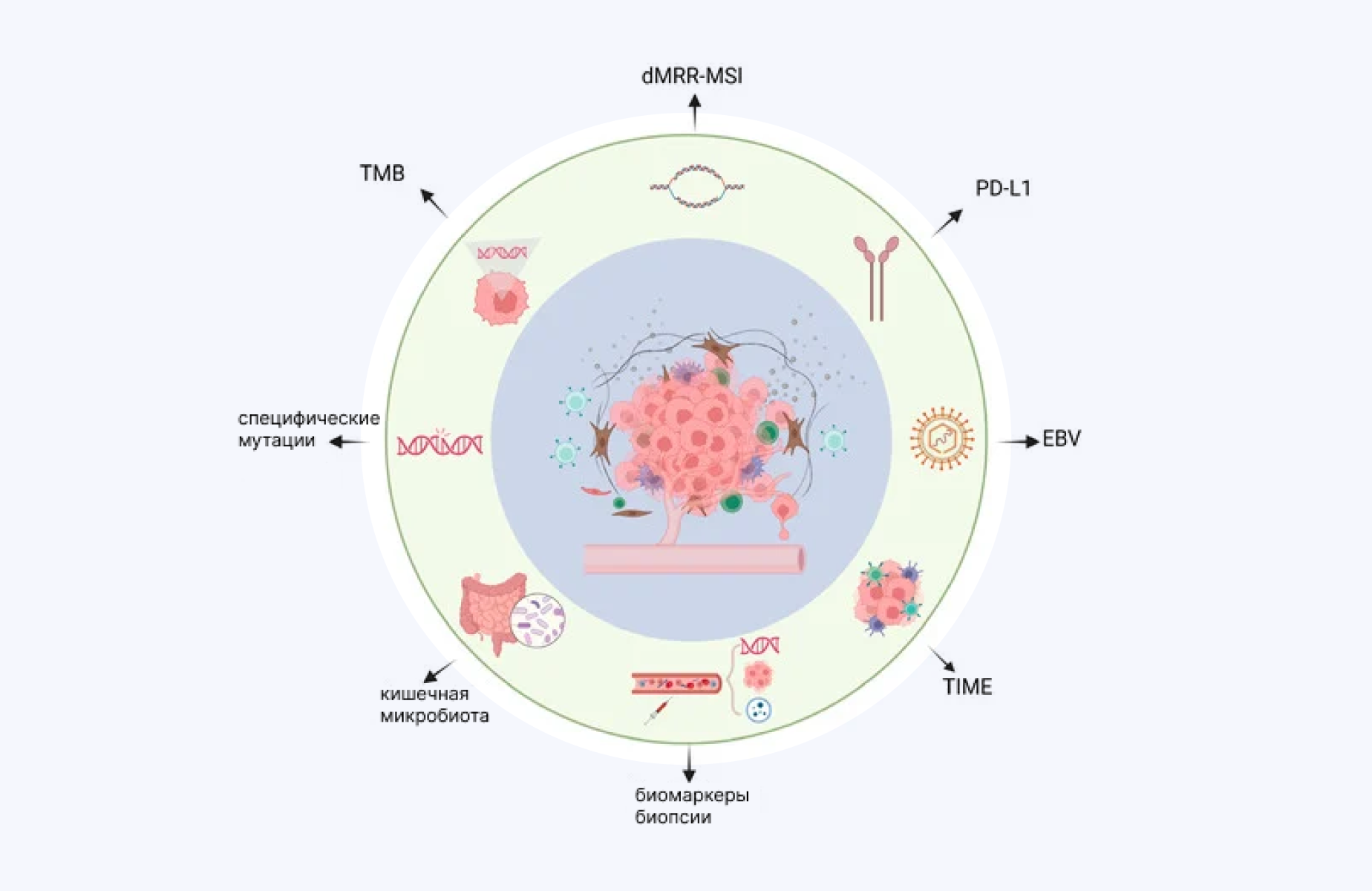
Источник: адаптировано из MDPI
PD-1/PD-L — важные, но не единственные иммунные чекпоинты. Кроме них, например, при раке желудка используют эффективную терапию ингибиторами против других контрольных точек, таких как dMRR/MSI, TMB, вируса Эпштейна — Барр (EBV), иммунного микроокружения опухоли (TIME) и т. д.
Аутоиммунные заболевания
Молекула-помощник для лечения рассеянного склероза
При рассеянном склерозе иммунная система по ошибке начинает разрушать миелиновые оболочки собственных нейронов в головном и спинном мозге. В результате этой демиелинизации нарушается передача сигналов нервной системы, что в конечном итоге приводит к быстро прогрессирующей нейродегенерации и инвалидности. На сегодняшний день зарегистрировано несколько препаратов, которые направлены на иммуносупрессию, чтобы снять воспаление и предотвратить дальнейшую потерю миелина. Но пока еще ни один из одобренных способов лечения не способствует эффективной ремиелинизации и смягчению прогрессирующей нейродегенерации. Однако недавно удалось охарактеризовать одну молекулу, которая потенциально способна помочь в этом направлении.
Один из маркеров воспаления у пациентов с рассеянным склерозом — лизофосфатидная кислота (LPA, Lysophosphatidic acid). Она представляет собой провоспалительный липид, уровень которого повышается в плазме и спинномозговой жидкости при рассеянном склерозе. Механизм действия LPA заключается в том, что этот липид активирует рецептор LPA1, в результате чего повышается уровень цитокинов и хемокинов в ЦНС и активируются клетки микроглии и астроциты. Это приводит к развитию нейровоспалительной реакции, из-за чего демиелинизируются нейроны и одновременно подавляются процессы ремиелинизации. Однако недавно удалось выявить антагонист LPA1 — селективный ингибитор PIPE-791, способный преодолевать гематоэнцефалический барьер (ГЭБ) и проникать в мозг. Эту молекулу уже охарактеризовали in vitro и in vivo: выяснилось, что она запускает дифференцировку клеток-предшественников олигодендроцитов и способствует ремиелинизации после предшествующих нейродегенеративных процессов. В исследованиях in vivo на мышиных моделях, которым вводили PIPE-791 перорально, удалось продемонстрировать, что молекула легко преодолевает ГЭБ и блокирует действие LPA1 в ЦНС. Эти результаты подтверждают потенциальное направление для лечения пациентов с рассеянным склерозом и другими иммуносупрессивными заболеваниями благодаря селективному ингибитору LPA1. — Discovery of a brain penetrant small molecule antagonist targeting LPA1 receptors to reduce neuroinflammation and promote remyelination in multiple sclerosis.
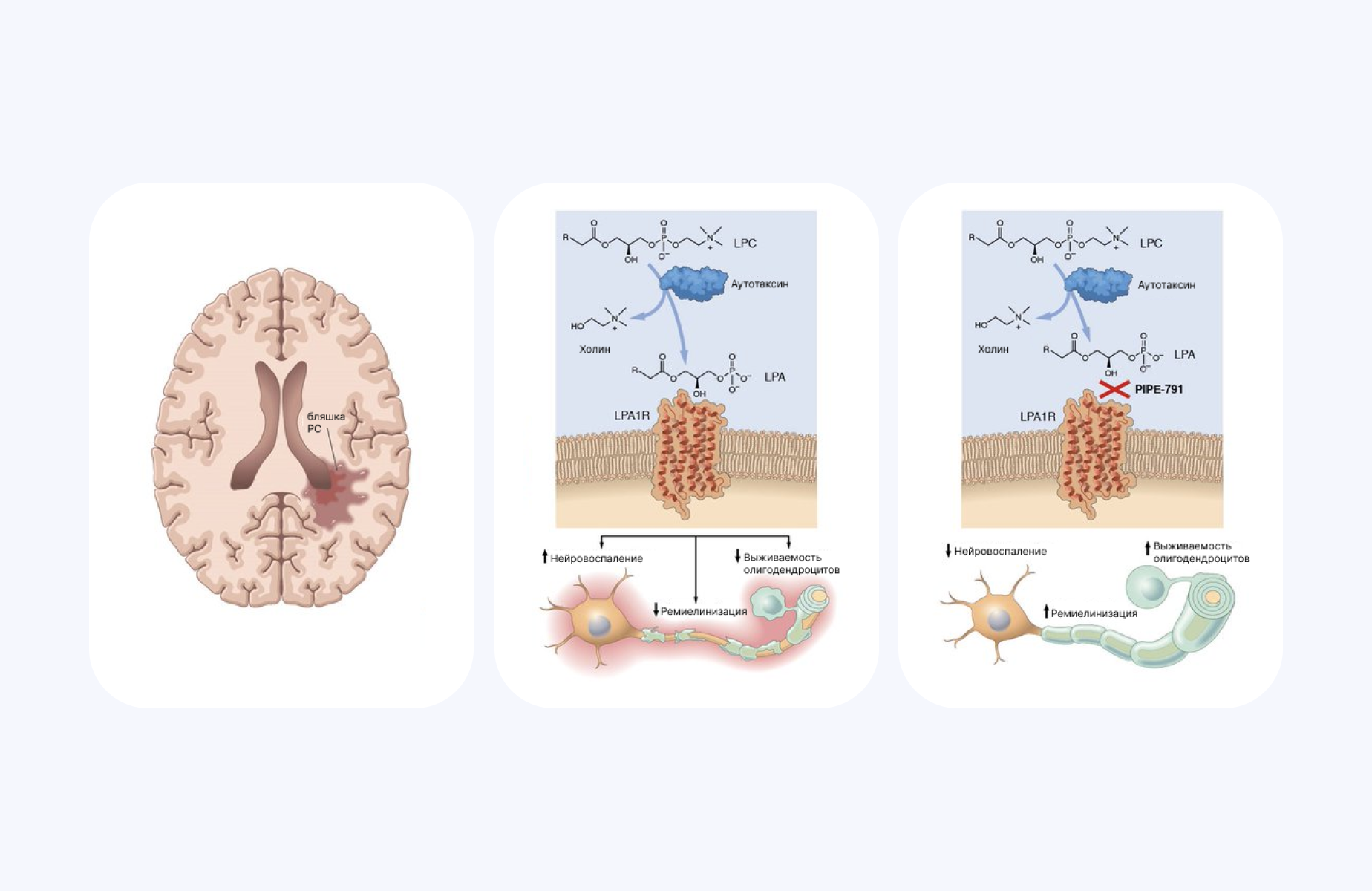
Источник: адаптировано из Nature Scientific Reports
При рассеянном склерозе на месте очагов демиелинизации в мозге возникают бляшки — один из важнейших маркеров воспаления. Суть нового подхода к лечению заболевания — использовать селективный ингибитор PIPE-791, который блокирует распознавание рецептором молекулы LPA1. В результате снижаются нейровоспалительные процессы, улучшается ремиелинизация и повышается количество олигодендроцитов.
Генная и клеточная терапии
Новый метод для оценки количества AAV
Масштабное производство векторов на основе аденоассоциированного вируса (AAV) для генной терапии пока еще остается ограниченным. Одна из причин, почему это происходит, — неизбежная выработка в процессе производства векторов пустых капсидов, которые не несут целевой геном. Более того, ситуацию осложняет еще и то, что пока еще не существует стандартизированного аналитического метода, который позволил бы оценивать количество нормальных векторов и «пустышек». Возможным решением этой проблемы может стать недавно разработанный метод CRAAVE (CRISPR-AAV Evaluation). Этот подход, основанный на CRISPR-технологии (CRISPR-Cas12a), позволяет надежно и за короткое время определять концентрацию генома AAV. Среди преимуществ метода — то, что он определяет титры AAV всего за полчаса, а количество ошибок составляет менее 3%. Возможно, метод CRAAVE станет новым инструментом для эффективного определения векторов с AAV и позволит более широко применять эту технологию в целях генной терапии. — Adeno-associated virus genome quantification with amplification-free CRISPR-Cas12a.
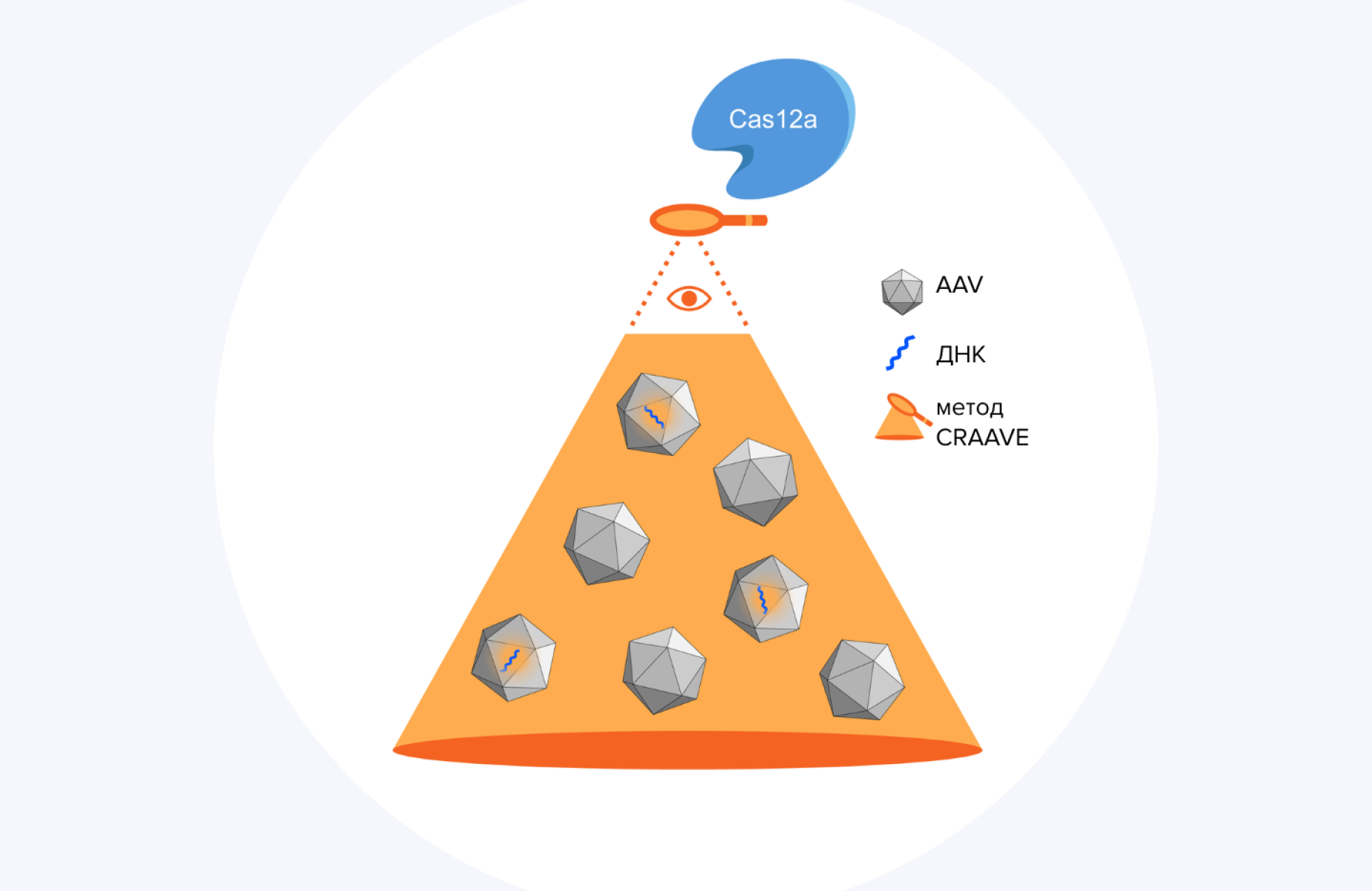
Источник: адаптировано из Nature Gene Therapy
Метод CRAAVE позволяет эффективно «отсеять» целевые векторы на основе AAV от пустых оболочек.
Как усовершенствовать применение векторов на основе AAV
Векторы на основе аденоассоциированных вирусов широко используются в терапии для доставки нужных генов в клетки. Однако в их применении есть и недостатки: небольшая емкость, ограниченный трансфер лишь в некоторые типы клеток, а также безопасность. Последний фактор уже давно вызывает вопросы, так как пока еще не существует четких регламентированных правил по работе с побочными продуктами, содержащими векторы. Недавно исследователи из Германии решили проанализировать этот процесс, чтобы оценить качество выделения AAV из мышей. Для этого животным сначала провели инъекцию AAV8 в ЦНС, а затем изучили состав биологических жидкостей испытуемых — слюны и мочи. При помощи метода количественной ПЦР удалось выявить фрагменты вирусной ДНК в течение четырех дней после инъекции AAV. Также ученые решили проверить функциональность AAV, но им не удалось обнаружить полноразмерные вирусные геномы ни в одном из анализируемых образцов, за исключением всего двух проб. Эти результаты позволяют сделать вывод о том, что необходимы новые адекватные правила в отношении биобезопасности при выделении AAV у животных. — A shedding analysis after AAV8 CNS injection revealed fragmented viral DNA without evidence of functional AAV particles in mice.
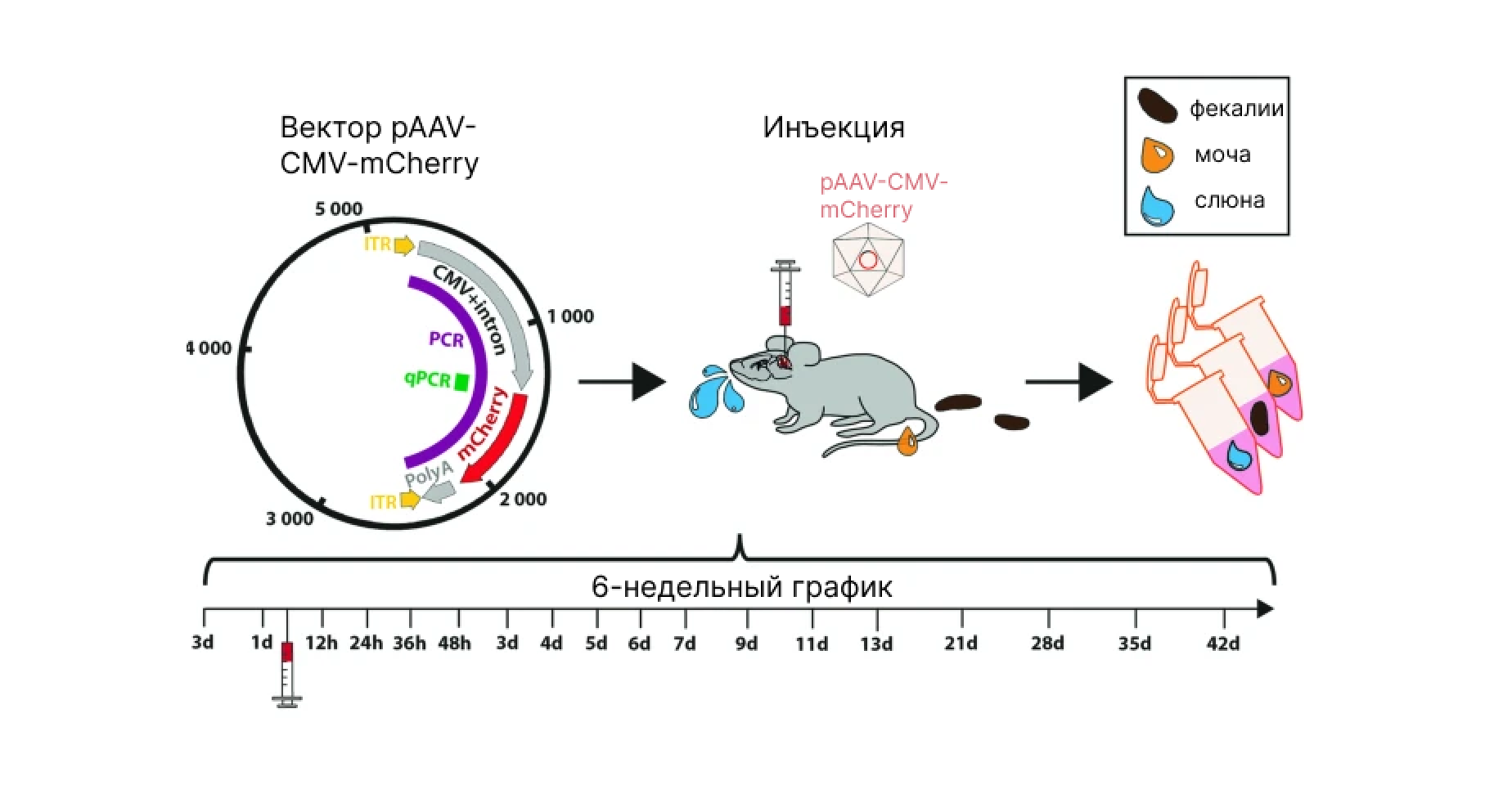
Источник: адаптировано из Nature Gene Therapy
Вектор pAAV-CMV-mCherry вводили шести мышам в мозжечок, после чего собирали образцы кала, мочи и слюны. Затем оценивали количество AAV в собранных образцах на протяжении шести недель после инъекции.