Дайджест #14. Братоубийство в клеточном мире
Клетки способны поглощать вещества множеством способов: захватывать капли и твердые кусочки, впячивать свою мембрану внутрь вместе с добычей — и даже кусаться! Процесс откусывания одной клеткой части другой клетки называется трогоцитозом и необходим, чтобы передавать различные сигналы, удалять ненужные компоненты или уничтожать врагов. Но еще трогоцитоз может приводить к клеточному братоубийству, когда Т-клетки считывают сигнал на уничтожение своих же собратьев. Подробнее об этом необычном явлении и способе его устранения при клеточной терапии рака читайте в новом дайджесте.
Онкология, клеточная терапия
Модифицированные и «неуязвимые» CAR-T-клетки для терапии лейкоза
Т-клеточный острый лимфобластный лейкоз — злокачественное заболевание крови и костного мозга, которое тяжело поддается лечению из-за высокой устойчивости к химиотерапии и возможными рецидивами. В недавнем исследовании среди пациентов с рецидивирующим Т-клеточным лейкозом применили новый способ терапии с помощью CAR-T-клеток. Особенность этого подхода была в том, что химерные Т-клетки экспрессировали анти-CD7 CAR и блокатор экспрессии белка анти-CD7 (PEBL). Благодаря этому удалось избежать так называемого Т-клеточного братоубийства (T-cell fratricide). Суть этого явления в том, что «переодетые» CAR-Т-клетки несут на своей поверхности пептид, который опознается как чужеродный, а значит, такая модифицированная клетка становится мишенью для других Т-клеток — и из-за этого введение химерных CAR-T-клеток приводит к их гибели. Новый подход, несмотря на высокую лейкозную нагрузку, позволил сделать терапию более успешной: 16 из 17 пациентов, участвовавших в исследовании, достигли полной ремиссии в течение месяца после лечения. Если смотреть на более долгосрочные результаты, то у 11 пациентов не было рецидивов болезни после 15 месяцев наблюдения. Эти результаты демонстрируют перспективность аутологичных анти-CD7 PEBL-CAR T-клеток для лечения Т-клеточного острого лимфобластного лейкоза. — Fratricide-resistant CD7-CAR T cells in T-ALL.
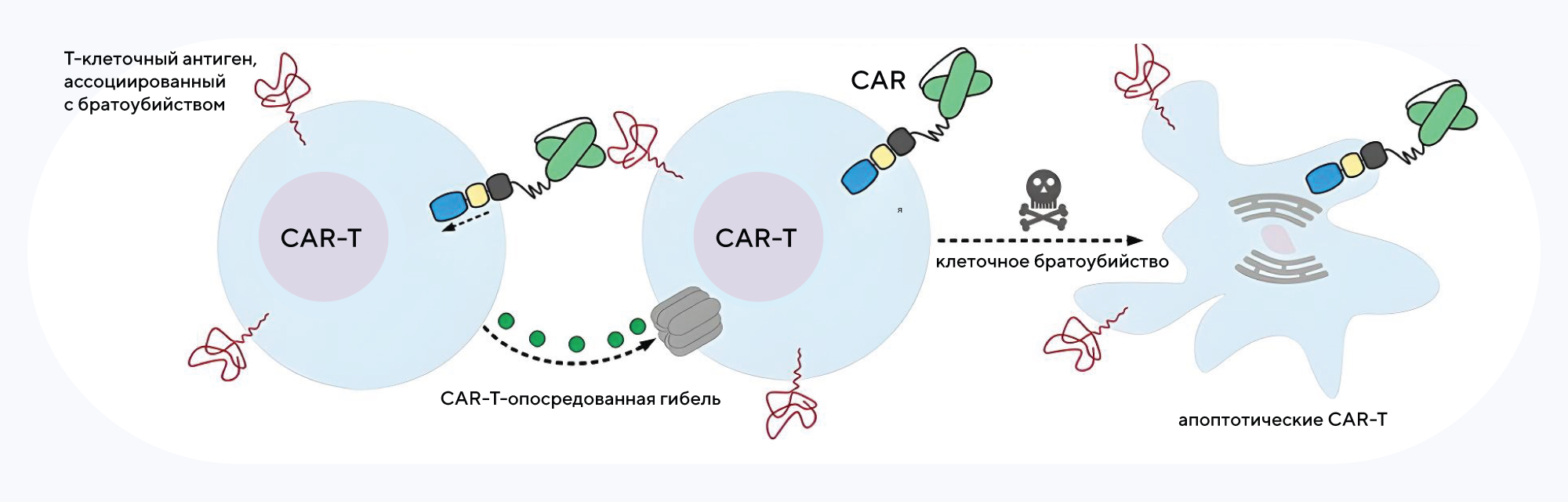
Сущность клеточного братоубийства: эффекторные Т-клетки видят специфичный для себя пептид на поверхности другой клетки, который воспринимается как чужеродный. Его узнавание и связывание распознается как сигнал к атаке — происходит Т-клеточное «братоубийство». Источник: адаптировано из ResearchGate
Что помогает персистирующим клеткам опухолей не сдаваться
Одна из наиболее важных проблем современной медицины — антибиотикорезистентность: чем больше и чаще нам назначают антибиотики, тем быстрее появляются новые штаммы, резистентные к лекарствам. Но не менее важным остается и вопрос устойчивости опухолевых клеток к лечению — раковая резистентность. Особую роль в устойчивости опухолей к лекарствам играют персистирующие клетки, изучаемые на протяжении последних 20 лет. Такие клетки отличаются высокой пластичностью: они способны переходить между разными клеточными состояниями. В результате внутри одной опухоли создается разнообразие клеточных фенотипов, что поддерживает ее устойчивость и «выживаемость». В обзоре суммируют все накопленные данные о персистирующих клетках: об их взаимодействии с опухолевым микроокружением, способах уклонения от иммунного надзора и о механизмах, которые обеспечивают им устойчивость к лекарствам. — Cancer drug-tolerant persister cells: from biological questions to clinical opportunities.
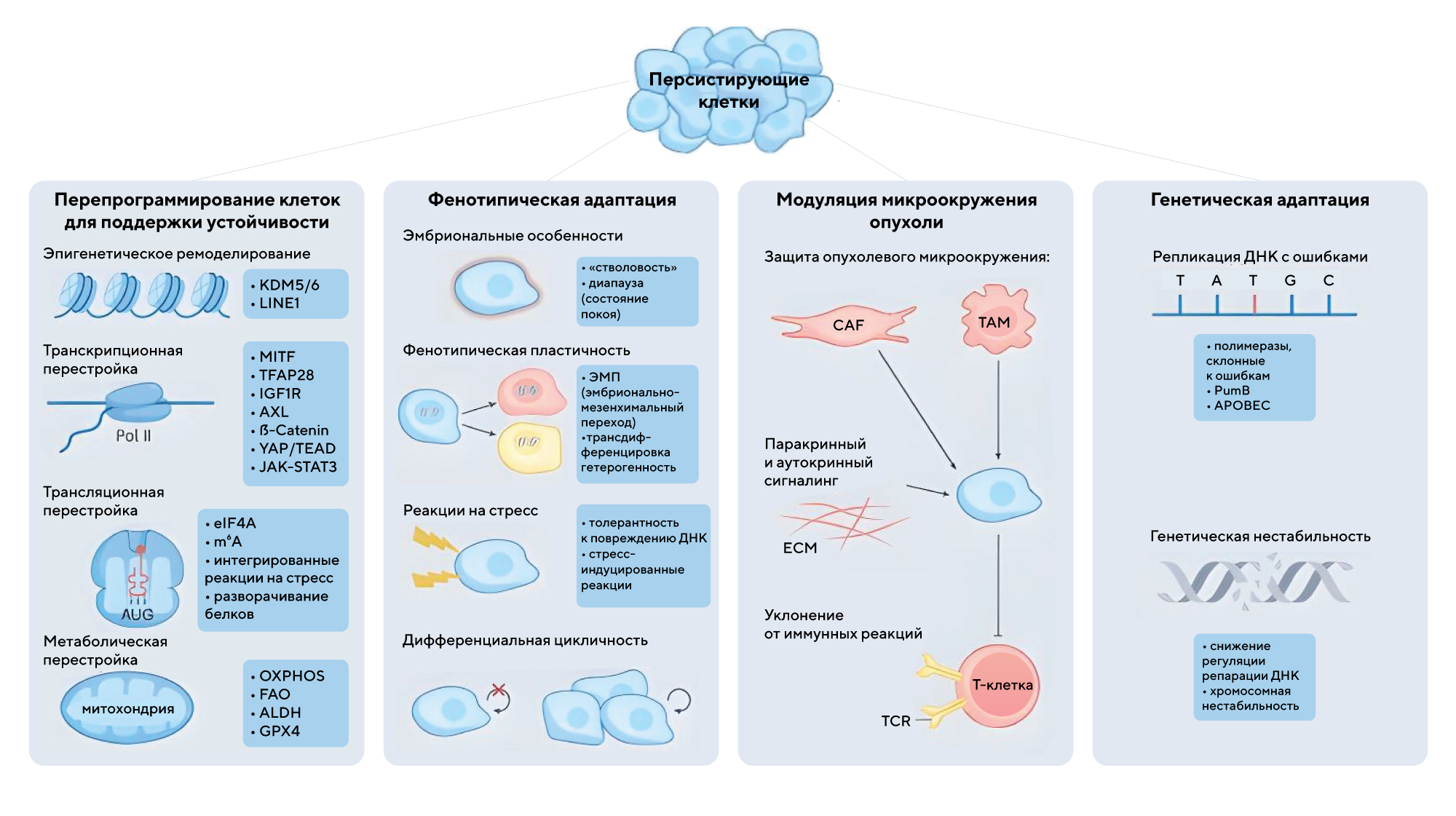
Чтобы уклоняться от противоопухолевой терапии, персистирующие клетки взяли на вооружение разные стратегии. Источник: Nature Reviews Cancer
Нацеливание на сосуды вокруг опухоли для терапии рака
Ангиогенез — процесс восстановления сосудов, который в норме происходит физиологично, например, при заживлении ран. Обычно этот процесс надежно контролируется факторами VEGF (фактор роста эндотелия сосудов), FGF (фактор роста фибробластов) и другими. Но если баланс факторов смещается, например, в сторону повышения, то это приводит к неконтролируемому росту сосудов. Устойчивый ангиогенез, связанный со стремительным ростом сосудов вокруг опухоли, способствует прогрессированию рака и распространению онкоклеток по всему организму. Попытки ударить по факторам ангиогенеза для лечения раковых заболеваний предпринимаются уже давно и задействуют множество разных способов — от ингибирования роста сосудов или их разрушения до перепрограммирования VEGF. Некоторые из этих подходов уже показали свою эффективность в сочетании с классическим лечением, но, к сожалению, часто такие стратегии ограничены конкретным видом рака. Недавно опубликовали обзор возможных способов нацеливания на сосуды вокруг опухоли, который обобщает накопленные сведения о влиянии ангиогенеза на прогрессирование и метастазирование опухолей. — Targeting the tumour vasculature: from vessel destruction to promotion.
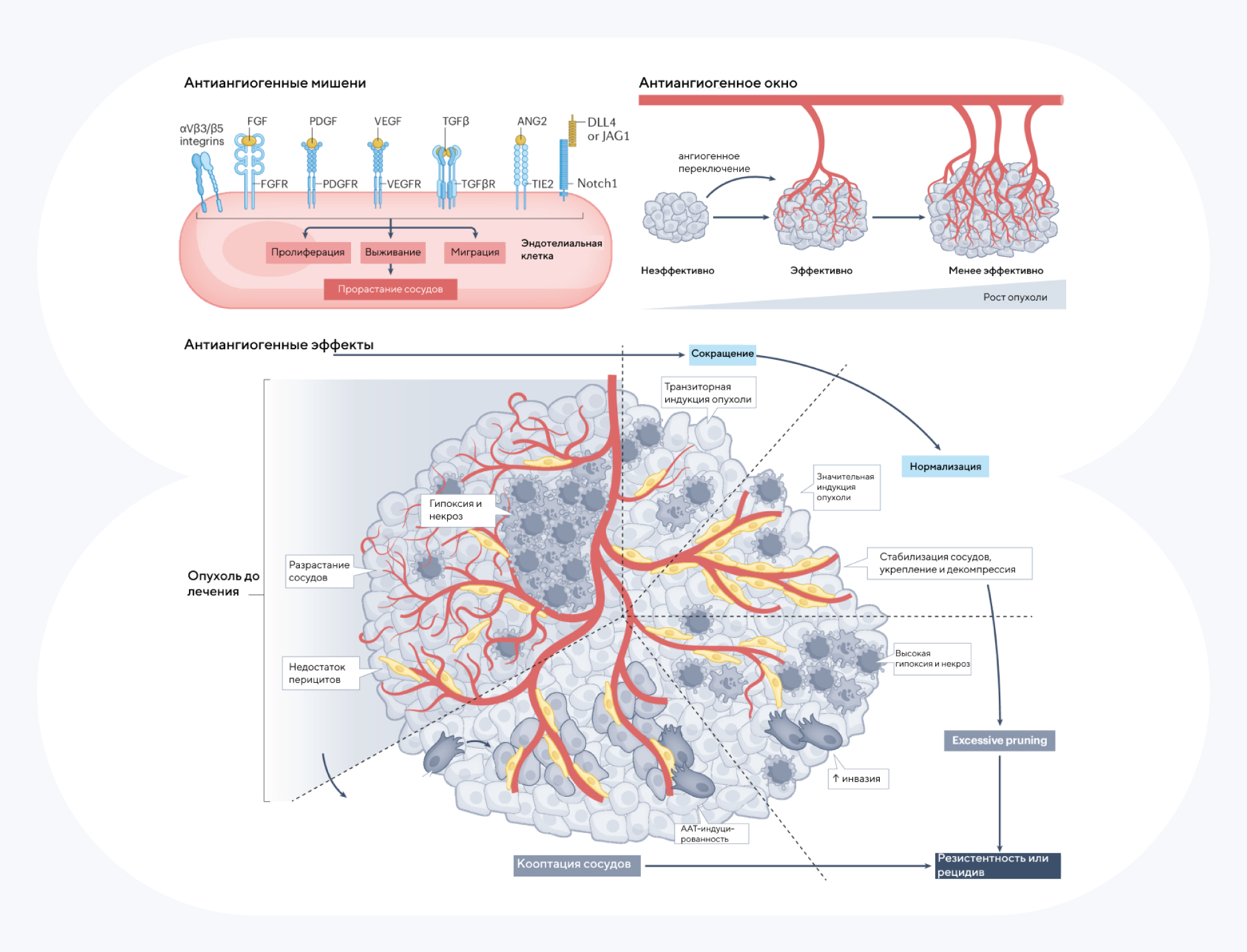
Накопленные знания об ангиогенезе в опухолях привели к альтернативным методам терапии рака, например к двойному нацеливанию на сосудистые и иммунные клеточные компартменты. Источник: Nature Reviews Cancer
Еще одна мишень для снижения метастазирования при РМЖ
Кавеолин-1 (Cav-1) — белок клеточной мембраны, который способствует образованию особых впячиваний (кавеол) и участвует в процессах эндоцитоза, в липидном обмене и в регуляции сигнальных путей. Однако у этого белка есть еще одно необычное свойство, делающее его «двойным агентом»: Cav-1 может быть как супрессором, так и промотором опухоли. Так, его экспрессия в разных типах опухолей может и повышаться, и снижаться. Недавно впервые удалось представить доказательства, что нокаут Cav-1 в эпителиальных клетках молочной железы значительно снижает метастазирование в легких. Клеточные эксперименты показали, что нокаут Cav-1 подавляет секрецию внеклеточных везикул и клеточную подвижность. А опыты in vivo на мышиных моделях продемонстрировали заметное снижение очагов метастазирования в легких. Эти результаты показывают один из возможных способов смягчить распространение метастазов при РМЖ и улучшить прогнозы заболевания. — Caveolin-1 knockout mitigates breast cancer metastasis to the lungs via integrin α3 dysregulation in 4T1-induced syngeneic breast cancer model.
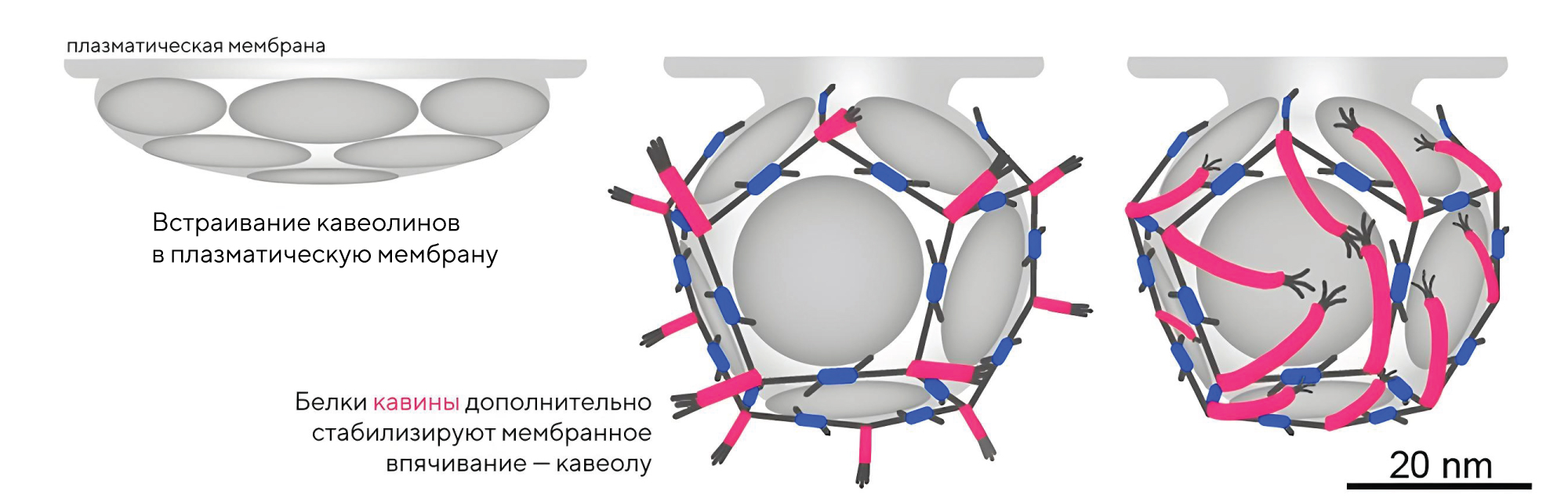
Кавеолин-1 играет особую роль в образовании мембранных впячиваний в форме буквы Ω — кавеол. Источник: PNAS
Клеточная неоднородность влияет на развитие рака желудка
Рак желудка — одно из самых распространенных онкологических заболеваний в мире. С его развитием и прогрессированием тесно связана аномальная активация сигнального пути Hedgehog, однако до сих пор не известны потенциальные терапевтические мишени в этом биохимическом каскаде. Чтобы глубже изучить роль пути Hedgehog при раке желудка, исследователи из Китая объединили данные одноклеточного секвенирования single-cell и метод пространственной транскриптомики. Интерес привлекли разнородные фибробласты, которые обладают разными свойствами. Эти различия связаны с циклином D1, CCND1, который играет важную роль на финальной стадии развитии фибробластов. Так, высокоинфильтрующие CCND1-положительные фибробласты являются фактором риска для пациентов с раком желудка и способны влиять на успешность применения химио- и иммунотерапии. Эти результаты показывают один из потенциальных способов раннего наблюдения и корректирования терапии при раке желудка. — Combined single cell and spatial transcriptome analysis reveals cellular heterogeneity of hedgehog pathway in gastric cancer.
Избыточная экспрессия циклина D1 наблюдается при некоторых видах рака, например при раке молочной железы, что делает его биомаркером заболевания. Источник: Википедия
Аутоиммунные заболевания
Обнаружен ключевой метаболит при ревматоидном артрите
Золотой стандарт в лечении ревматоидного артрита — метотрексат. Это вещество обладает выраженными противовоспалительными свойствами: так, метотрексат способен связываться с ферментами и выключать их биохимическую активность, блокируя воспаление. В новом исследовании решили сравнить пациентов с ревматоидным артритом, которых разделили на две группы: тех, кто лечился метотрексатом, и тех, у кого не было лечения. Цель этого исследования заключалась в том, чтобы провести метаболомный анализ эритроцитов и понять, существует ли разница в метаболитах до и после лечения. Выяснилось, что некоторые метаболиты накапливаются у людей с ревматоидным артритом, например валин и креатин, а другие, наоборот, снижаются — в их числе был эрготионеин. Так, у пациентов, которые проходили предварительную терапию метотрексатом, количество эрготионеина было значительно ниже, чем у тех, кто не ответил на терапию. Результаты исследования показывают, что низкий уровень эрготионеина в эритроцитах может стать своеобразным маркером заболевания и характерен для пациентов, которые ранее либо не принимали противовоспалительные препараты, либо не ответили на лечение метотрексатом. — Red blood cell metabolomics identify ergothioneine as a key metabolite in DMARD-naïve rheumatoid arthritis and response to methotrexate.
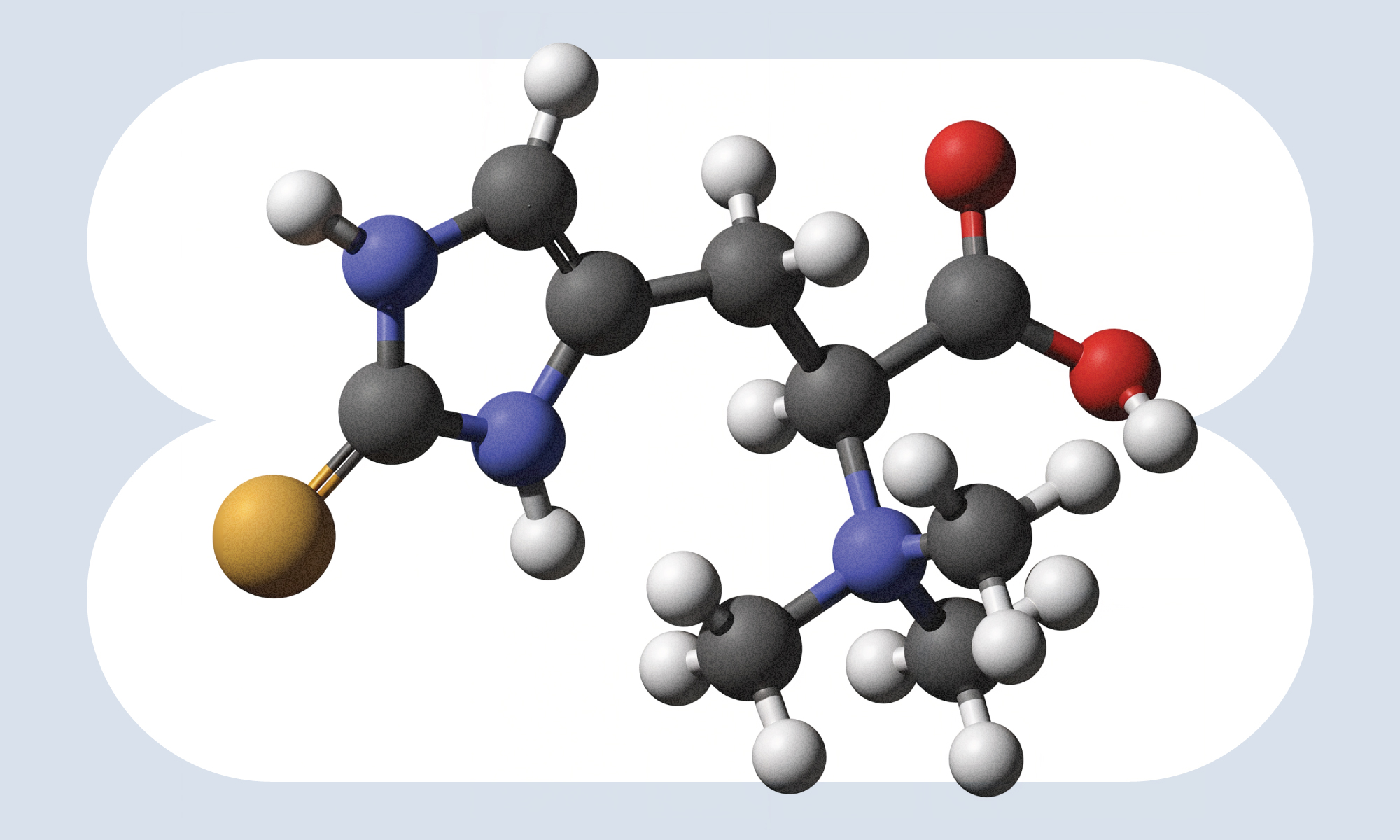
Эрготионеин — аминокислота, которая синтезируется некоторыми бактериями и грибами. В организм человека эрготионеин попадает с пищей и выполняет функции антиоксиданта. Источник: Википедия