
Дайджест #15. Маленькие молекулы против рака
Огромное количество процессов в нашем организме контролируется молекулами, которые долгое время не были известны и не считались серьезными регуляторами, — микроРНК. Эти небольшие некодирующие молекулы участвуют в экспрессии множества генов, среди которых могут быть и факторы, связанные с развитием рака. О том, какие микроРНК позволяют останавливать распространение метастазов и как удалось усилить их эффект с помощью генной терапии, читайте в новом дайджесте.
Появление агрессивных В-клеточных лимфом связано с белком DEK
В нескольких исследованиях уже удалось показать роль белка DEK в качестве протоонкогена и побочного «виновника» аутоиммунных заболеваний. В новой работе американских биологов получилось доказать связь между экспрессией DEK и повышенной пролиферацией опухолей в случае В-клеточных лимфом. Эти злокачественные новообразования развиваются в лимфатической системе и связаны с перерождением В-лимфоцитов. Выяснилось, что экспрессия DEK напрямую связана с агрессивным течением В-клеточной лимфомы. Чтобы обнаружить эту связь, ученые использовали модель клеточной линии с нокаутом гена DEK — в таких клетках с «выключенным» белком DEK снижалась способность к пролиферации и изменялись клеточные циклы. Но только сдвигами клеточных программ не ограничилось — клетки без DEK оказались более чувствительными к препаратам, вызывающим апоптоз, в частности к венетоклаксу и стауроспорину. Все эти результаты подчеркивают терапевтический потенциал DEK в качестве мишени, против которой стоит разрабатывать ингибиторы для лечения В-клеточного лимфоза. — DEK regulates B-cell proliferative capacity and is associated with aggressive disease in low-grade B-cell lymphomas.
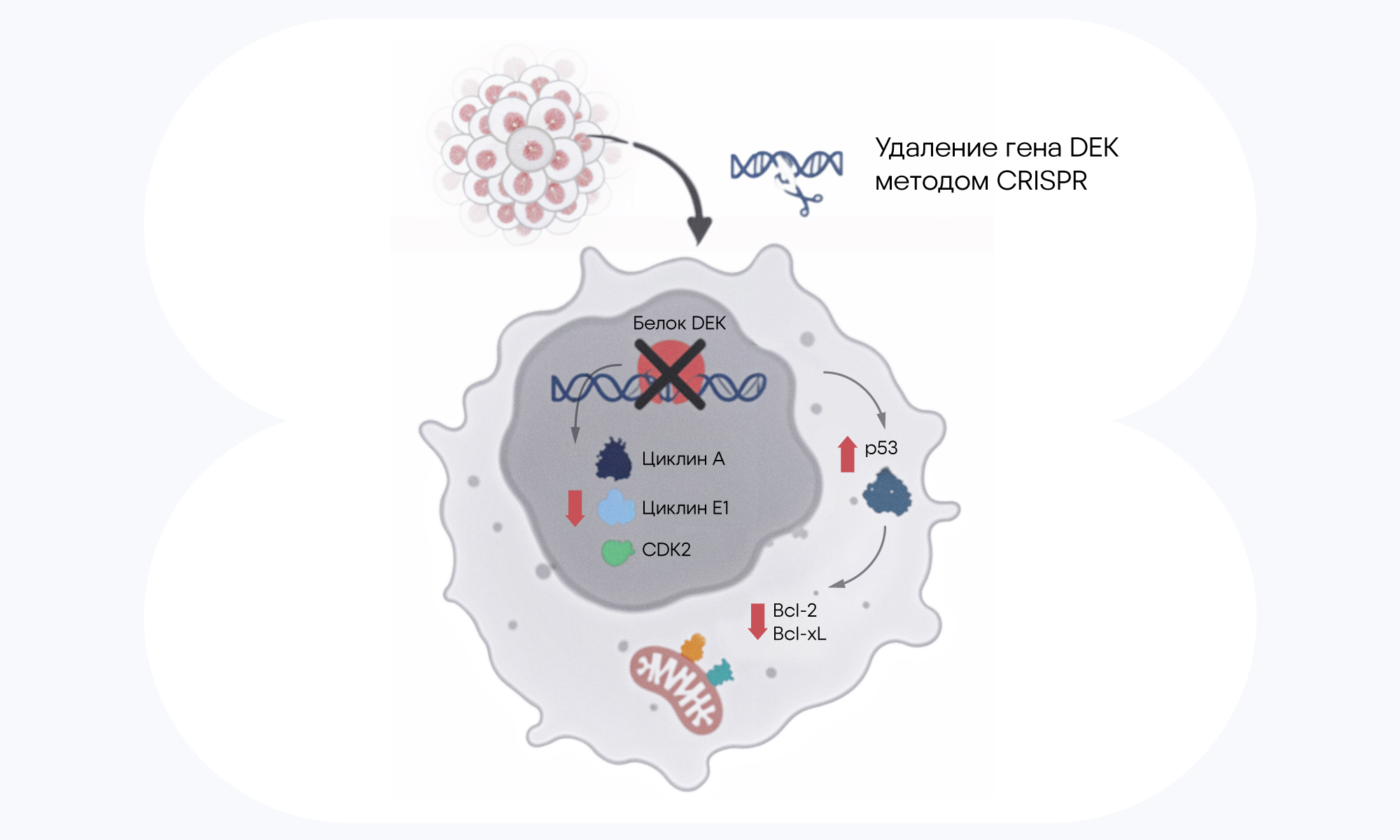
Источник: Blood Cancer Journal
В исследование включили клеточную линию с нокаутом гена DEK, который инактивировали методом CRISPR/Cas9. Это заблокировало выработку белка DEK, в результате чего снизилась экспрессия ключевых регуляторов клеточного цикла — циклинов, А и Е1, CDK2, а также регуляторов апоптоза — p53, Bcl-2 и Bcl-xL. В результате клетки теряли способность к неконтролируемому делению и становились восприимчивы к терапии.
Сравниваем эффективность анти-PD-1 препаратов
PD-1 — один из самых известных иммунных чекпоинтов, который ограничивает активацию Т-лимфоцитов. В результате в норме повышается аутотолерантность и снижается аутоиммунность. Но «в плохих руках» эти эффекты не работают во благо: опухолевые клетки могут использовать сигнальный путь с участием PD-1, чтобы уходить из-под иммунного надзора.
Иммунотерапия анти-PD-1 препаратами — одно из давно сложившихся направлений лечения разных видов рака. В BIOCAD также разработали рекомбинантное антитело пролголимаб против PD-1 для терапии солидных опухолей, например меланомы или рака легкого. Недавно сотрудники R&D-подразделения BIOCAD опубликовали в Nature Scientific Reports сравнительные данные доклинических исследований пролголимаба в сравнении с другими ранее одобренными противоопухолевыми препаратами — пембролизумабом и ниволумабом. Это сравнение показало, что пролголимаб активирует Т-лимфоциты и ингибирует рост солидных опухолей более эффективно, чем аналогичные препараты. — Preclinical comparison of prolgolimab, pembrolizumab and nivolumab.
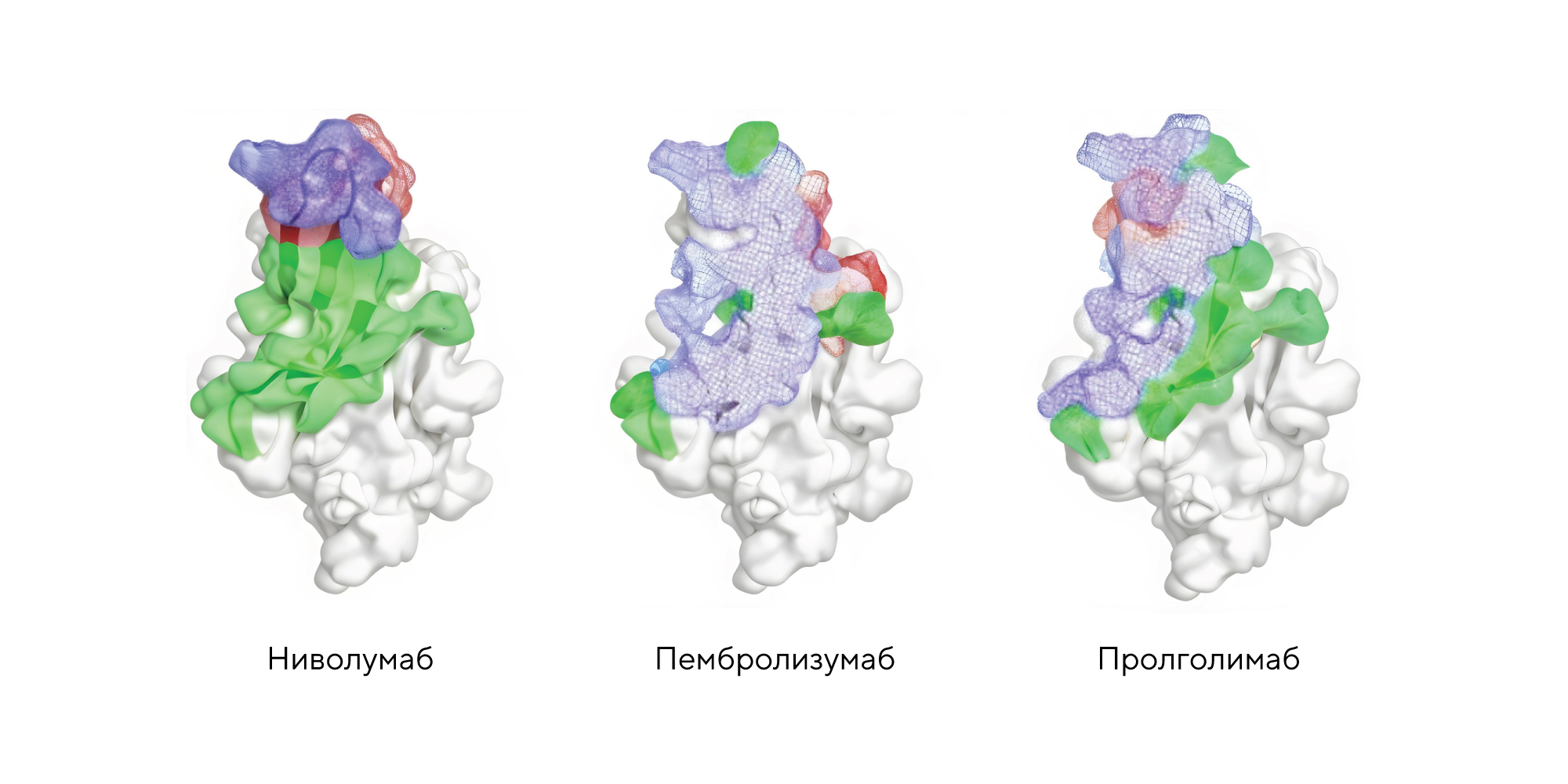
Принцип действия всех трех противоопухолевых препаратов — ниволумаба, пембролизумаба и пролголимаба — основан на блокировании взаимодействия между рецептором PD-1 и его основным лигандом PD-L1. На рисунке синим цветом обозначены перекрытия между регионом связывания PD-1 с антителами и собственным лигандом PD-L1 (чем больше по размеру область синего цвета, тем эффективнее антитело предотвращает связь между PD-1 и PD-L1). Зеленый цвет показывает часть региона связывания PD-1 с PD-L1, которая не перекрывается антителом. Красный цвет — часть эпитопа антитела к PD-1, который не относится к региону связывания с PD-L1.
Выявление рака по циркулирующей ДНК
В крови людей с онкологическими заболеваниями может обнаруживаться циркулирующая ДНК опухолевых клеток. Это небольшие фрагменты ДНК, которые свободно циркулируют в кровеносных сосудах. Многие онкотесты для раннего выявления рака направлены как раз на обнаружение этой ДНК. В недавнем исследовании ученые из Дании решили проверить, существует ли взаимосвязь между проявлением симптомов рака и выявлением циркулирующей опухолевой ДНК. Для этого они набрали две когорты пациентов с колоректальным раком: тех, у кого наблюдались выраженные симптомы болезни, и тех, у кого рак протекал бессимптомно. Выяснилось, что из крови бессимптомных пациентов выделяется незначительное количество опухолевой ДНК, в отличие от второй когорты — «симптоматических» участников исследования. Несмотря на кажущуюся очевидность этого вывода, полученные результаты дают важную информацию для разработки процедур раннего выявления рака у бессимптомных пациентов, особенно в случае рецидивов болезни. — Circulating tumour DNA and risk of recurrence in patients with asymptomatic versus symptomatic colorectal cancer.
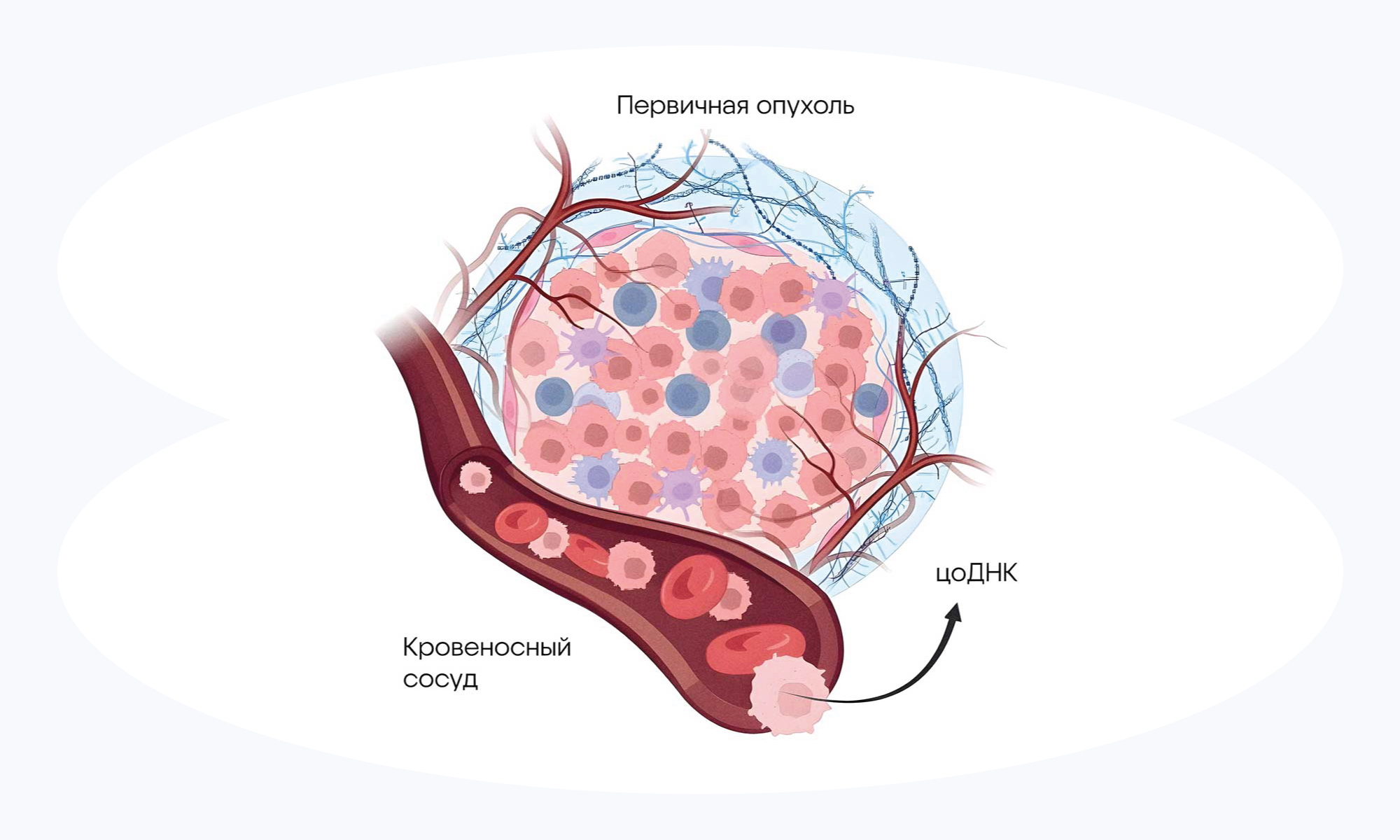
Циркулирующая опухолевая ДНК (цоДНК) может служить маркером воспалительного процесса, который не диагностируется рутинными методами исследования. Источник: «Википедия»
Обнаружена новая мишень для лечения глиобластомы
Глиобластома — злокачественная опухоль мозга, которая формируется из клеток глии. Свой вклад в развитие этого агрессивного новообразования могут вносить стволовые клетки. В нормальных условиях стволовые клетки дифференцируются и заменяют собой утраченные клетки. Но если программа развития дает сбой, стволовые клетки выходят из-под контроля и начинают безостановочно делиться — и в результате образуется опухоль. Наличие стволовых клеток в глиобластоме ухудшает прогноз течения болезни и повышает резистентность к терапии.
Ранее было показано, что при глиобластоме мозга в стволовых клетках экспрессируется фермент гамма-глутамилциклотрансфераза (ГГТ). Если же подавить экспрессию ГГТ, пролиферация онкоклеток останавливается. Чтобы лучше разобраться в молекулярно-генетических механизмах этого эффекта, ученые из Японии изучили модель глиобластомы у мышей. Выяснилось, что на экспрессию ГГТ влияют протоонкоген NRas и транскрипционный фактор c-Jun. Если ингибировать с-Jun и заблокировать NRas, останавливается деление опухолевых клеток. Эти результаты подсвечивают важность ГГТ, экспрессия которого опосредованно стимулируется с-Jun и NRas, в лечении глиобластомы. — γ-Glutamylcyclotransferase is transcriptionally regulated by c-Jun and controls proliferation of glioblastoma stem cells through Notch1 levels.
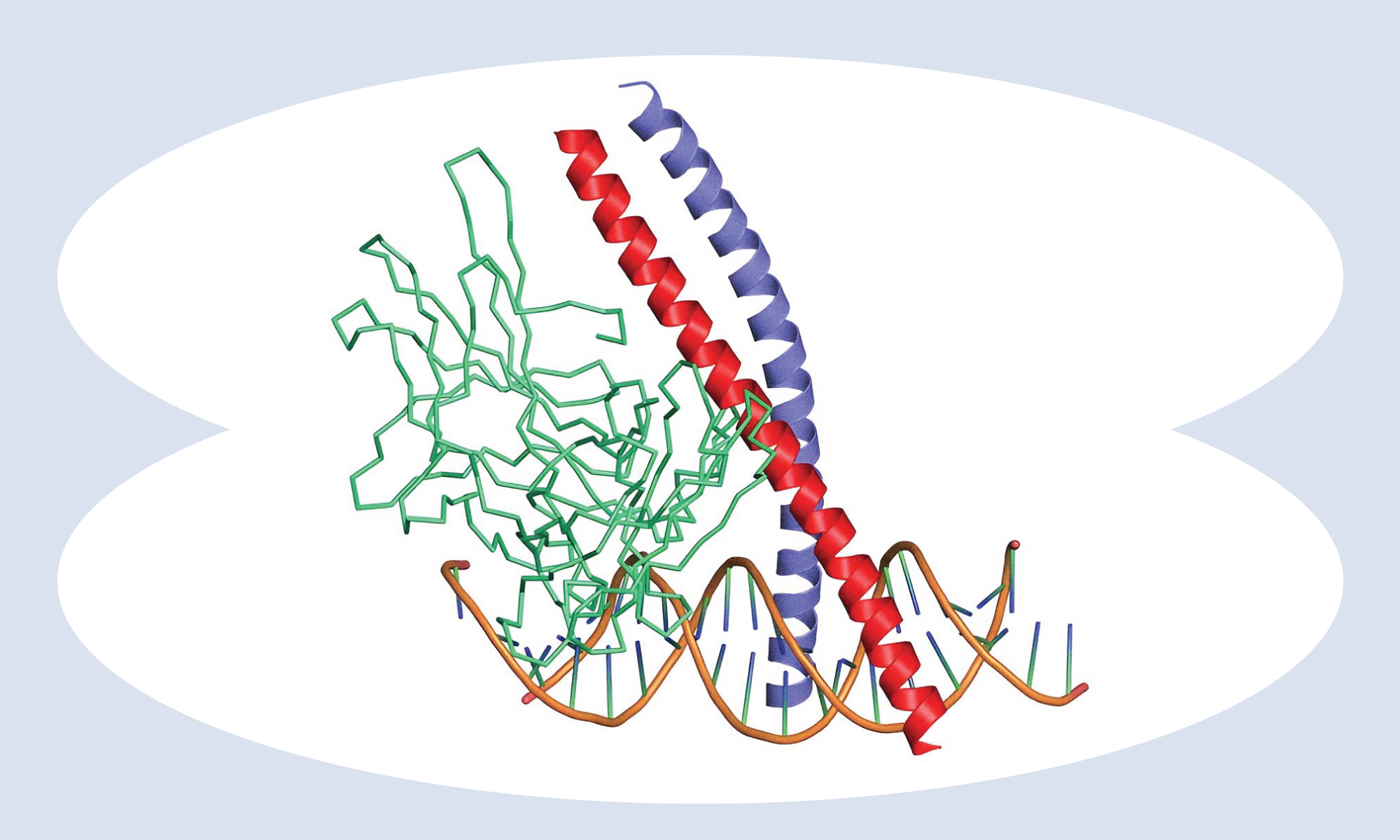
Транскрипционный фактор с-Jun в норме участвует в регуляции клеточного цикла и предотвращает апоптоз. Однако в случае поломок его неправильная работа запускает процессы онкогенеза. Источник: «Википедия»
Как снизить метастазирование с помощью генной AAV-терапии
Одним из самых серьезных заболеваний печени считается гепатоцеллюлярная карцинома, или рак печени. Выживаемость после выявления этого злокачественного новообразования обычно составляет менее одного года. Лечение рака печени во многом осложняется метастазированием, которое вызывается сверхэкспрессией HIF-1α — фактора, индуцируемого гипоксией 1-альфа. С помощью компьютерного моделирования было показано, что на экспрессию HIF-1α влияют некоторые микроРНК — так, экспрессия hsa-miR-199a-5p при гепатокарциноме приводит к подавлению экспрессии HIF-1α. Эти результаты позволили разработать схему генной терапии на основе аденоассоциированного вектора (AAV) с каспазой 9 (inducible caspase 9, iCasp9) и miR-199a. Проверяли эту схему на клеточной модели ксенотрансплантантов. Сначала терапевтический эффект проверяли только при участии микроРНК. В результате удалось показать, что сверхэкспрессия miR-199a примерно в два раза снизила уровень мРНК HIF-1α, уменьшая метастазирование и увеличивая уязвимость онкоклеток к цитотоксическим иммунным клеткам. Если же использовать комбинацию miR-199a и каспазы iCasp9, экспрессия HIF-1α снижалась еще значительнее, уже в четыре раза. Эти результаты продемонстрировали потенциал генной AAV-терапии с участием микроРНК и каспазы 9 для лечения рака печени. — AAV-mediated combination gene therapy of inducible Caspase 9 and miR-199a-5p is therapeutic in hepatocellular carcinoma.
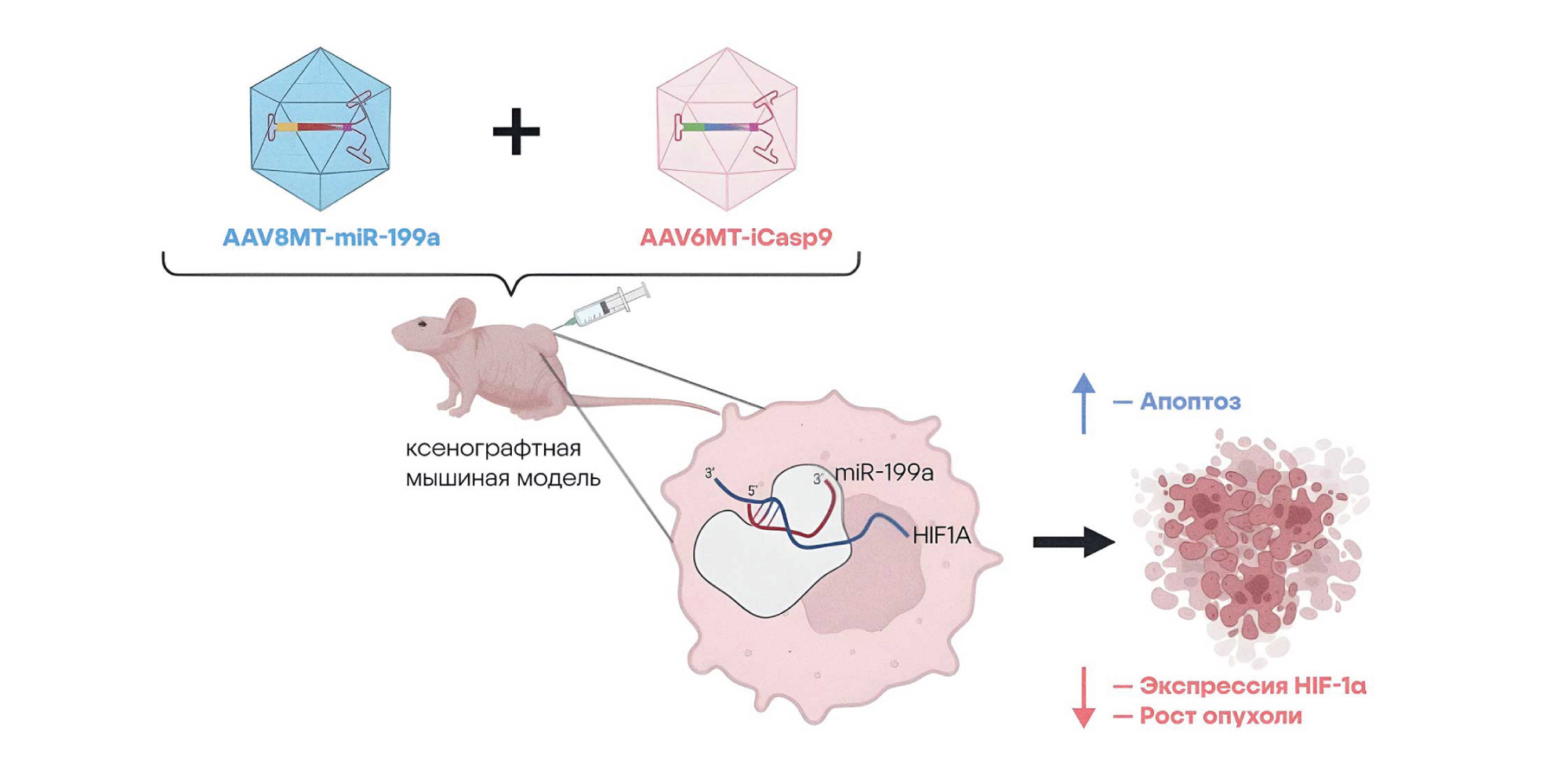
В исследовании проверили эффект комбинированной генной терапии с использованием микроРНК и каспазы 9 в составе вектора AAV для лечения рака печени. Источник: AAV-mediated combination gene therapy of inducible Caspase 9 and miR-199a-5p is therapeutic in hepatocellular carcinoma