
Когда стало ясно, что лекарства нужно контролировать: история фармаконадзора
Сегодня многим известно, что ни одно лекарство не бывает абсолютно безопасным. Но ученые поняли это не сразу. Еще сто лет назад о побочных эффектах чаще узнавали постфактум: по странным случаям в больницах, единичным заметкам аптекарей и крупным трагедиям, которые уже нельзя было предотвратить.
Фармаконадзору понадобился не один век, чтобы вырасти в систему, которая замечает риск раньше, чем он станет катастрофой. Подробнее о том, как развивался фармаконадзор и какую роль он играет в BIOCAD, расскажем в статье.
Эпоха зарождения, или Как люди поняли, что лекарства нужно контролировать
Фармаконадзор не сразу стал системой, которая быстро реагирует на нежелательные реакции и вовремя предупреждает риски. Заметить, что лекарство может не только помогать, но и вредить, до XIX века было сложно.
Препараты готовили малыми партиями в аптеках. И если лечебная смесь была загрязнена или содержала слишком высокую концентрацию действующего вещества, то страдали лишь несколько пациентов. Обычно они не связывали ухудшение состояния с лекарством, особенно если болезнь была тяжелой. Нежелательные реакции воспринимали как часть болезни или «слабость здоровья» и не думали о небезопасности препарата.
Ситуация начала меняться в XIX веке, когда производство лекарств стало массовым. Препараты перестали быть результатом работы одного конкретного аптекаря в уездном городе, а превратились в товар, который можно было изготавливать большими партиями, перевозить и продавать в другие города и страны.
Вместе с этим вырос и масштаб риска: одна ошибка в составе или дозировке уже представляла опасность не для одного человека, а для нескольких тысяч.
Одной из них стал британский закон — Pharmacy Act 1868, который ограничил продажу ядовитых и сильнодействующих веществ и закрепил, что их распространение требует надзора. Это еще не был фармаконадзор в современном понимании, но уже важный шаг к нему: государство признало, что лекарства нельзя рассматривать как обычный товар.
Трудный опыт на пути развития
Одного осознания того, что лекарства нужно контролировать, было мало. Не зря эксперты говорят, что правила эвакуации при пожаре написаны кровью. Так и история развития фармаконадзора состоит из крупных трагедий, из которых пришлось делать неутешительные выводы.
Урок от лошади по имени Джим
В начале XX века сыворотки и вакцины часто получали из крови животных. Одним из таких доноров была лошадь по имени Джим. Ее кровь использовали для производства противодифтерийной сыворотки в США.
В 1898 году ей начали вводить дифтерийный токсин. После этого в организме лошади вырабатывались антитела, а из ее крови производили сыворотку для лечения дифтерии. За три года благодаря Джиму ученые получили более 30 литров сыворотки, которая спасла множество жизней.
Но в 1901 году лошадь заразилась столбняком, поэтому ее пришлось усыпить. Однако сыворотку, полученную из ее крови, продали без проверки. В результате 13 детей умерли от столбняка после введения инфицированной сыворотки.
Эта история показала, что даже полезный препарат становится опасным, если не контролировать его производство. Недостаточно верить в лечебный эффект — нужно проверять каждую серию, следить за чистотой, условиями хранения и качеством сырья.
После этой трагедии в 1902 году в США приняли закон о контроле биологических препаратов — один из первых в своем роде. Он обязал государство проверять препараты в лаборатории, следить за тем, чтобы их производили в определенных условиях и по строгим правилам. Кроме того, по закону производитель должен был указывать на упаковке название препарата, срок годности, свой адрес и номер лицензии.
Что случилось с эликсиром сульфаниламида
В 1937 году американская компания S. E. Massengill выпустила жидкую форму популярного тогда антибиотика сульфаниламида — Elixir Sulfanilamide. Сам по себе сульфаниламид врачи уже активно применяли, но проблема была не в действующем веществе, а в растворителе.
Чтобы сделать препарат жидким, его развели в диэтиленгликоле. Это токсичное вещество, которое поражает почки и нервную систему. Но главный химик компании-производителя Гарольд Уоткинс об этом тогда не знал.
Получилось, что препарат поступил в продажу без полноценных испытаний на безопасность: тогда их проведение не было обязательным по законодательству. Через несколько недель по стране начали поступать сообщения о тяжелых отравлениях. Более 100 человек, среди которых были и дети, погибли от почечной недостаточности.
Эта история вскрыла главный дефект регулирования: закон не требовал доказывать безопасность лекарства до выхода на рынок. Общественный резонанс был настолько сильным, что уже в 1938 году в США приняли Федеральный закон о пищевых продуктах, лекарствах и косметических средствах (Federal Food, Drug, and Cosmetic Act). После этого FDA (Food and Drug Administration — Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США) получило полномочия требовать данные о безопасности лекарств, проверять производство и изымать опасные препараты с рынка.
Талидомидовая трагедия
В конце 1950-х годов талидомид продавали как успокоительное и средство от тошноты у беременных. Препарат считался почти безвредным: он не вызывал побочных реакций даже в высоких дозах и потому казался безопасным. Но вскоре врачи заметили, что у женщин, принимавших талидомид во время беременности, рождались дети с тяжелыми пороками развития — прежде всего с недоразвитием конечностей. По разным оценкам, пострадали более 10 тысяч детей в десятках стран.

Дети, рожденные от женщин, которые во время беременности принимали талидомид. Источник: The Standard
Трагедия с талидомидом показала, что препарат может не вызывать у взрослого пациента выраженных нежелательных эффектов, но при этом вмешиваться в развитие плода и приводить к тяжелым врожденным нарушениям. Для экспертов фармаконадзора это стало важным напоминанием о том, что безопасность лекарства нужно оценивать не только при краткосрочном, но и при длительном применении.
Почему появились «желтые карты»
В клинических испытаниях участвуют тысячи человек, а после регистрации препарат начинают принимать миллионы. Именно тогда могут проявиться редкие, отсроченные и неожиданные побочные реакции.
Так появилась система спонтанных сообщений о нежелательных реакциях. Одним из самых известных инструментов стала британская система Yellow Card Scheme, запущенная в 1964 году. Врачи получали специальные желтые бланки, на которых описывали побочные эффекты лекарства у пациента. Смысл был не в том, чтобы доказать вину препарата, а в том, чтобы заметить сигнал: если одно и то же осложнение описывают несколько врачей, лекарство нужно проверить.

Желтые карточки для сообщения о нежелательных реакциях на препараты, Великобритания, 1960-е годы
С этого момента медицина перестала считать регистрацию лекарства финальной точкой контроля над ним. Напротив, с момента выхода препарата на рынок начиналось новое наблюдение — уже в реальной практике. Позже к сообщениям подключили фармацевтов, медсестер и самих пациентов, а бумажные карточки превратились в электронные базы данных.
Фармаконадзор в России: от СССР до наших дней
В СССР лекарства проходили государственную экспертизу, а их использование контролировали через централизованную систему здравоохранения. Сведения о нежелательных реакциях стекались в научные институты, профильные комитеты и крупные клиники. Это помогало экспертам контролировать безопасность препаратов, но такая система плохо выявляла отсроченные побочные реакции.
Для централизованной системы этого было достаточно, пока рынок был сравнительно узким и государство контролировало почти весь путь препарата. Но с приходом рыночной экономики появились десятки новых производителей, импортные препараты, дженерики, новые схемы лечения. Старой модели контроля уже не хватало.
Именно тогда фармаконадзор начал превращаться в отдельную систему наблюдения за безопасностью.
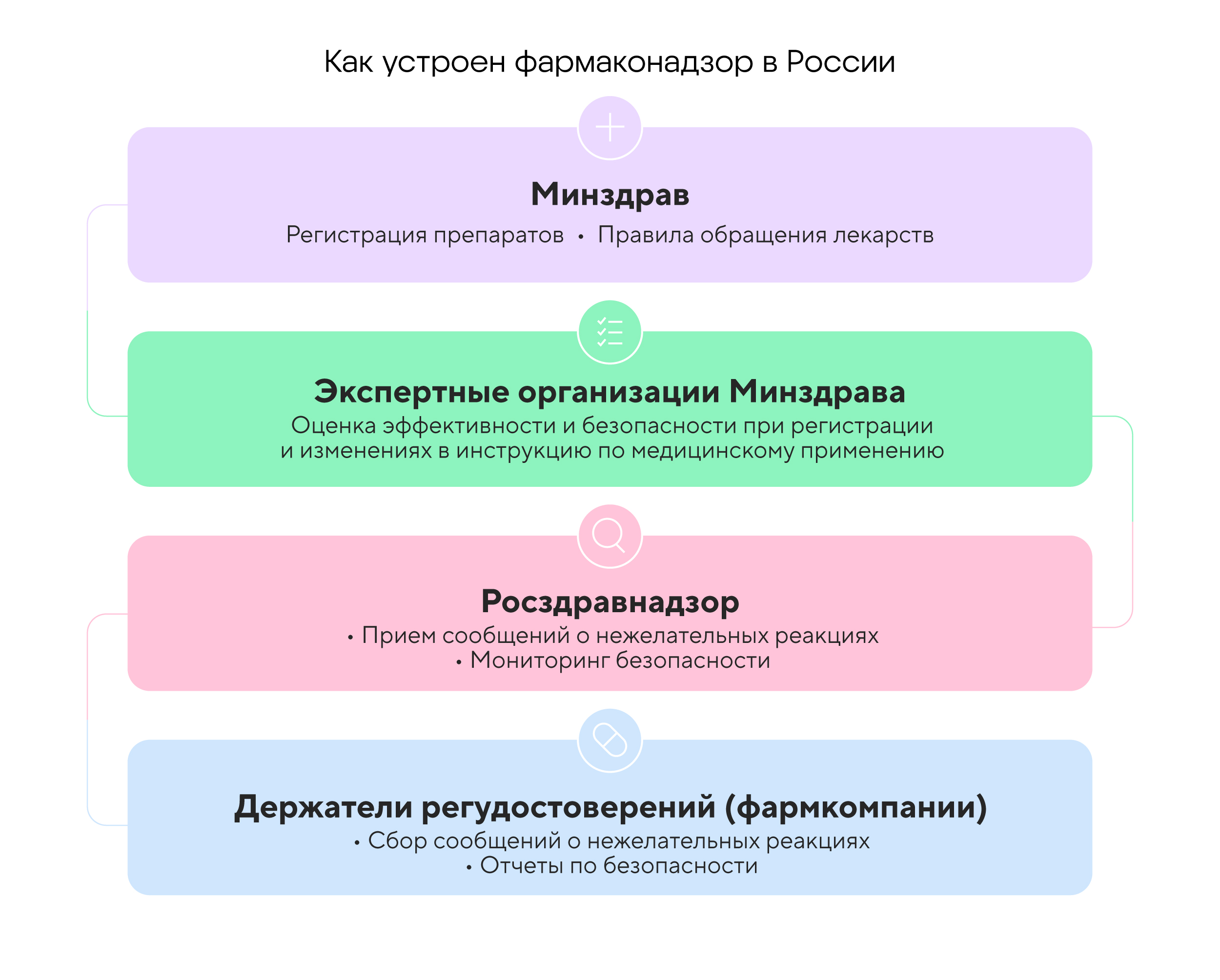
Как происходит в BIOCAD. В компании уверены, что безопасность препарата так же важна, как и эффективность. Поэтому фармаконадзор в BIOCAD — это не формальная функция отдельного подразделения, а часть общей системы ответственности за пациента.
Каждый сотрудник компании — участник системы фармаконадзора. Чтобы система работала без сбоев, все сотрудники проходят обязательное обучение по фармаконадзору не реже одного раза в год. Все должны знать, что делать, если получают сообщение о нежелательной реакции.
Система фармаконадзора в компании также представлена Отделом безопасности лекарственных средств Департамента клинической разработки.
Ежегодно сотрудники Отдела безопасности лекарственных средств обрабатывают до двух тысяч сообщений из 30 стран активной регистрации препаратов. И делают это максимально точно: в каждый сложный кейс погружается один сотрудник. То есть в отделе действует правило: 1 случай — 1 сотрудник. Так удается сократить время обработки заявок: даже в сложных случаях оно не превышает 24 часов.

В безопасности препарата важна роль каждого
Мир давно отказался от идеи, что лекарство можно один раз проверить перед регистрацией и на этом успокоиться. После крупных трагедий в США и Великобритании контроль стал непрерывным: препарат изучают до выхода на рынок, а затем еще внимательнее — после начала массового применения.
Врачи, фармацевты, производители и сами пациенты могут сообщать о нежелательных реакциях. Даже если связь с препаратом пока не доказана, информация все равно важна: именно из таких сообщений часто формируется первый сигнал.
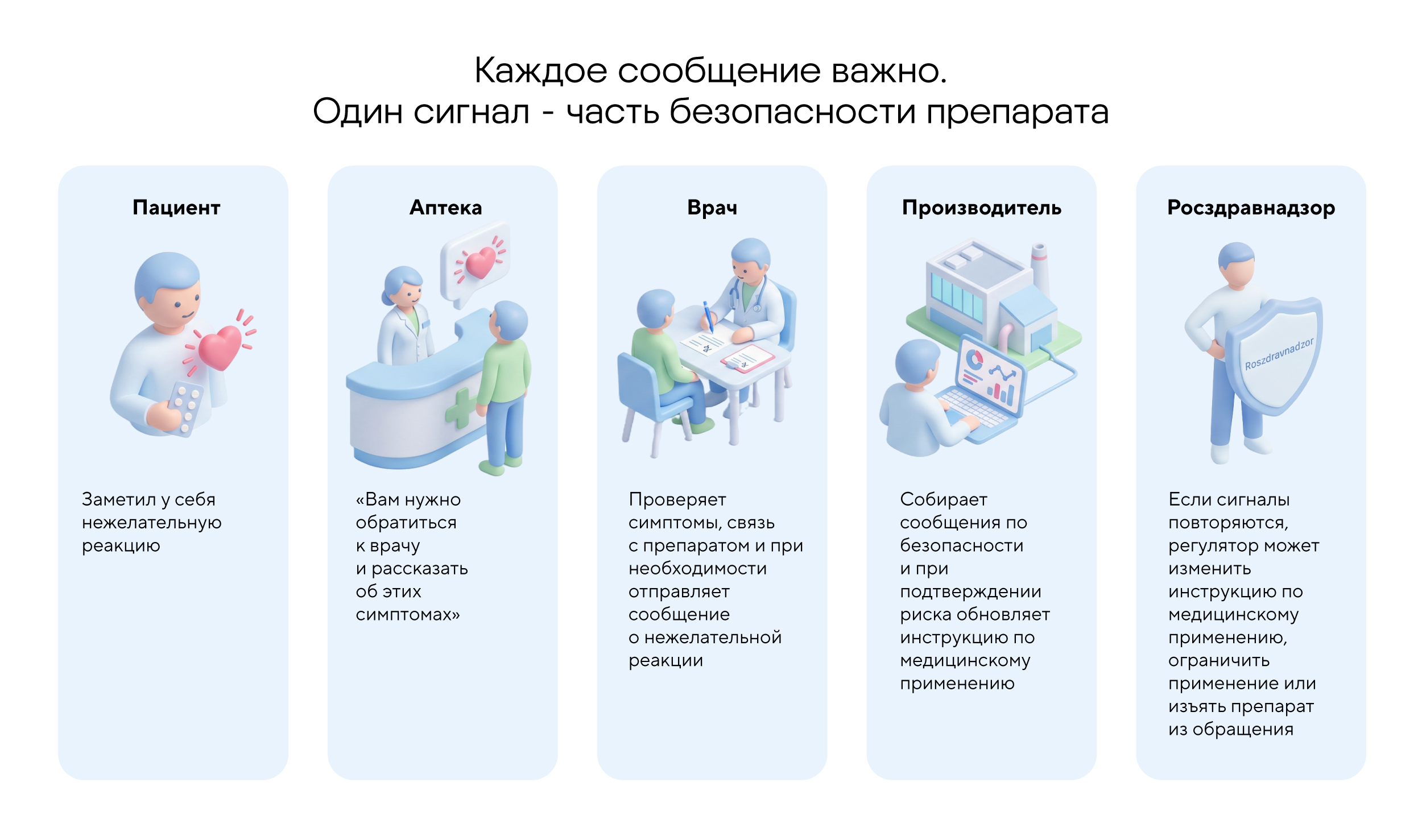
Сегодня фармаконадзор — это международная сеть, которая в своей работе опирается на базы данных, пострегистрационные исследования и быстрый обмен информацией между странами.
Базы данных. У крупных регуляторов есть собственные базы: например, в США работает FAERS, в Евросоюзе — EudraVigilance. На глобальном уровне важную роль играет программа ВОЗ и база VigiBase, куда поступают сообщения из многих стран. Ее задача — как можно раньше заметить угрозу и помочь принять решения, например внести изменения в инструкцию по медицинскому применению препарата.
Сегодня сигналы ищут не только вручную. Используют алгоритмы статистического анализа и электронные медкарты, иногда — инструменты машинного обучения. Это помогает быстрее замечать нетипичные реакции и оценивать риски.
Но полностью заменить экспертную оценку технология пока не может. Любой сигнал нужно проверить: выяснить, не объясняется ли эффект сопутствующими болезнями, другими препаратами или ошибками при приеме препарата.
Обмен информацией между странами. Безопасность лекарства больше не оценивают только внутри одной страны. Если сигнал появился в России, Китае или США, он быстро становится предметом внимания и в других регионах. Ведь многие препараты, в том числе вакцины, применяют во всем мире.
Пострегистрационные исследования. Результатов клинических исследований (КИ) может быть недостаточно для понимания общей картины. Препарат принимают дольше, в сочетании с другими средствами, на фоне хронических заболеваний, иногда с нарушением дозировки или инструкции по медицинскому применению. Именно тогда могут проявиться редкие и отсроченные реакции. Поэтому пострегистрационные исследования необходимы командам фармаконадзора: благодаря им они дополняют информацию, полученную в результате КИ.
Сегодня фармаконадзор считается одной из опор современной системы здравоохранения. Он не делает лекарства абсолютно безопасными, это невозможно. Но позволяет вовремя видеть риски и постепенно снижать их.
Памятка «Что делать, если заметили у себя нежелательную реакцию, которая не описана в инструкции по медицинскому применению препарата»
Шаг 1. Обратитесь к лечащему врачу и подробно опишите нежелательную реакцию. Возьмите на прием лекарственный препарат в упаковке. Доктор уточнит:
- производителя препарата;
- торговое наименование лекарственного средства;
- номер и серию партии;
- дозировку;
- режим приема и способ введения;
- дату начала и окончания терапии.
Шаг 2. Попросите врача заполнить «Извещение о нежелательной реакции или отсутствии терапевтического эффекта лекарственного препарата». Скачать форму можно на сайте Росздравнадзора.
Важно отметить, что документ может заполнить только человек с медицинским образованием. Заполненное извещение можно направить в центральный аппарат или территориальный орган Росздравнадзора по почте либо на электронный адрес roszdravnadzor.ru.
Шаг 3. Сообщите о нежелательной реакции производителю препарата. Можно связаться с компанией-производителем через ее официальный сайт, где обычно есть форма обратной связи, а также по телефону горячей линии или электронной почте.
Шаг 4. Дождитесь ответа от Росздравнадзора: обычно это занимает до 30 дней с момента регистрации обращения. При необходимости регулятор может запросить у вас или лечащего врача дополнительную информацию о препарате, течении реакции, сопутствующем лечении и результатах обследований.