
Как стать Qualified Person: интервью с экспертами по качеству
Когда мы говорим о том, что качественно выполняем свою работу, каждый может представить что-то свое: хороший результат без переделок и досадных ошибок, тщательное планирование, вложение сил и энергии… Но когда речь заходит о работе в сфере качества, ассоциации придумать сложнее. Чтобы лучше в этом разобраться, мы пообщались с сотрудниками разных подразделений Направления «Качество» в компании BIOCAD. Из этого интервью мы узнаем, с какими задачами регулярно сталкиваются уполномоченные лица по качеству, в чем разница между контролем и обеспечением качества, а также почему при производстве лекарственных препаратов важна каждая деталь — от расположения приборов в лаборатории до цвета колпачка на флакончике.
Как обеспечивают и контролируют качество в фарминдустрии
Качество терапевтических продуктов — важнейшая их характеристика, так как степень качества лекарства напрямую влияет на жизнь и здоровье людей. Процесс контроля качества на каждом из этапов разработки и производства терапевтических средств строго регламентирован. Чтобы погрузиться в каждый из процессов контроля и обеспечения качества, пришлось бы написать целый цикл статей. Поэтому ограничимся упрощенным определением качества: это соответствие всех характеристик лекарства (подлинности, дозировки, чистоты и др.) его целевому назначению — лечению конкретной болезни и популяции пациентов, а также требованиям государственной регистрации. Перед выпуском лекарства на рынок нужно обязательно удостоверить его соответствие заявленной цели и показать, что терапевтический продукт способен эффективно и безопасно лечить конкретную болезнь. Этим подтверждением в BIOCAD занимаются уполномоченные лица по качеству (или Qualified Person, если говорить на языке GMP — Правил надлежащей производственной практики). Уполномоченные лица подтверждают, что производство каждой серии лекарственного препарата было проконтролировано в соответствии с требованиями регистрационного досье и GMP.
«Уполномоченное лицо — это уникальный специалист, к которому на законодательном уровне предъявляются очень строгие требования к навыкам и компетенциям. Это „верховный судья“, который анализирует полное „дело“, где описан весь жизненный путь произведенной серии — от ее зарождения из сырья и материалов, последовательных стадий производственных операций до финальных результатов контроля качества, — и выносит окончательный вердикт: достаточно ли у нас доказательств того, что серия может быть выпущена в обращение. Фактически уполномоченное лицо допускает препарат к применению среди пациентов. Это огромная ответственность, как формальная, так и моральная, ведь ничего идеального в этом мире не бывает. Именно уполномоченное лицо принимает решение, насколько мы уверены в том, что качество не пострадало, если хоть что-то пошло не так. Своей подписью уполномоченное лицо дает „зеленый свет“ на реализацию результатов труда всех подразделений компании, ведь наша главная общая цель — обеспечить тех, кто остро нуждается в наших препаратах, надежным средством для выздоровления и улучшения качества жизни», — Елена Арькова, вице-президент BIOCAD по качеству.
Качество терапевтического препарата закладывают еще на этапе ранней разработки и продолжают непрерывно контролировать на протяжении всего жизненного цикла. Например, если в ходе фармацевтической разработки или доклинических исследований появится новая информация о стабильности качества продукта, эти характеристики будут контролировать в процессе производства.
Качество лекарственных препаратов потребитель не может оценить самостоятельно, ведь для этого требуются сложные лабораторные исследования. При этом здоровье и зачастую жизнь пациента напрямую зависят от эффективности и безопасности принимаемой терапии. Поэтому мы, как производитель, должны сделать так, чтобы некачественные продукты по умолчанию не могли бы попасть к пациентам.
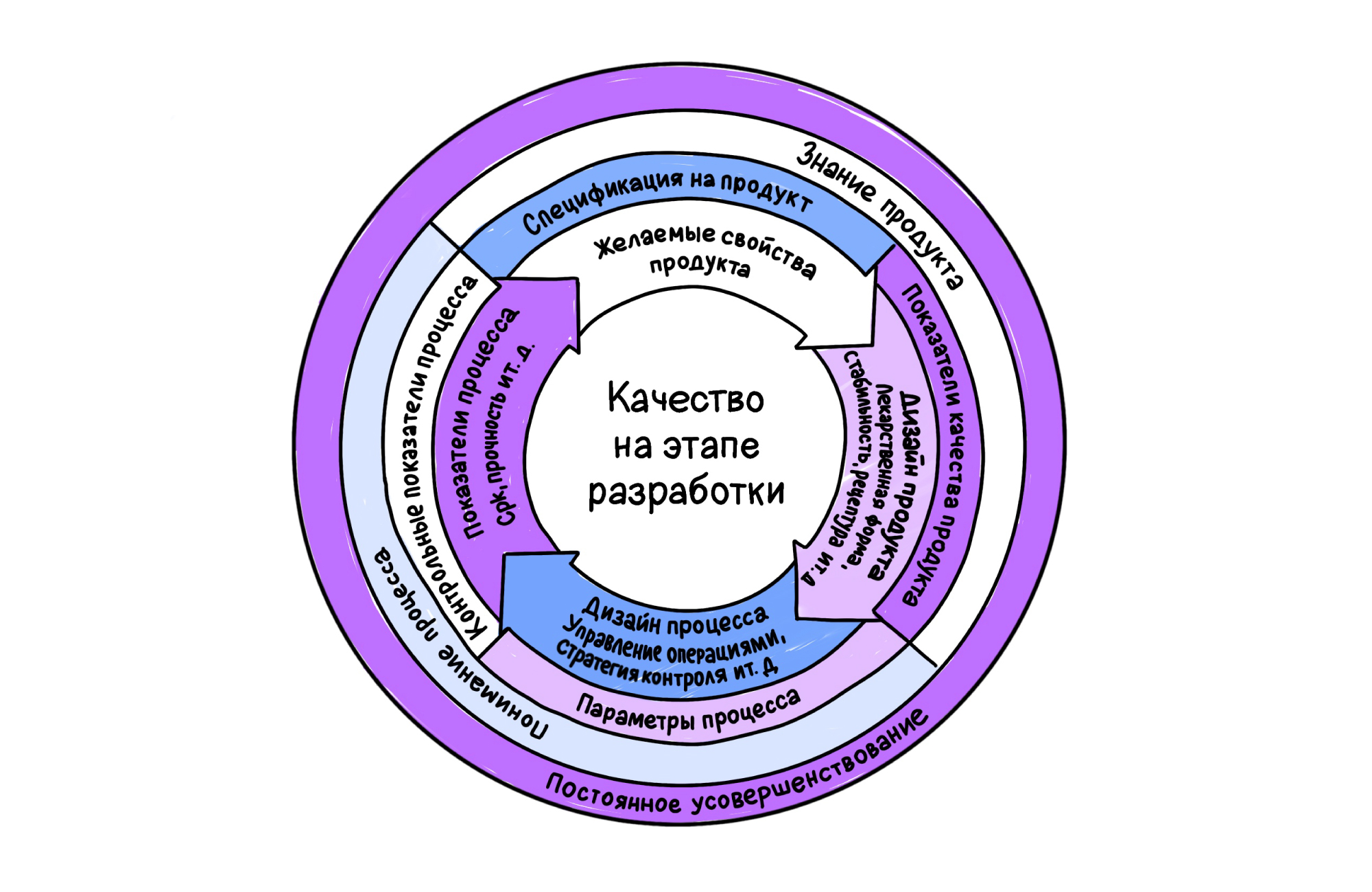
Для обеспечения качества терапевтических препаратов применяют подход Quality by Design, или QbD («качество на этапе разработки»). С помощью этого подхода можно спроектировать качество будущего препарата на самых ранних этапах. Отличительные особенности QbD — детальный «портрет» фармацевтического продукта и всех его характеристик, а также непрерывное и постоянное улучшение его качества по мере получения новых данных в процессе производства
Соответствие качества терапевтического препарата целевому назначению проверяют два направления — контроль качества и обеспечение качества. На первый взгляд эти два процесса кажутся синонимичными, а разница между ними — расплывчатой, но все же они отличаются друг от друга.
«Обеспечение качества отвечает за разработку системы управления и процессов таким образом, чтобы на всех этапах жизни препарата минимизировать или предотвратить риск ошибок, приводящих к снижению качества.
Контроль качества проводит анализ сырья и материалов, которые поступают в производство, потому что из испорченных ингредиентов никогда не получится пригодный к использованию продукт. А также тестирует в лаборатории каждую произведенную серию, чтобы подтвердить соответствие наших продуктов требованиям, которые к ним предъявляются регуляторными органами тех стран, куда наша продукция поставляется», — Елена Арькова, вице-президент BIOCAD по качеству.

Чтобы лучше запомнить разницу между контролем и обеспечением качества, можно провести такую аналогию: направление обеспечения качества — это законодательный орган, который определяет правила всех операций, связанных с разработкой и производством лекарств. А контроль качества — это исполнительный орган: сотрудники этого направления непосредственно измеряют, испытывают и проверяют материалы, условия и процессы в ходе разработки и производства терапевтических препаратов

Из аптечного бизнеса — в биотех: интервью с Мариной Волоцковой
Как я попала в биотех
В фарминдустрии я работаю уже более 15 лет, и десять из них — в BIOCAD. В компанию я пришла из аптечного бизнеса — помню, как меня поразили четкость и отлаженность всех процессов. Первое время я боялась, что могу чего-то не знать или не уметь, но мои коллеги и руководитель помогли влиться в работу. За все время работы в компании я прошла путь от специалиста Отдела обеспечения качества и специалиста по сертификации до инженера по качеству. Но должность, которую я занимаю уже несколько лет — уполномоченное лицо по качеству, — особая.
Чем занимается уполномоченное лицо
Эта должность очень интересная, но и крайне ответственная. Если описывать эту роль простыми словами, то главная цель уполномоченного лица — подтвердить соответствие препарата предъявляемым требованиям и характеристикам, а также гарантировать, что лекарство произведено в соответствии со всеми правилами производства и контроля качества. Уполномоченное лицо по качеству вносит свой вклад в принятие самых важных решений на жизненном пути препарата — возможно ли поставлять это лекарство для дальнейшего использования в целях терапии или нет.
Как строится мой рабочий день
Задачи уполномоченного лица по качеству очень разные, благодаря чему удается рассмотреть терапевтические препараты с нескольких сторон. С одной стороны, ты работаешь в режиме производства: если возникает какой-то вопрос с технической стороны, связанный с производством препарата, вся наша команда ищет для него оптимальное решение. Для этого важно погрузиться в нюансы работы машин, как они функционируют, какие поломки могут возникать в процессе производства и насколько они критичны для всей производственной линии. Каждая такая задача — как мини-расследование со своим заключением. С другой стороны, ты изучаешь досье на выпуск препарата. Досье можно сравнить с некой «книгой жизни» лекарства — от момента возникновения идеи молекулы и смешивания необходимых компонентов до поступления на склад уже готовой упаковки с препаратом.
Каждый препарат — как отдельный человек со своими особенностями и характеристиками, с которыми нужно считаться.
Работая в Направлении «Качество», ты постоянно развиваешься и обогащаешь свой опыт знаниями о новых высокотехнологичных препаратах, изменяешься вместе с трансформацией всей компании. Чтобы просто оставаться на одном месте, то есть хотя бы на том же уровне компетенций, нужно бежать со всех ног — постоянно учиться и знакомиться с международным опытом фармацевтических компаний.
Был такой случай
Однажды уже на этапе заключительной проверки досье выяснилось, что маркировка серии препарата не соответствует требуемой. Из-за этого мог возникнуть риск перепутывания разных серий лекарства у международных партнеров. Благодаря уполномоченным лицам по качеству удалось вовремя обнаружить это несоответствие — мы исправили ошибку и уложились в срок, требуемый для поставки препарата клиентам.

При производстве терапевтических препаратов важно контролировать каждую деталь — даже цвет крышечек на обжимных колпачках. Это позволит не перепутать разные препараты при упаковке. Поэтому фармацевтические компании уделяют большое внимание разработке оригинальных упаковочных материалов для своих продуктов. Например, для колпачка на флаконе препарата Фортека® выбрали цвет «маджента»
А если вспоминать самые интересные проекты, то мне больше всего запомнился запуск контрактного производства на площадке ПК-137. Мы много взаимодействовали с коллегами из АО «Генериум», для которых по контракту производим препарат Ревелиза®, перенимали опыт и интегрировали в свою систему производства их лучшие практики. Такие кейсы — пример пополнения «копилочки» знаний о новых технологиях контроля качества.

Хочу сказать кое-что еще
Работать в сфере качества одновременно и сложно, и безумно интересно. Мне нравится, что можно и понаблюдать за производственными процессами, и заглянуть в чистые помещения в стерильном одноразовом костюме, и самой разобраться в процессах — например, возникают ли нарушения при работе с агарозной средой в чашках Петри.
Думаю, главное достижение BIOCAD в области качества — здоровье наших пациентов и положительные отзывы о препаратах. И как раз для того, чтобы выпускать надежные и безопасные терапевтические препараты, важно поддерживать на должном уровне все производственные процессы и систему качества. Преимущество нашей компании в сфере качества — в собственных лабораториях с высокотехнологичным оборудованием и в квалифицированных сотрудниках, которые проводят испытания.

Карьерный рост внутри компании: интервью с Юлией Молчановой
Как я попала в биотех
С июля 2024 года я выполняю роль уполномоченного лица по качеству в BIOCAD. Этому назначению предшествовали повышение квалификации и государственная аттестация. Рост экспертизы сотрудников внутри компании — важный ключ к обеспечению качества.
Чем занимается уполномоченное лицо по качеству
Уполномоченные лица по качеству несут ответственность за производство и выпуск безопасных и эффективных препаратов. Для этого мы ежедневно сталкиваемся с ситуациями выбора, когда приходится принимать сложные и ответственные решения. Конечно, нельзя быть абсолютным экспертом во всех областях, которые касаются производства терапевтических препаратов. Поэтому уполномоченные лица поддерживают тесные контакты со всеми вовлеченными в процесс сотрудниками, опираясь на их опыт и экспертизу. Нам приходится балансировать между потребностями разных людей и подразделений компании, сталкиваясь с конфликтами интересов. Наверное, это одна из самых сложных задач. Вот почему уполномоченным лицам по качеству важно находить компромиссы и эффективный выход из сложных ситуаций — этот навык мы прокачиваем каждый день.
Каждый сотрудник компании в той или иной степени влияет на качество производимых препаратов.
Как строится мой рабочий день
Моя основная регулярная задача — выпускать серии препаратов для проведения клинических исследований. Каждый день я проверяю досье на серии, анализирую результаты отклонений, этапы внедрения изменений и подписываю разрешения на выпуск. Эта подпись подтверждает, что серия препарата была произведена в соответствии со стандартами GMP.
Главное в моей работе — обеспечить стабильное качество наших лекарств. Для этого мы валидируем все основные процессы на жизненном пути препарата: проверяем работу оборудования, соблюдение стандартных процедур производства, условия упаковки и хранения готовых лекарственных форм. А при внедрении изменений в любой из процессов мы тщательно оцениваем все возможные риски, чтобы вовремя выявить потенциальные «источники опасности», и придумываем план действий для минимизации последствий этих рисков. Например, трансфер нового продукта на производственный участок — это изменение в уже сложившемся процессе. Перед запуском производства нового препарата мы анализируем, как этот процесс повлияет на уже сложившиеся практики на производственной линии. Важна каждая мелочь: в какой форме выпуска будем производить лекарство, есть ли у него какие-то особенности, из-за которых потребуется дополнительно очищать все поверхности на производственной линии, потребуется ли закупать новое оборудование и где оно будет стоять.
Был такой случай
Один из самых запоминающихся проектов, в которых я участвовала, — переход на систему электронных журналов. В работе участвовала кросс-функциональная команда из ИТ-специалистов, аналитиков, технологов, специалистов по контролю и обеспечению качества. Помню, как мы сталкивались с нестандартными ситуациями — например, одно и то же оборудование могло называться по-разному, и нам приходилось искать способы сделать названия единообразными. Но именно благодаря этому кейсу удалось подсветить узкие места в подходах к стандартизации.
Хочу сказать кое-что еще
BIOCAD строит социально ориентированный бизнес — мы работаем для улучшения качества жизни людей, поставляя качественные, доступные и надежные препараты. Поэтому так важен системный подход к качеству нашей продукции. И в этом помогает эффективная и синергетическая работа всех систем качества: управление отклонениями, управление рисками, управление знаниями.
Стать частью команды BIOCAD
Хочешь присоединиться к команде qualified persons? Смотри все наши крутые вакансии на карьерном сайте 🤘


