
Дайджест #10. Мал, да удал — как наночастицы помогают в иммунотерапии рака. Аутоиммунные реакции на «хорошие» и «плохие» Т-хелперы
Наночастицы уже давно у всех на слуху, но их использование в практической медицине пока что ограничено. Недавно удалось разработать новый способ терапии с помощью наночастиц, который потенциально можно будет использовать в лечении немелкоклеточного рака легкого. Сама по себе наночастица выполняет роль своеобразной упаковки, которую «прокачивают»: вооружают ее поверхность антителами, а внутрь помещают лекарственную молекулу. Подробнее — читайте в новом дайджесте.
Онкология
Как улучшить иммунотерапию при НМРЛ с помощью наночастиц
В 2016 году прорывом в лечении немелкоклеточного рака легкого (НМРЛ) стала терапия с помощью иммунных чекпоинтов, в частности с помощью пембролизумаба — ингибитора рецептора PD-1. Однако у этого способа лечения есть свои недостатки, в числе которых — низкий отклик у определенных групп пациентов. Чтобы обойти возможные ограничения, биологи из США предложили новый способ нанотерапии с помощью антител, который сочетает в себе иммунотерапию и молекулярную таргетную терапию — ADN (antibody-conjugated drug-loaded nanotherapeutics). Для этого разработали антитела против CD47 и PD-L1, которые разместили на поверхности наночастицы, а также использовали ингибитор PI3K/AKT/mTOR — его поместили внутрь наночастицы. Введение этой модифицированной наночастицы мышам с агрессивным типом НМРЛ продемонстрировало более высокую противоопухолевую эффективность, чем уже принятые варианты лечения с помощью ингибитора PD-L1. — Antibody nanoparticle conjugate-based targeted immunotherapy for non-small cell lung cancer.
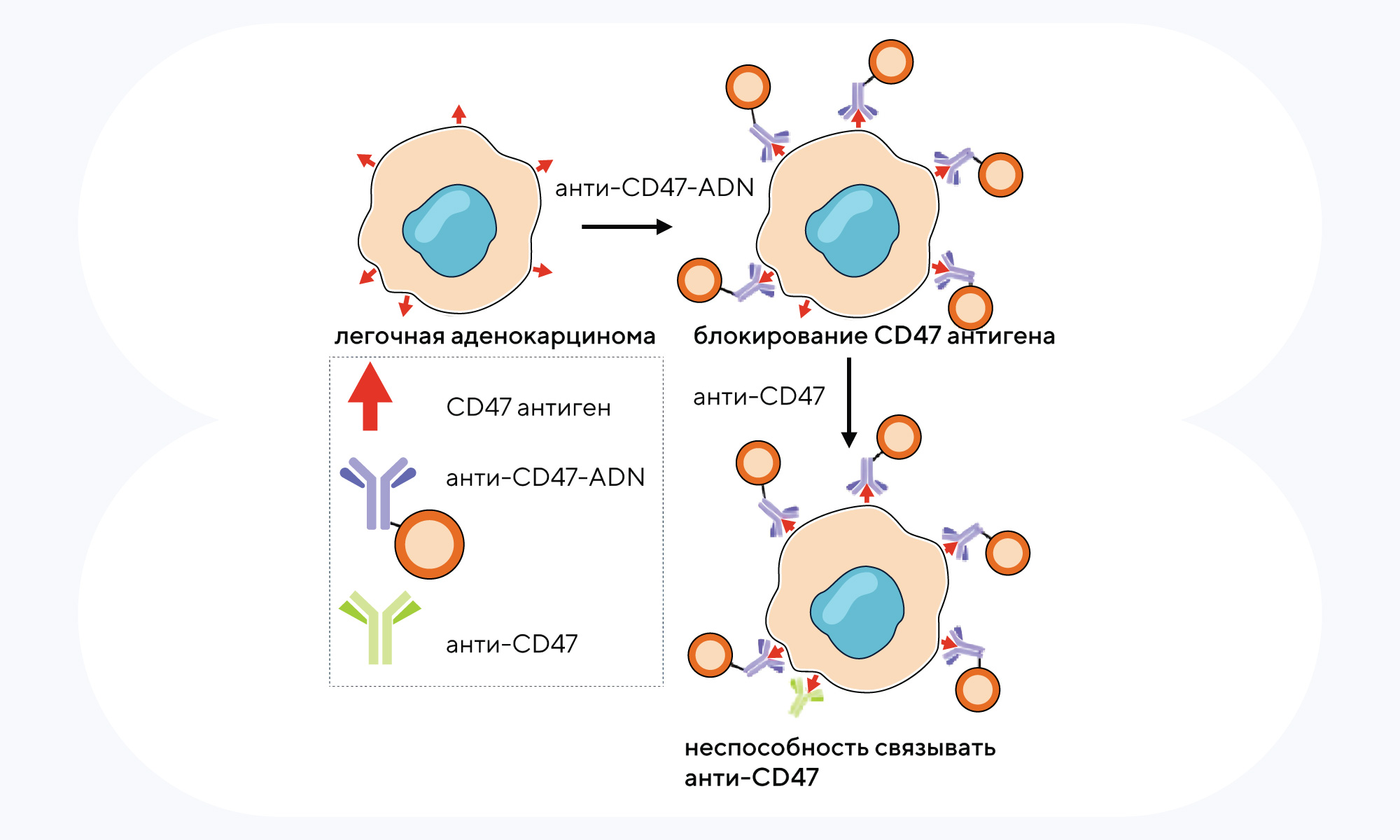
Схема эксперимента: как проверяли блокирование иммунных контрольных точек анти-CD47-PDL1-ADN в легочных клетках при НМРЛ. Источник: адаптировано из Science Advances
Обнаружены новые маркеры инфекционных осложнений при миелолейкозе
Один из серьезных факторов риска, который сопровождает пациентов с острым миелобластным лейкозом, — возникновение инфекций. Они могут приводить к осложнениям, например к сепсису или грибковым заболеваниям. Ранее предполагалось, что на восприимчивость к инфекциям влияет наличие в организме конкретных однонуклеотидных полиморфизмов — снипов (SNPs, single nucleotide polymorphisms). Чтобы подтвердить это предположение, биологи из Германии проверили вклад 11 снипов на шести генах у пациентов с острым миелобластным лейкозом. Выяснилось, что наличие множественных снипов в ДНК людей непосредственно связаны с риском развития инфекции. Например, снип DC-SIGN rs4804800 влияет на развитие сепсиса, а снипы в генах PTX3 и Dectin-1 определяют возникновение грибковой инфекции. Это исследование, а также дальнейшее изучение генетической предрасположенности пациентов к инфекционным осложнениям потенциально могут повлиять на сценарий антимикробной профилактики у людей с острым миелобластным лейкозом. — Validating genetic variants in innate immunity linked to infectious events in acute myeloid leukemia post-induction chemotherapy.
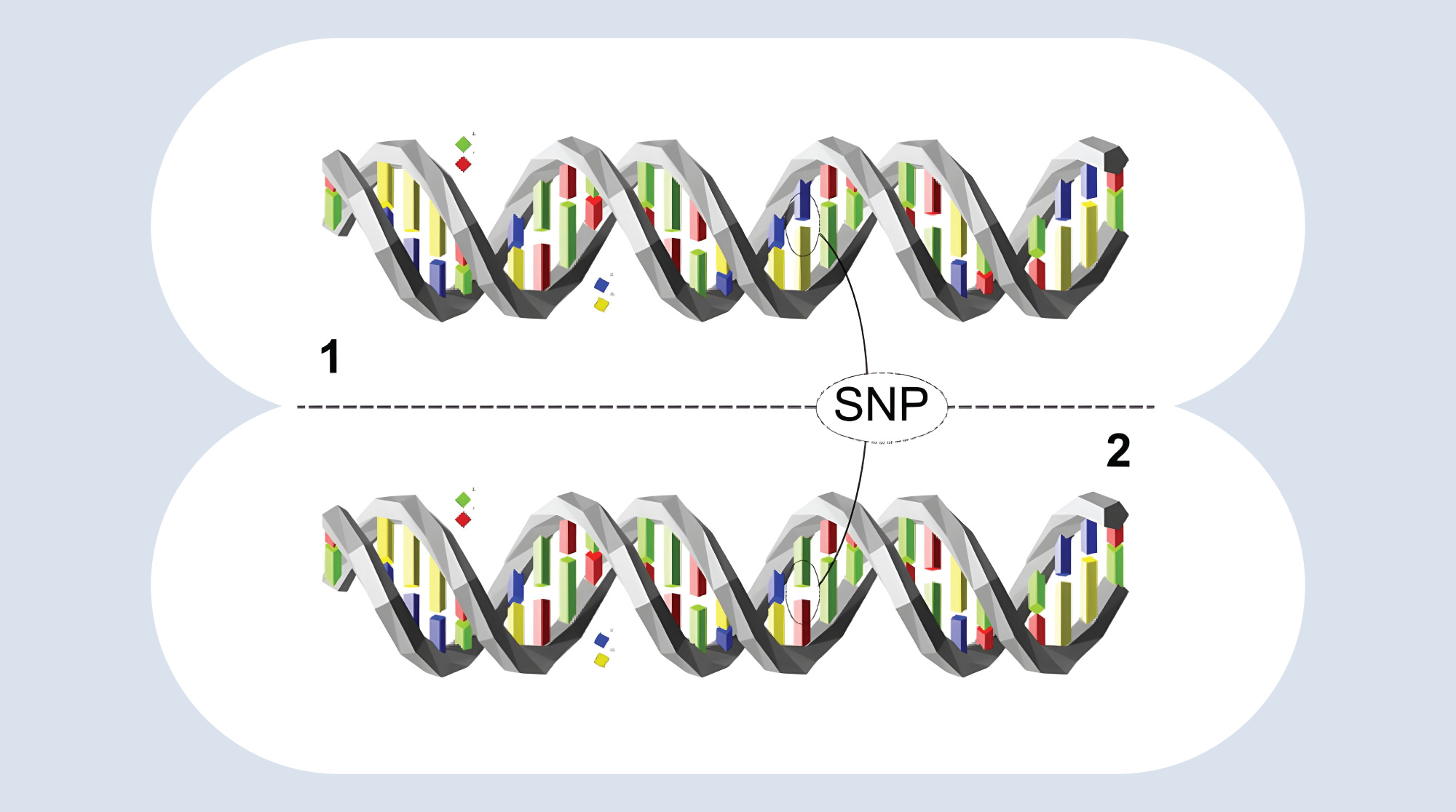
Снипы возникают, когда структура молекулы ДНК (2) отличается от исходной (1) на один нуклеотид. Источник: Wikimedia
Обнаружен новый активатор ферроптоза при раке
Устойчивость к терапии и склонность к метастазированию у раковых клеток часто наблюдаются при запуске программы эпителиально-мезенхимального перехода (ЭМП). В норме этот сценарий включается в процессе развития эмбриона и при заживлении ран на поверхности эпителия. Но иногда происходит сбой, и смена эпителия на мезенхиму провоцирует прогрессирование опухолей и воспалительных процессов. Это происходит из-за того, что мезенхимальный фенотип предрасполагает к ферроптозу — особому типу гибели клеток, при котором липиды окисляются при участии железа. Восприимчивость к ферроптозу увеличивает ряд факторов активации эпителиально-мезенхимального перехода. В новом исследовании удалось идентифицировать одного из таких участников — транскрипционный фактор Zeb1. Под его влиянием увеличивается соотношение фосфолипидов, содержащих проферроптотические полиненасыщенные жирные кислоты, что в результате приводит к ферроптозу. Если же ингибировать конкретные ферменты, ответственные за синтез жирных кислот, можно снизить склонность онкоклеток с Zeb1 к ферроптозу. Эти результаты открывают новые перспективы для терапии агрессивных типов рака, склонных к метастазированию. — Zeb1 mediates EMT/plasticity-associated ferroptosis sensitivity in cancer cells by regulating lipogenic enzyme expression and phospholipid composition.
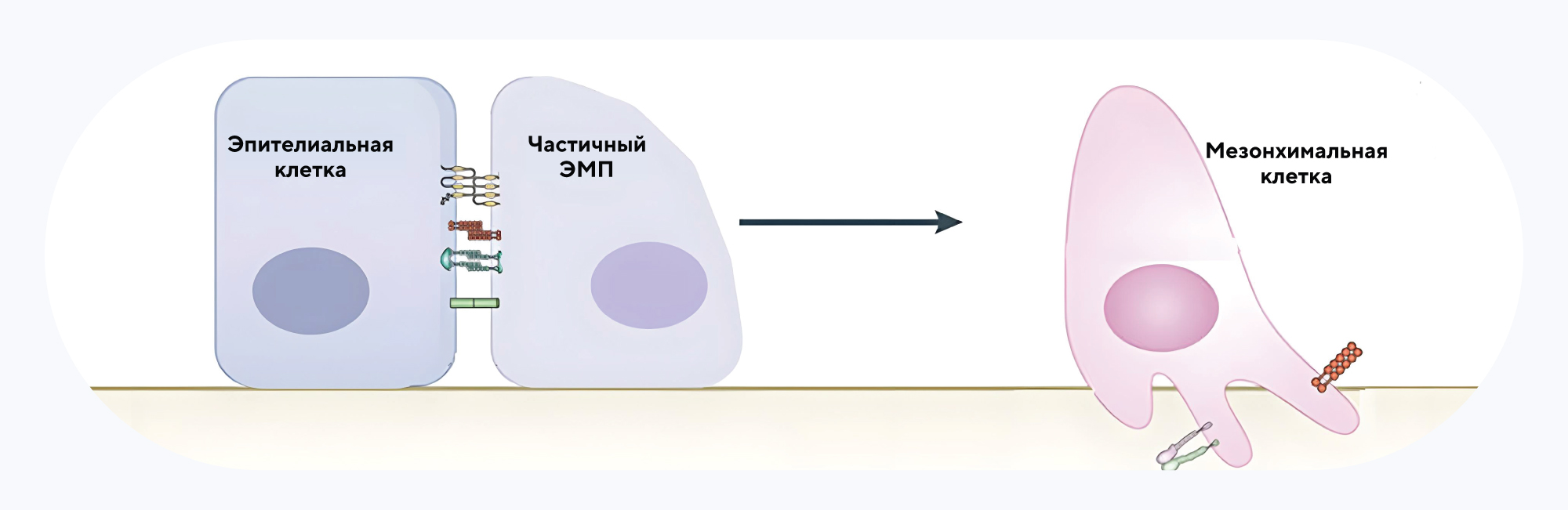
Источник: Molecular mechanisms of epithelial-mesenchymal transition
На первом этапе эпителиально-мезенхимального перехода (слева) разрушаются межклеточные контакты, которые плотно удерживали эпителиальные клетки между собой, а также изменяется клеточная полярность. На втором этапе (справа) клетки формируют ламеллоподии и филоподии и приобретают способность к подвижности.
Аутоиммунные заболевания
Соотношение «хороших» и «плохих» Т-хелперов влияет на аутоиммунные реакции
Интерлейкин 17 — провоспалительный цитокин, который секретируют Т-хелперные клетки. Однако популяции этих клеток различаются: часть Т-хелперов (TH17) обеспечивает гомеостаз тканей, а другая часть — это патогенные клетки, которые опосредуют воспаление тканей. В новой работе изучили гетерогенность Т-хелперов TH17 и обнаружили значительные различия в хроматиновом ландшафте обычных и патогенных клеток. Так, непатогенные клетки содержат те же конфигурации хроматина, что и остальные регуляторные Т-клетки, а TH17, вызывающие воспаление, помимо обычных конфигураций, включают в себя черты Т-хелперов 1-го типа (Th1). Соотношение патогенных и непатогенных TH17 контролируется различными сигнальными путями и факторами транскрипции. Один из важных участников этого процесса — фактор BACH2: он поддерживает программу иммунной модуляции и сдерживает провоспалительную программу, в которой участвуют патогенные Т-хелперы. Исследователи предполагают, что BACH2 может также играть противовоспалительную роль при рассеянном склерозе, смягчая аутоиммунные реакции в организме. — BACH2 regulates diversification of regulatory and proinflammatory chromatin states in TH17 cells.
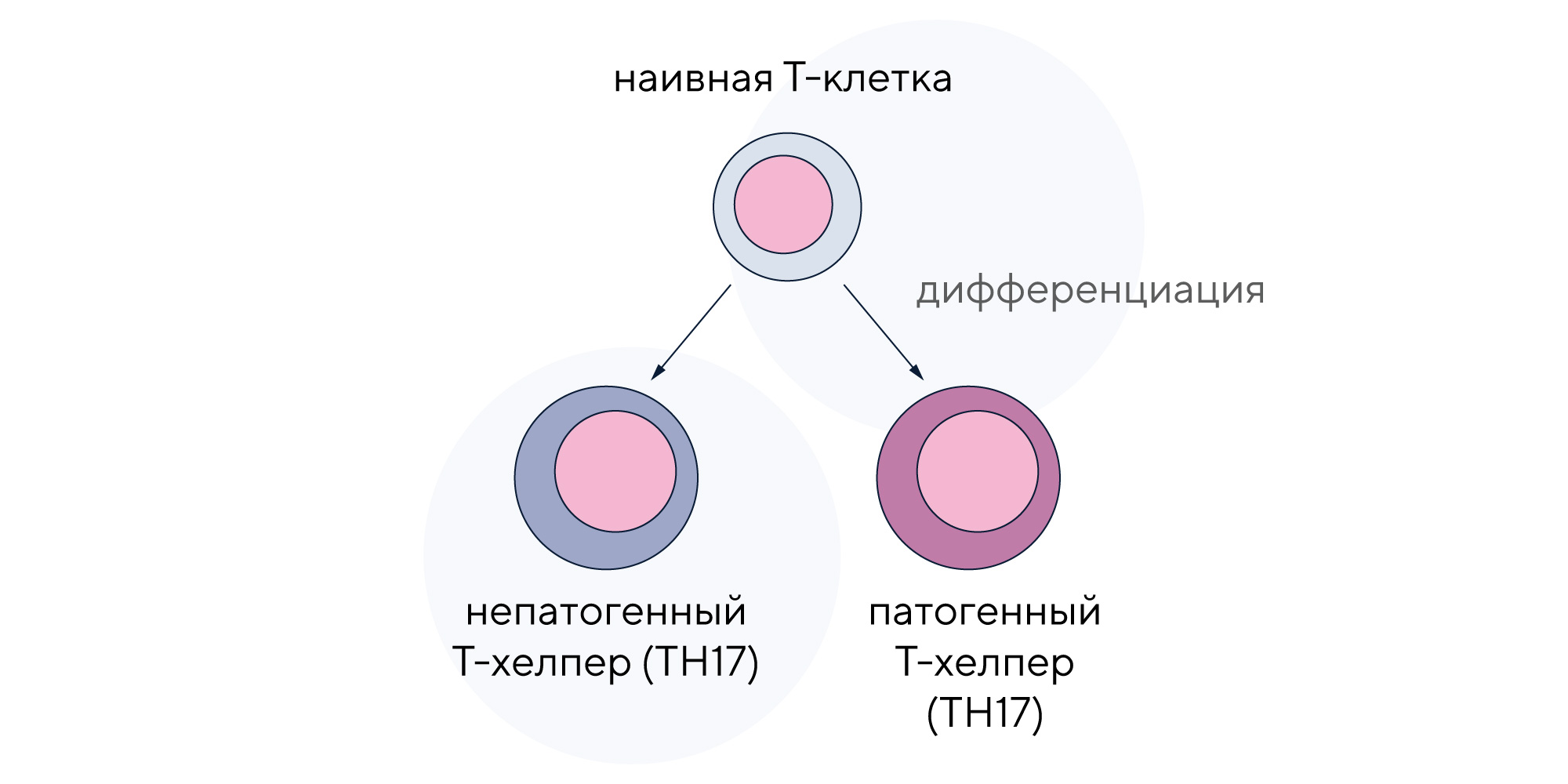
В процессе дифференциации Т-клеток, связанных с интерлейкином 17, возможно образование непатогенных или патогенных Т-хелперов TH17. Регуляторный белок BACH2 способствует сдерживанию воспалительных программ при участии патогенных ТH17.
Влияние оксида азота на патогенез псориаза
Оксид азота (NO) — свободный радикал, который участвует в передаче сигналов, а также обеспечивает антимикробную и противоопухолевую защиту. Концентрация оксида азота в организме может по-разному влиять на течение различных заболеваний. Чтобы лучше разобраться в этом вопросе, шведские ученые решили изучить влияние гена индуцируемой синтазы оксида азота NOX2 на течение псориаза — болезни, связанной с воспалением кожи. В ходе исследования на мышиной модели псориаза удалось продемонстрировать, что течение псориаза можно облегчить за счет полного устранения или повышения уровня NO в клетках. — NOS2-derived low levels of NO drive psoriasis pathogenesis.
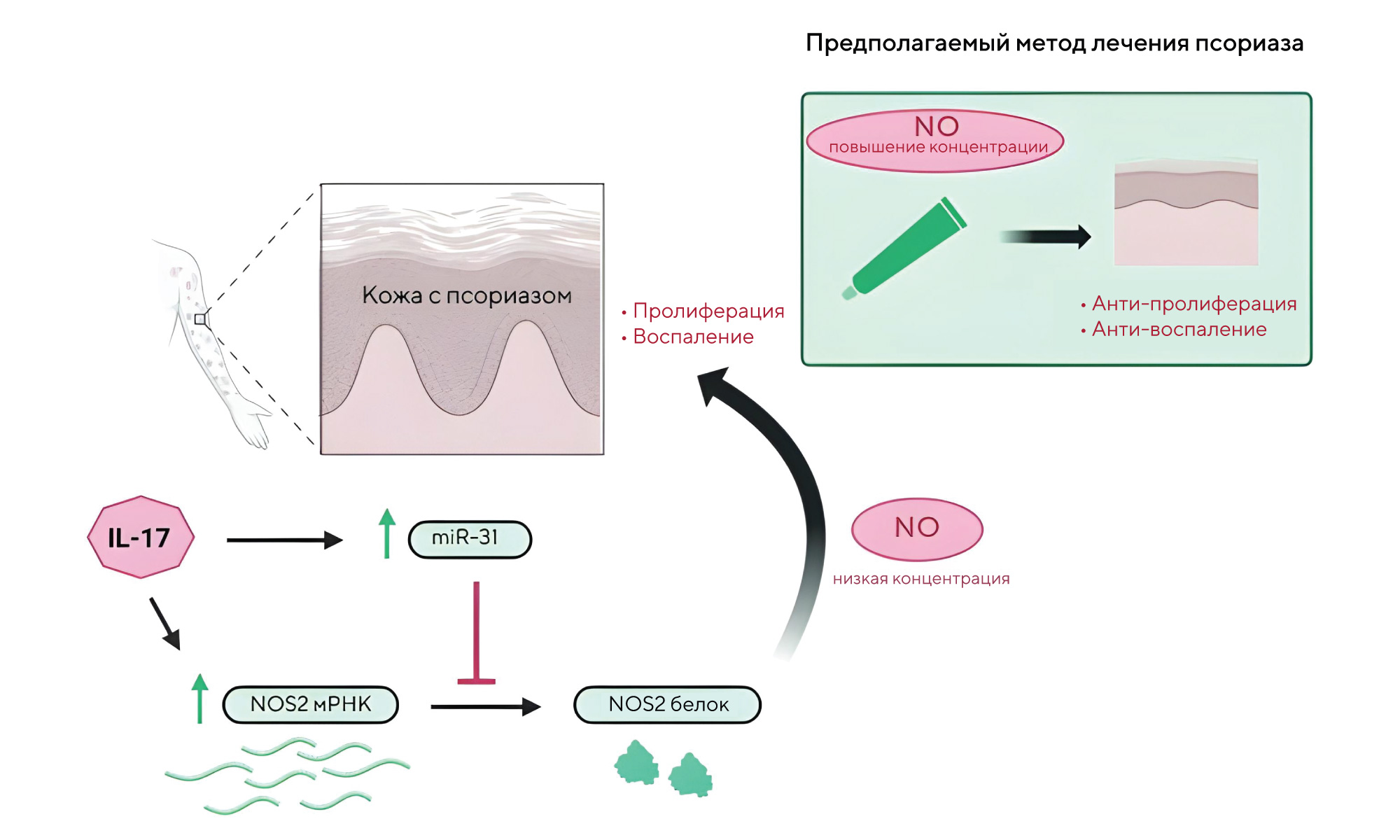
Источник: Cell Death & Disease
В эпидермисе пациентов с псориазом наблюдается сильная экспрессия мРНК NOS2, опосредующая синтез фермента индуцируемой синтазы оксида азота. Однако полная трансляция этого белка предотвращается из-за IL-17-индуцированной miR-31, что приводит к незначительному повышению уровня NO в псориатическом эпидермисе. Получается, небольшие концентрации оксида азота косвенно влияют на тяжесть течения псориаза. Предлагаемая схема лечения этого заболевания заключается либо в полном устранении, либо в повышении уровня NO в организме.