
Дайджест #2. Путешествие плазматической клетки. Иммуноинженерия в аутоиммунном
Один из героев нового дайджеста — долгоживущая плазматическая клетка. Недавнее исследование заставило пересмотреть уже ставшие привычными взгляды на этот тип клеток: оказывается, они любят путешествовать по всему организму и могут возникать в процессе формирования гуморального ответа. Более подробное досье на них, а также на другие виды клеток читайте в новом дайджесте.
Ревматология
Зачем используют классификацию «генетически переходных» заболеваний
В случае когда мы говорим о наследственных заболеваниях, применяют концепцию генетически переходного заболевания, когда мутация гена возникает, но одной ее недостаточно для полноценного развития болезни. В новой работе, опубликованной в Nature Reviews Rheumatology, эту же концепцию применили к ревматическим заболеваниям, которые не проявляются только из-за одного фактора, а чаще связаны с сотнями генетических вариантов.
Эти варианты находятся в переходной «серой зоне» между моногенными генетическими вариантами, обладающими значимым эффектом, и аллелями общей восприимчивости, которые по отдельности вызывают незначительные эффекты. Многие варианты генов, ассоциированных с редкими аутовоспалительными заболеваниями, которые встречаются с низкой частотой и слабо проявляются, повышают восприимчивость организма к системному воспалению. Так, при аутоиммунных заболеваниях сотни генетических вариантов HLA (Human leukocyte antigen) и не-HLA относятся к аллелям умеренного риска, соответственно, заболевания, связанные с этими вариантами, можно назвать генетически переходными. Если начинать разбираться в связях между факторами и болезнями, которые они вызывают, можно отследить тот же принцип. Делать это стоит хотя бы потому, что приложение концепции генетически переходных заболеваний к терапии потенциально может улучшить данные генетических тестирований и диагностику, а также помочь с выбором способа лечения. — Genetically transitional disease: conceptual understanding and applicability to rheumatic disease.
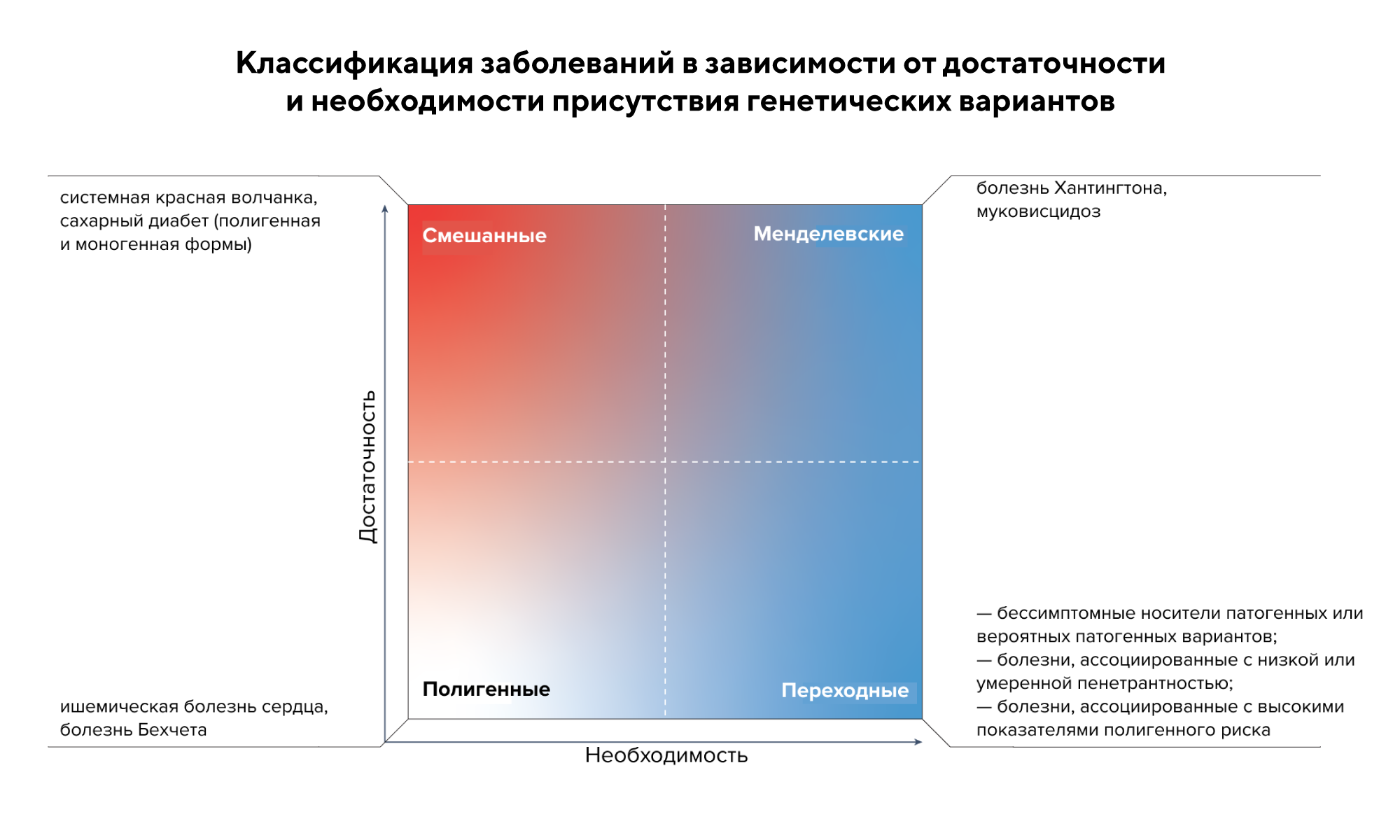
Источник: адаптировано из Nature Reviews Rheumatology
Потенциал иммуноинженерии для лечения системных аутоиммунных заболеваний
Новая область терапии системных аутоиммунных заболеваний — иммуноинженерия, при которой модуляцию иммунной системы проводят, используя новые химически модифицированные материалы. Благодаря своим физико-химическим свойствам, такие материалы способны более таргетно нацеливаться на конкретные ткани и органы, где необходимо вмешательство, проникать внутрь лимфоидной ткани и доставлять иммунорегуляторы, важные для терапии заболевания. Применение иммуноинженерных методов позволит развивать персонализированную медицину для индивидуального лечения конкретных пациентов, например, воздействовать на иммунофенотипическую регуляцию клеток, связанных с заболеванием, и влиять на микроокружение пораженной ткани. — The therapeutic potential of immunoengineering for systemic autoimmunity.
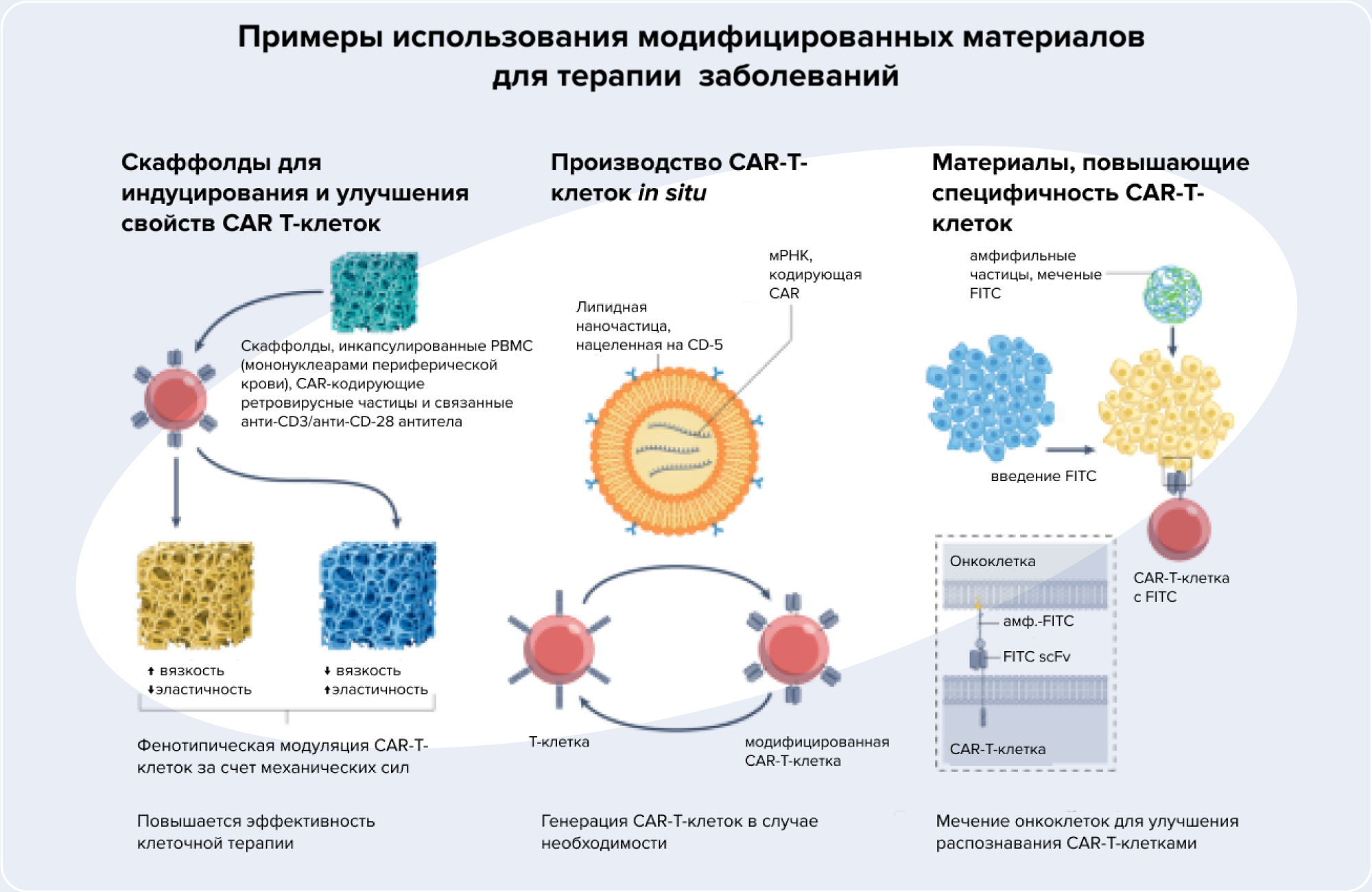
Источник: адаптировано из Nature Reviews Rheumatology
Новые подходы к лечению несистемного ювенильного идиопатического артрита
За последние двадцать лет лечение ювенильного идиопатического артрита заметно изменилось, в частности, за счет большей доступности новых терапевтических молекул и более раннего достижения ремиссии. Но сложность терапии заключается в том, что ювенильный идиопатический артрит — это целая группа заболеваний, каждое из которых требует своего подхода к лечению. Еще одна особенность — то, что в терапии все еще широко используются препараты старого поколения, такие как метотрексат, сульфасалазин и внутрисуставные инъекции глюкокортикоидов. Но в последние пять лет клиническое сообщество получает свежую информацию о результатах нескольких рандомизированных контролируемых исследований новейших биологических и синтетических препаратов. Уже полученные данные и опубликованные терапевтические руководства поспособствовали разработке рекомендаций по стратегии лечения ювенильного идиопатического артрита и достижению устойчивой ремиссии. В новом обзоре обсуждают уже изученные терапевтические подходы к лечению несистемных фенотипов ювенильного артрита, включая олигоартрит, полиартрит и псориатический артрит. — Treatment of non-systemic juvenile idiopathic arthritis.
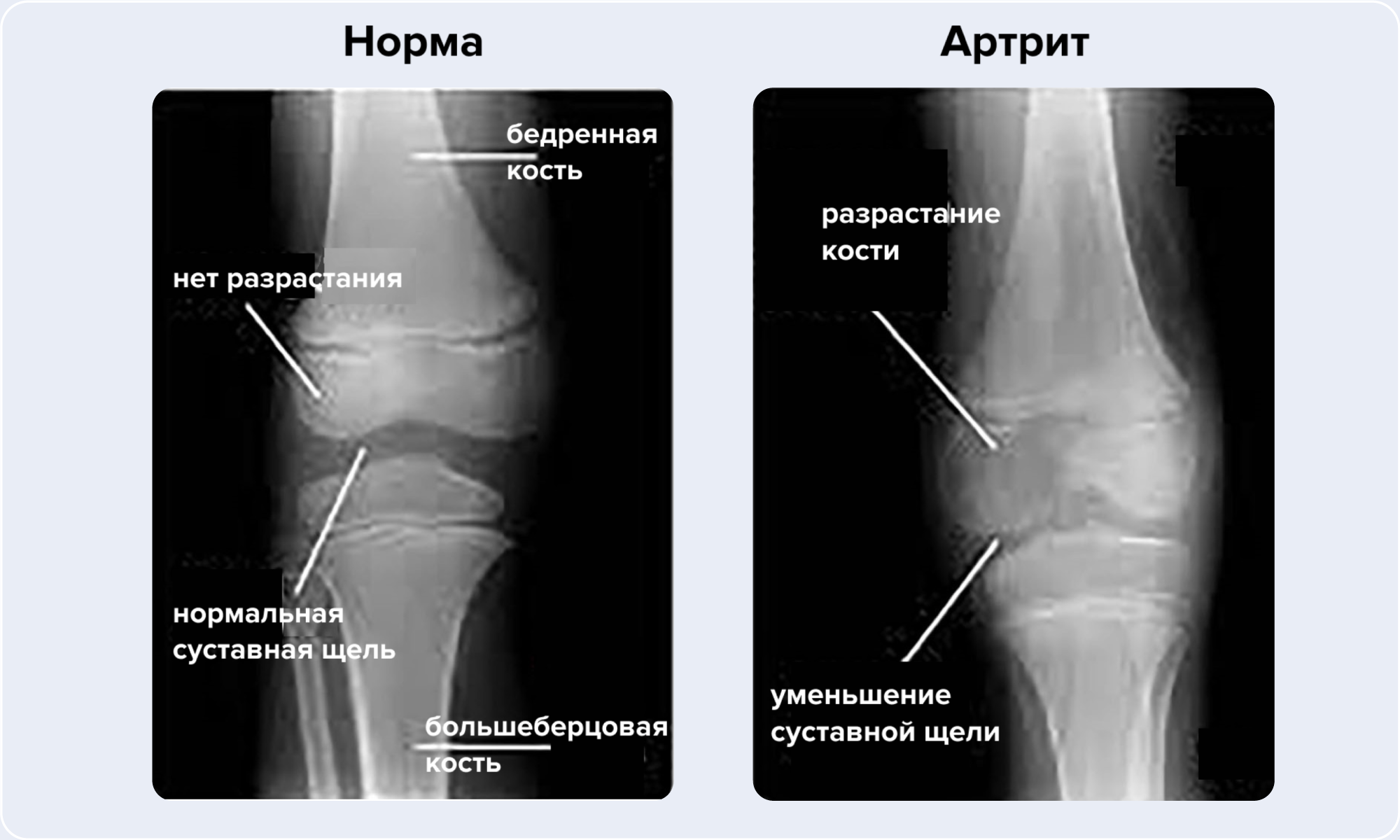
Источник: адаптировано из Indian Journal of Muscoskeletal Radiology
Иммунология
Пути регуляции Тreg-клеток и их роль в развитии аутоиммунных заболеваний
Клеточная линия регуляторных клеток FOXP3+ играет центральную роль в регуляции иммунных ответов. В частности, транскрипционный фактор FOXP3+ участвует в поддержании линии Treg-клеток, однако одного этого фактора недостаточно — более точной настройкой функций регуляторных Т-клеток управляют и другие факторы. Например, в недавнем исследовании было показано, что дисфункция регуляторных Т-клеток может происходить независимо от фактора FOXP3+. Получается, что в развитии Treg-клеток участвуют многоуровневые механизмы, которые включают FOXP3+-зависимые и независимые пути. В обзоре обсуждают многообразие путей, влияющих на функции Т-клеток, и их взаимодействие между собой в приложении к развитию ряда заболеваний — рассеянного склероза, воспалительных заболеваний кишечника, системной красной волчанки и ревматоидного артрита. — The regulation and differentiation of regulatory T cells and their dysfunction in autoimmune diseases.
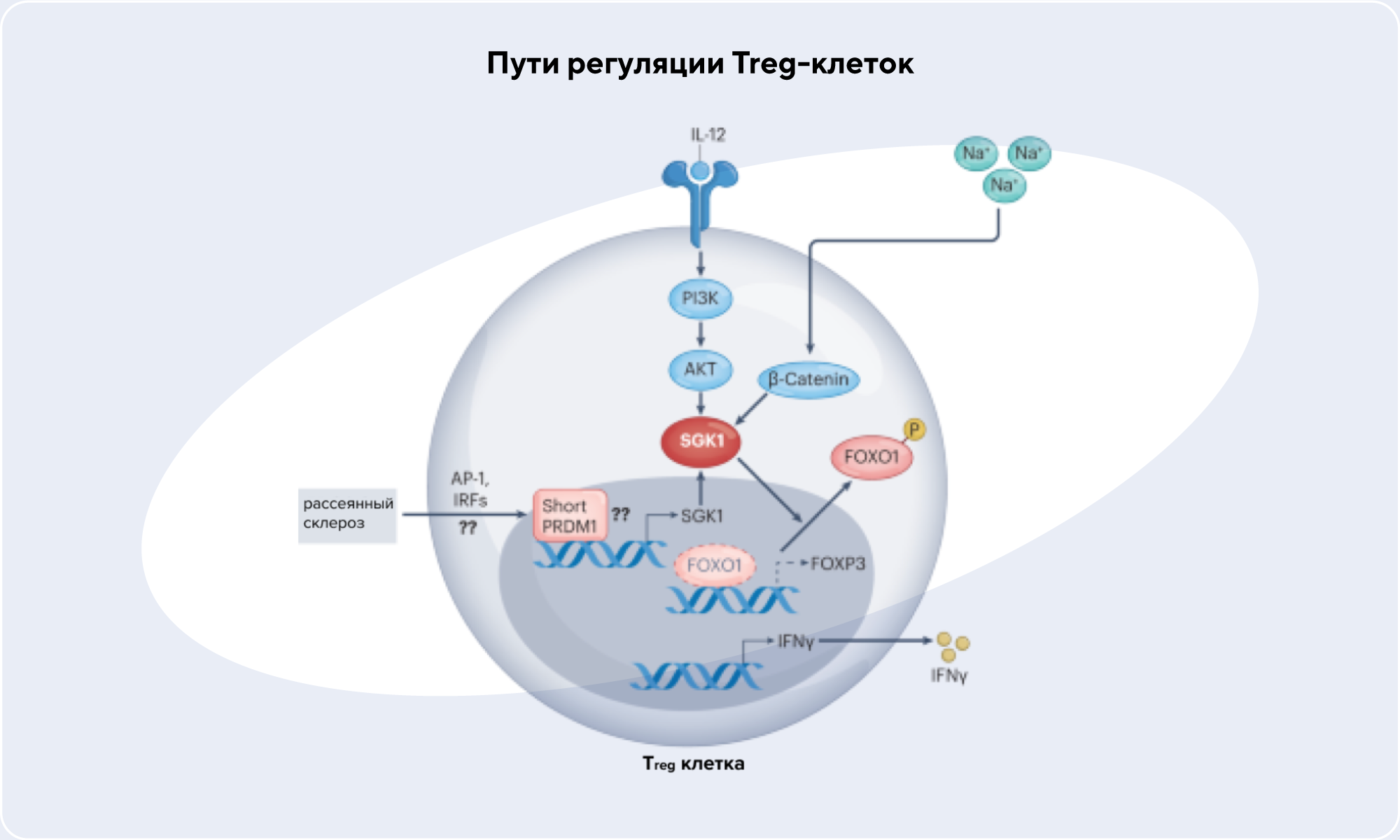
Источник: адаптировано из Nature Reviews Immunology
Иммунотерапия сахарного диабета 1-го типа
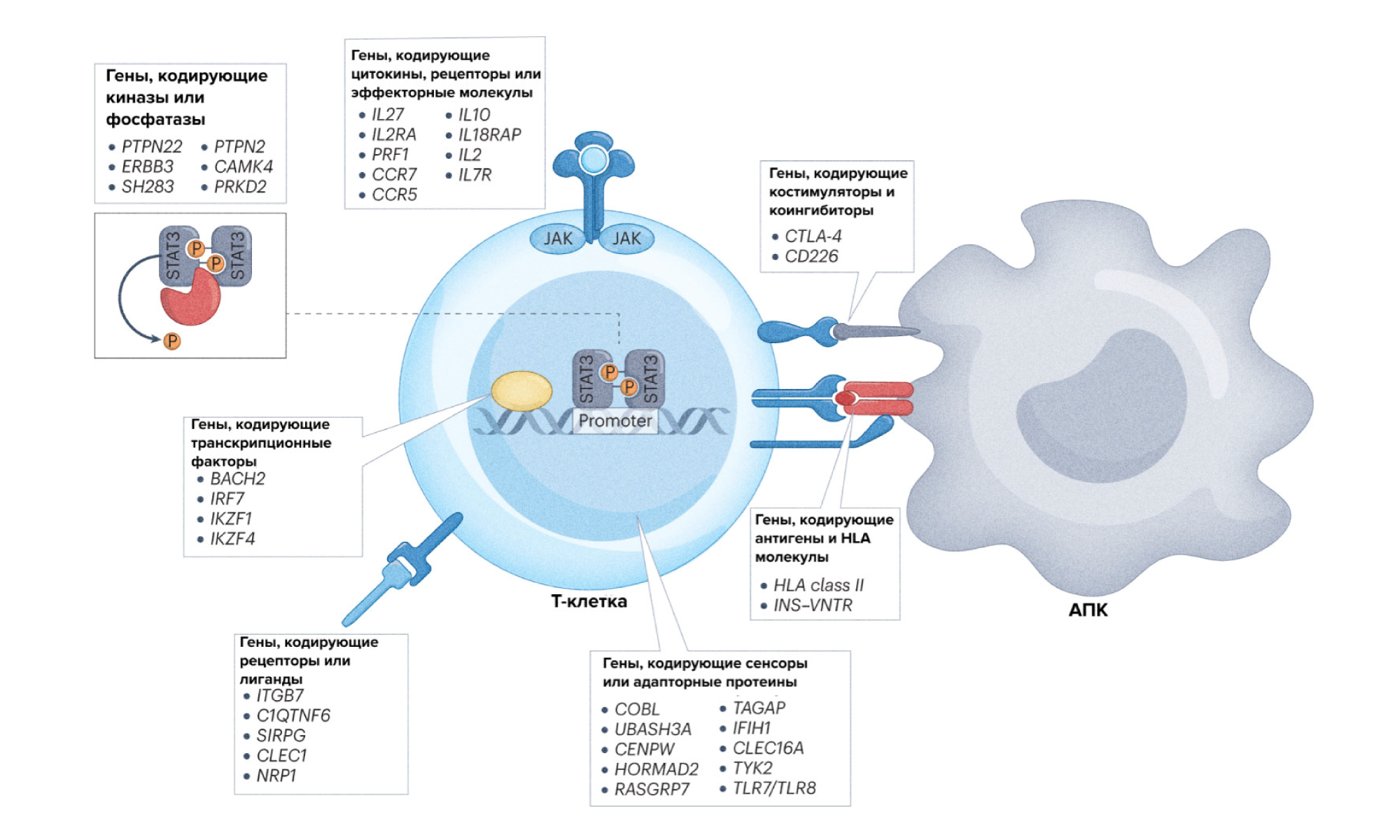
Лечение сахарного диабета 1-го типа стало возможным почти сто лет назад, с момента открытия инсулина. До недавнего момента терапия ограничивалась консервативными методами: мониторингом уровня глюкозы в крови и при необходимости введением инсулина. Однако врачи и ученые продолжают искать другие, более совершенные способы терапии сахарного диабета, в частности — методами иммунотерапии. В новом обзоре детально разбирают различные иммунные механизмы и гены, связанные с развитием сахарного диабета 1-го типа, с акцентом на Т-клетки. — The immunology of type 1 diabetes.
Источник: адаптировано из Nature Reviews Immunology
Обнаружены новые активаторы иммунных клеток для иммунотерапии рака
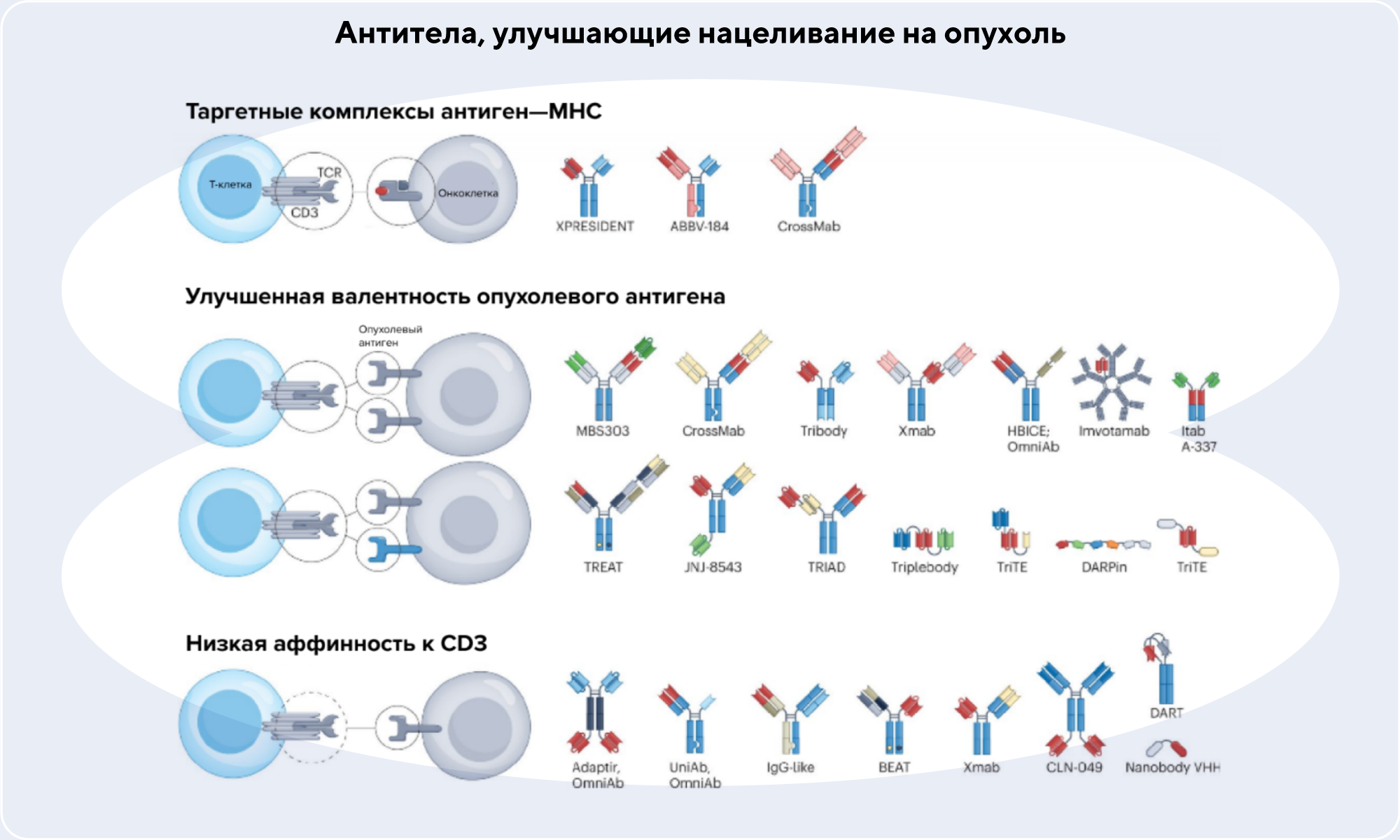
За последние годы в медицине были достигнуты значительные успехи в иммунотерапии рака. В том числе они связаны с перспективными разработками ингибиторов Т-клеток для лечения гематологических злокачественных опухолей. Однако существуют и проблемы в разработке таких препаратов, включая эффективность для большинства пациентов (особенно в случае, когда речь идет о солидных опухолях), подбор оптимальных доз и резистентность к лечению. Чтобы по возможности решить эти проблемы, было разработано новое поколение молекул, нацеленных на Т-клетки. Потенциально эти молекулы более эффективны и безопасны, чем уже существующие, и могут использоваться для лечения разных видов рака. — New immune cell engagers for cancer immunotherapy.
Источник: адаптировано из Nature Reviews Immunology
Чем живут долгоживущие плазматические клетки
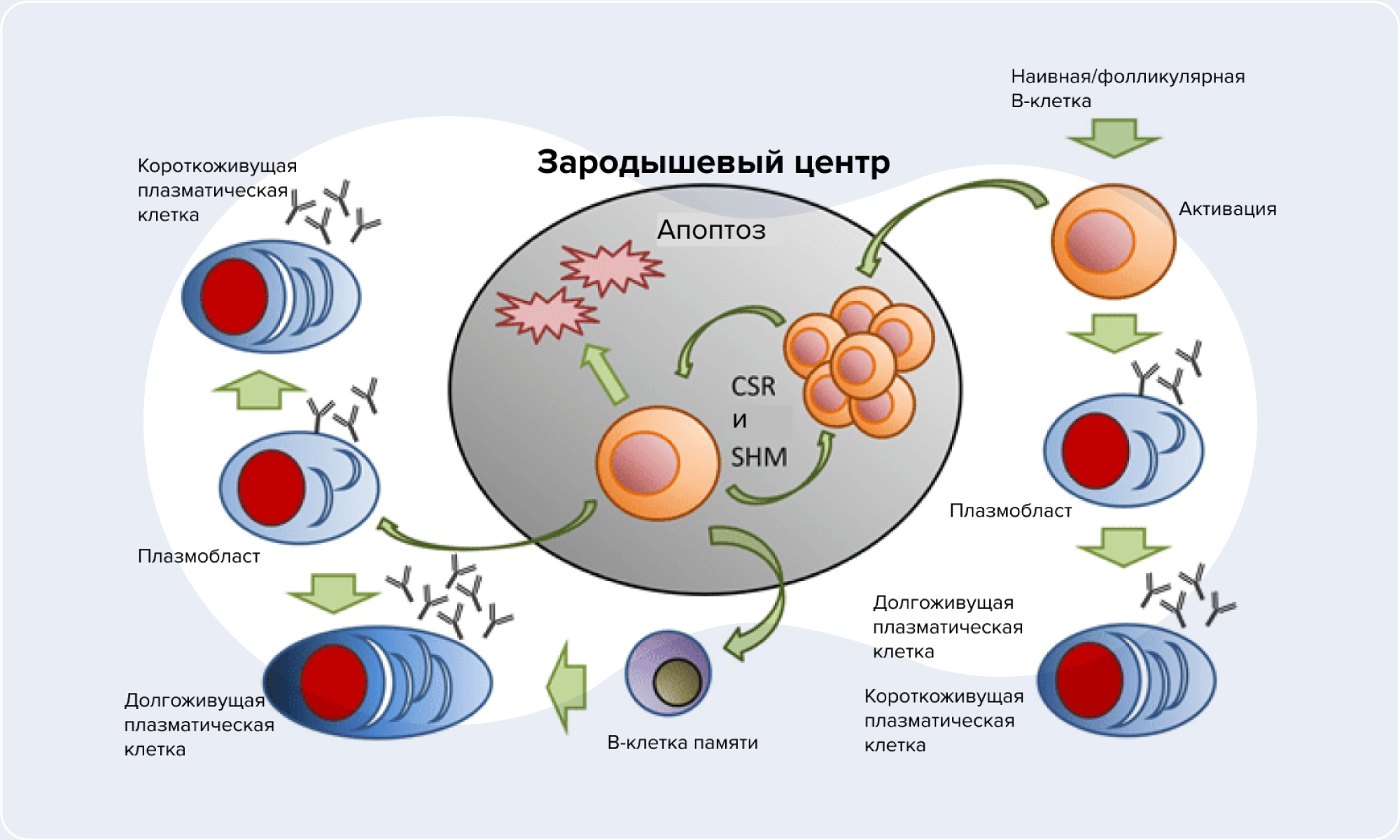
Плазматические клетки занимают особое место в иммунной системе благодаря своей способности производить большое количество разнообразных антител, защищающих от инфекций. Большинство плазматических клеток живут недолго, однако под влиянием определенных условий в организме могут появляться особые долгоживущие плазматические клетки, которые обеспечивают очень длительную, если не пожизненную, защиту организма от воздействия патогенов. Недавние исследования проливают свет на онтогенез, разнообразие, созревание и выживание этих уникальных клеток. Так, раньше считалось, что долгоживущие плазматические клетки возникают преимущественно из зародышевых центров, однако выяснилось, что они могут появляться на самых разных стадиях гуморального ответа. Более того, выяснилось, что плазматические клетки мышей и человека гетерогенны и могут подвергаться дальнейшему созреванию in situ в костном мозге. Еще один удивительный факт: раньше считалось, что плазматические клетки ведут исключительно сидячий образ жизни, однако это не так — потенциально они могут мигрировать и объединяться в кластеры. Все эти результаты, опубликованные в новом обзоре, дают новое представление о внутренних программах развития плазматических клеток и внешних факторах, которые способны регулировать их продолжительность жизни. — New insights into the ontogeny, diversity, maturation and survival of long-lived plasma cells.
Источник: адаптировано из The Longevity of the Humoral Immune Response: Survival of Long-lived Plasma Cells
Онкология
Перспективы адоптивной клеточной терапии для пациентов с меланомой
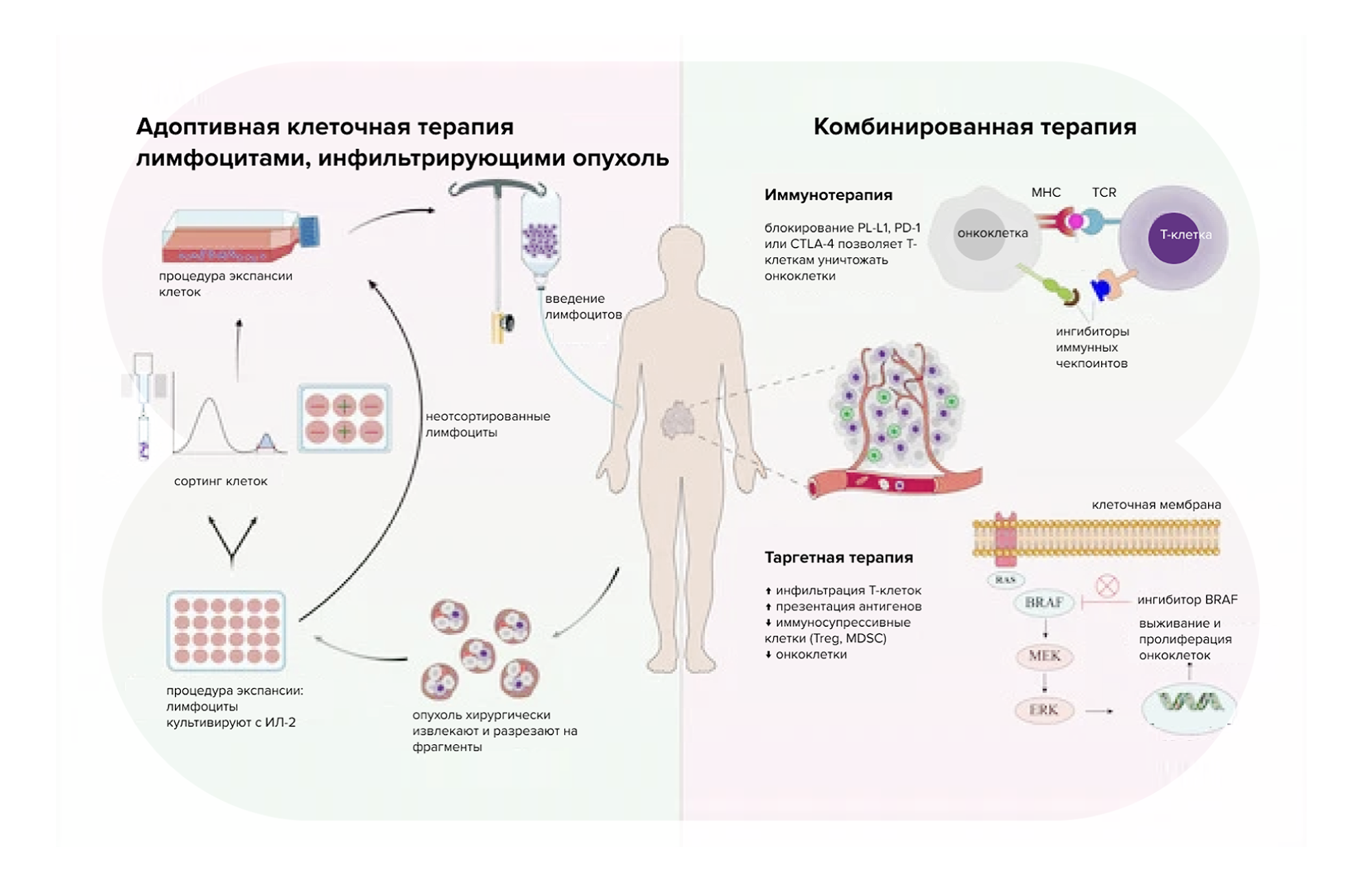
В последние десять лет были достигнуты значительные успехи в лечении пациентов с меланомой благодаря методам иммунотерапии ингибиторами иммунных чекпоинтов и таргетной терапии ингибиторами BRAF и MEK. Однако результаты пятилетней выживаемости пациентов с меланомой, выявленной на поздней стадии, все еще остаются достаточно низкими — не более 50%. Это подталкивает ученых искать новые терапевтические стратегии. Одна из них — адоптивная клеточная терапия лимфоцитами, инфильтрирующими опухоль. Этот метод за последние несколько лет продемонстрировал долгосрочную выживаемость в клинических исследованиях II–III фазы с участием пациентов с меланомой, включая тех, у кого болезнь прогрессировала на фоне предшествующей иммунотерапии ингибиторами иммунных чекпоинтов и ингибиторами BRAF и MEK. В новом обзоре суммированы результаты адоптивной клеточной терапии лимфоцитами для пациентов с поздней стадией меланомы, а также перспективы этого многообещающего лечения. — Tumour-infiltrating lymphocyte therapy for patients with advanced-stage melanoma.
Источник: адаптировано из Cancers
Терапия рака с использованием новых FGFR-ингибиторов
Через рецепторы FGFR1-4 передаются сигналы фактора роста фибробластов (fibroblast growth factor, FGF), что опосредует ряд важных функций: влияние на развитие плода, регуляцию гомеостаза тканей и органов и даже потенциальное развитие онкогенеза. Последнее свойство подтолкнуло ученых к разработке различных молекул для воздействия на эту мишень — так, были созданы ингибиторы pan-FGFR (эрдафитиниб и футибатиниб), ингибиторы FGFR1/2/3 (инфигратиниб и пемигатиниб) и другие препараты, некоторые из которых вошли в клиническое применение. Например, эрдафитиниб одобрен для пациентов с уротелиальной карциномой, связанной с мутациями в FGFR2/3, а футибатиниб и пемигатиниб используют для терапии пациентов с холангиокарциномой, ассоциированной с перестройками FGFR2. Однако у таких препаратов существуют и ограничения в использовании — это связано с патологическим увеличением в крови фосфора из-за нецелевого ингибирования FGFR1, а также с возникновением резистентных мутаций в генах FGFR. Исследователи возлагают надежду на следующее поколение низкомолекулярных ингибиторов, которые сейчас разрабатываются, - среди них лирафугратиниб и LOXO-435, а также FGFR2-специфическое антитело бемаритузумаб. Ожидается, что новые препараты будут с меньшей вероятностью вызывать гиперфосфатемию и будут способны преодолевать мутации, связанные с резистентностью. В новом обзоре представлены перспективы разработки и клинического применения новых ингибиторов FGFR, которые можно будет применять для более широкого списка терапевтических показаний. — FGFR-targeted therapeutics: clinical activity, mechanisms of resistance and new directions.
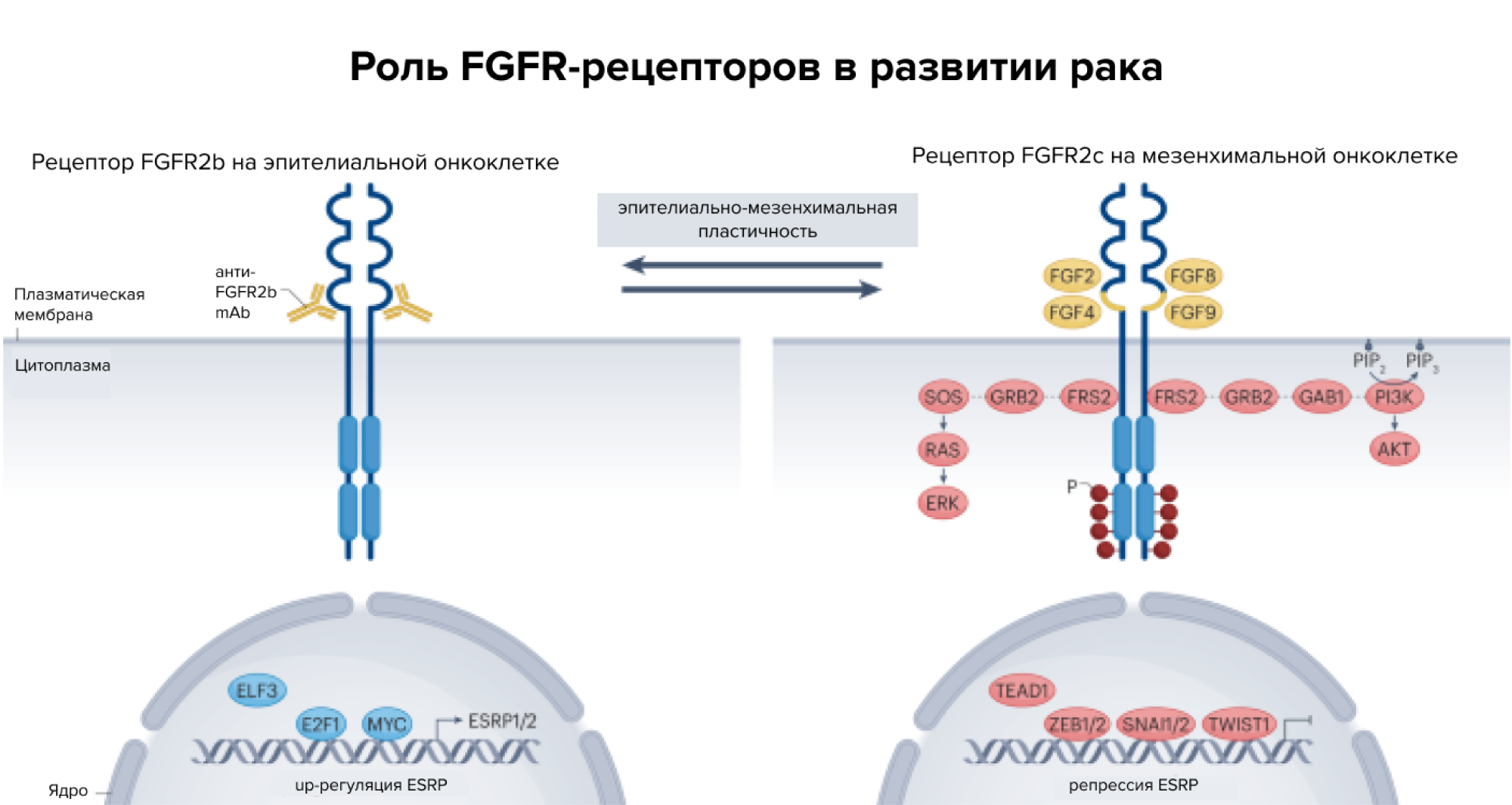
Источник: адаптировано из Nature Reviews Clinical Oncology