
Дайджест #8. Бактериальное оружие против рака мозга
Название «сальмонеллы» обычно ассоциируется с чем-то негативным: болезнями, отравлениями, нечистотой. Но иногда эти бактерии могут быть полезными — если модифицировать их особым образом, они из патогенов превратятся в помощников. Да еще в каких: сальмонелл можно научить «нацеливаться» на опухолевые клетки мозга, чтобы бороться с одним из самых агрессивных типов рака — глиобластомой. Подробности этой трансформации вы узнаете из нового дайджеста.
Онкология
Как улучшить CAR-T-терапию для сóлидных опухолей
Модифицированные T-клетки хорошо зарекомендовали себя для лечения лейкозов, но солидные опухоли все еще остаются сложной задачей для этого вида терапии. Дело в том, что микроокружение таких опухолей, например карцином, не позволяет CAR-T-клеткам проникнуть вглубь, к очагу воспаления. Эти препятствия могут быть связаны с молекулярными причинами, например с ингибированием CAR-T-клеток за счет взаимодействия PD-1/PD-L1. В новом исследовании удалось выяснить, что ключевым фактором, который влияет на высокую восприимчивость Т-клеток к рецепторам PD-1, может быть аффинность антигена CAR. Так, биологи сравнили эффекты воздействия CAR-T-клеток с высокой и низкой аффинностью по отношению к белку HER2, связанному с раком молочной железы, а также по отношению к другим мишеням. На in vitro моделях линий опухолевых клеток удалось показать, что CAR-T-клетки с низкой аффинностью к конкретной мишени (в том числе к HER2) более чувствительны к ингибированию через PD-1, чем клетки с высокой аффинностью. Если применить нокаут PD-1 с помощью CRISPR/Cas9, то у CAR-T-клеток с низкой аффинностью усиливается противоопухолевый ответ — чего не скажешь про CAR-T с высокой аффинностью, на эффективность которых нокаут PD-1 практически не влияет. Эти результаты потенциально способны помочь в совершенствовании CAR-T-терапии для солидных опухолей, связанной с нарушением сигнального пути PD-1/PD-L1. — CAR affinity modulates the sensitivity of CAR-T cells to PD-1/PD-L1-mediated inhibition.
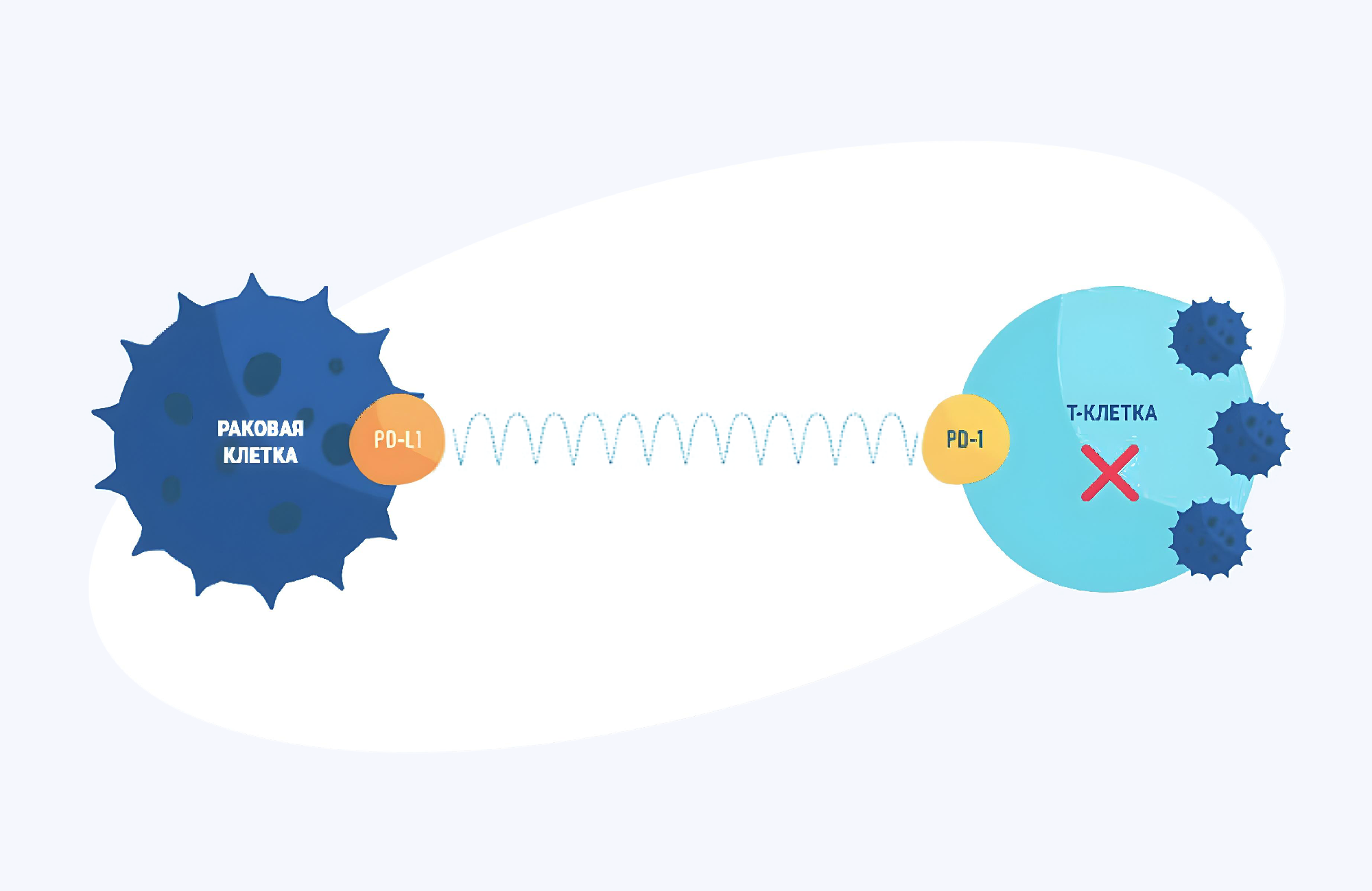
Опухолевые клетки могут ускользать от надзора иммунных Т-клеток. Для этого они активируют на своей поверхности белок PD-L1, который распознает рецептор PD-1 на Т-лимфоцитах, в результате чего подавляется их активность.
Как «прокачать» IL-12 для системного противоопухолевого ответа
Блокада иммунных контрольных точек — один из методов лечения рака. Этот вид терапии заключается в снижении супрессии Т-лимфоцитов, которые инфильтруют опухоль, и, как следствие, в повышении противоопухолевого ответа. К сожалению, существующие способы блокады контрольных точек часто оказываются недостаточно эффективными. Раньше уже предпринимались попытки повысить результативность этого вида лечения с помощью интерлейкина 12 (IL-12) — цитокина, который стимулирует натуральные киллеры и цитотоксические Т-клетки. Однако системное введение IL-12 при терапии ограничено из-за его высокой токсичности. В новом исследовании удалось снизить тяжесть этого побочного эффекта благодаря разработке гибридного белка. Модификация заключается в соединении анти-PD-1 и мышиного низкоаффинного мутанта IL-12-2 (αPD1-mIL12mut2). После введения этого гибрида мышам повышается противоопухолевая активность и практически не обнаруживается токсичность — по крайней мере в пилотных экспериментах. Более того, такое лечение способно подавлять дистальные опухоли и метастазы, что обещает потенциальные перспективы для устранения отдаленных воспалительных очагов. — Anti-PD-1 cis-delivery of low-affinity IL-12 activates intratumoral CD8+T cells for systemic antitumor responses.
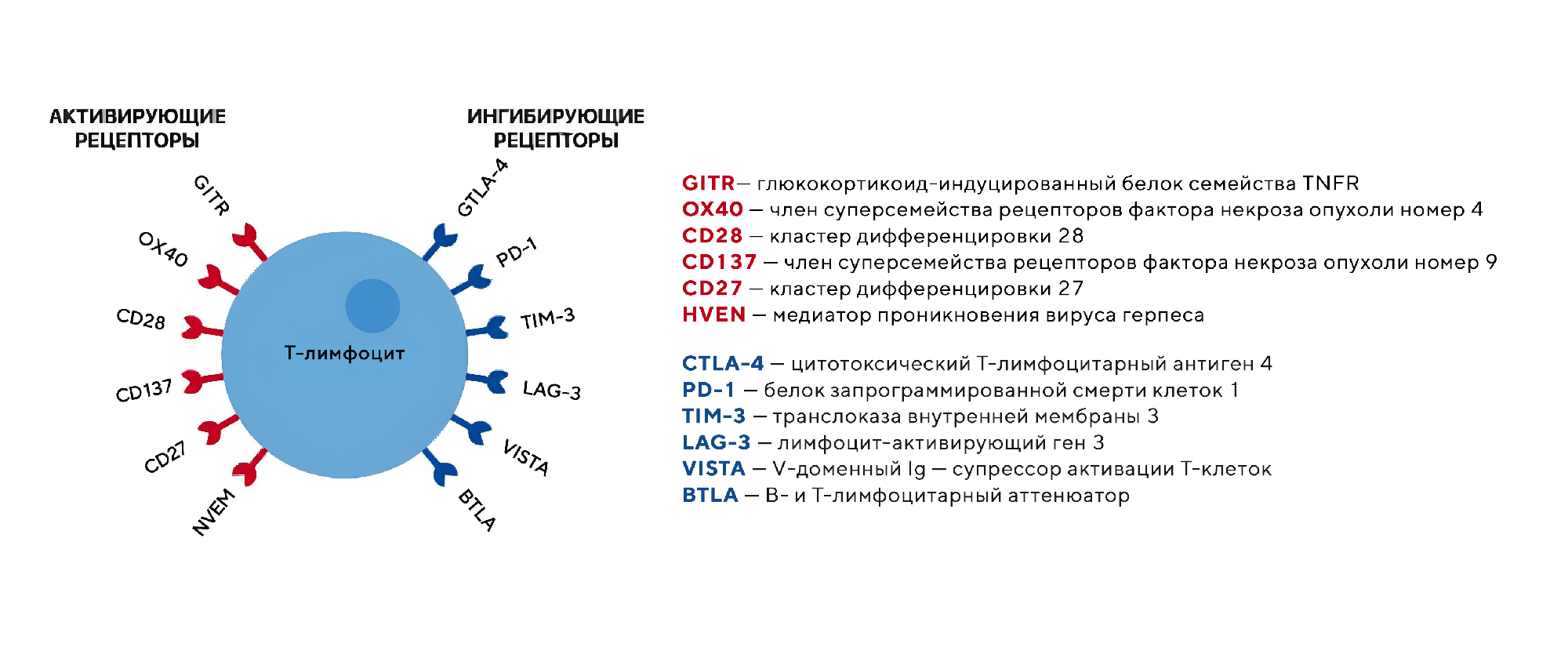
Иммунные контрольные точки — ключевой элемент регуляции Т-лимфоцитов. Активация или ингибирование соответствующих рецепторов на поверхности Т-клеток способно делать опухоль «видимой» для иммунной системы.
Кто стимулирует вторжение онкоклеток при РМЖ
YAP — белок-механорегулятор, который в норме участвует в регенерации кожи, конкретно — улучшает выравнивание коллагена. Однако нарушения регуляции YAP могут приводить к усиленной пролиферации и инвазии онкоклеток, способствуя развитию рака молочной железы. Недавно этот механизм удалось продемонстрировать на модели карциномы молочной железы. Так, белок-регулятор YAP активируется при вторжении онкоклеток, которые сохраняют характеристики эпителиальных клеток, во многом благодаря кератину 14. Оба этих события — появление онкоклеток и экспрессия кератина 14 — запускаются коллагеном 1, который, в свою очередь, повышает активацию белка YAP. Весь этот цикл еще увеличивает инвазию онкоклеток. Возможно, YAP-белок станет потенциальной мишенью для лечения рака молочной железы. — A YAP-centered mechanotransduction loop drives collective breast cancer cell invasion.
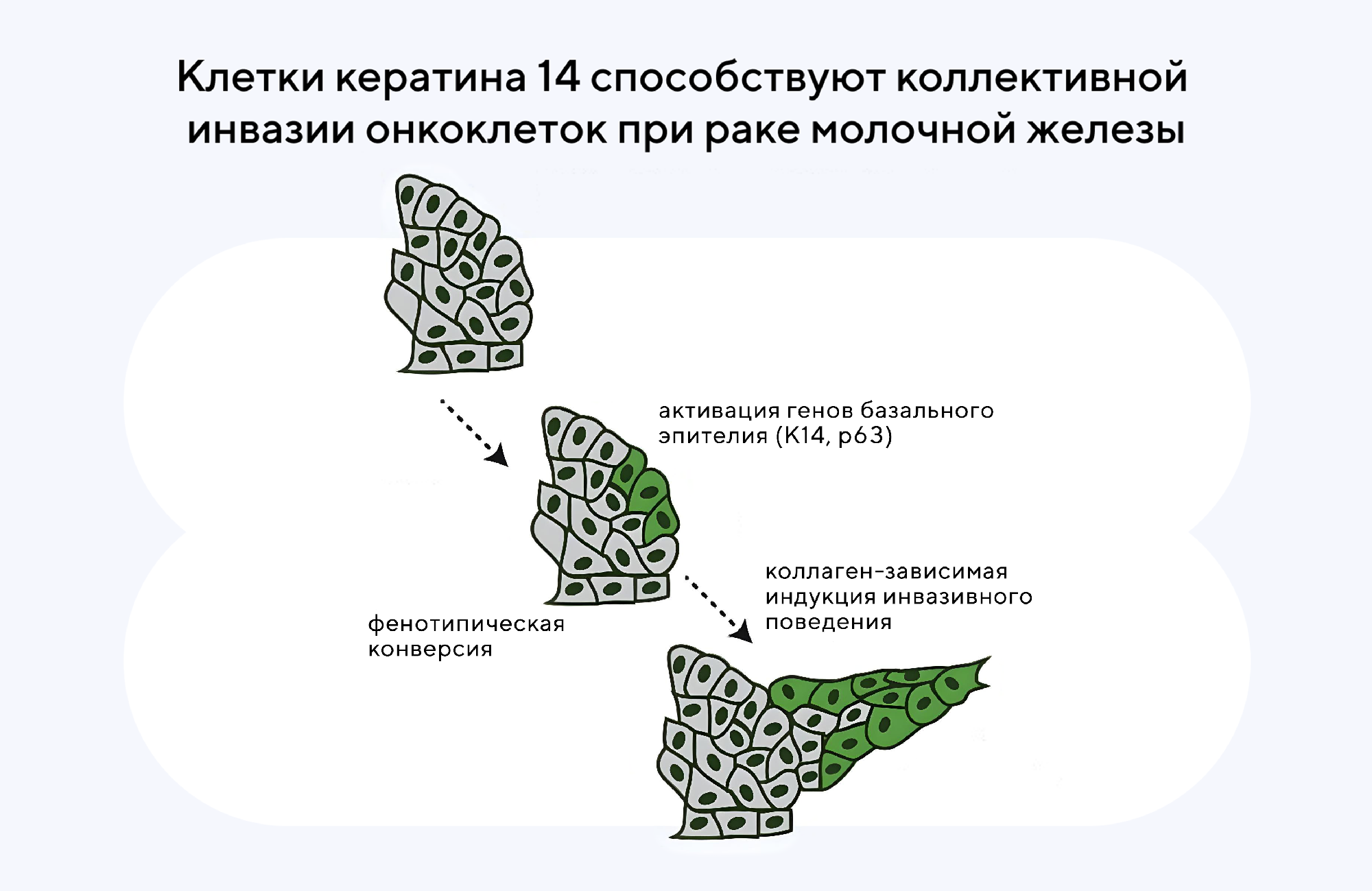
Источник: Cell
Бактерии против рецидивов рака мозга
Агрессивную форму опухоли мозга — глиобластому — очень сложно вылечить: даже после хирургического удаления в мозге могут остаться доброкачественные новообразования, способные со временем приводить к рецидиву. Ситуация усугубляется тем, что мозг является иммунологически привилегированным органом, в котором иммунные клетки проявляют толерантность по отношению к оставшимся после операции остаточным опухолевым клеткам. В новом исследовании, кажется, удалось обойти этот барьер: для предотвращения рецидивов ученые использовали особый гидрогель, точечно нацеленный на остаточные клетки-сателлиты опухоли. В основе этой гидрогелевой структуры — иммуностимулирующие средства доставки на основе аттенуированной сальмонеллы Salmonella typhimurium, которые целенаправленно ищут остаточные онкоклетки. Ранее подобные методы лечения с использованием ослабленных штаммов сальмонеллы уже удалось продемонстрировать в моделях колоректального рака и рака кишечника. В новой работе суть терапии заключается в следующем: сначала в организм вводят капсулы гидрогеля с сальмонеллой, которые ищут и внедряются в остаточные онкоклетки. После этого вводят нанокапсулы, которые запускают лизис сальмонеллы: бактерии погибают, разрушая вместе с собой раковые клетки. Дополнительно к месту, где это произошло, рекрутируются фагоциты, и происходит последующая презентация антигена, что формирует адаптивный иммунный ответ. Такая бактериотерапия усиливает иммунитет у пациентов, имеющих высокий риск рецидивов после удаления глиобластомы. — Stimulation of tumoricidal immunity via bacteriotherapy inhibits glioblastoma relapse.
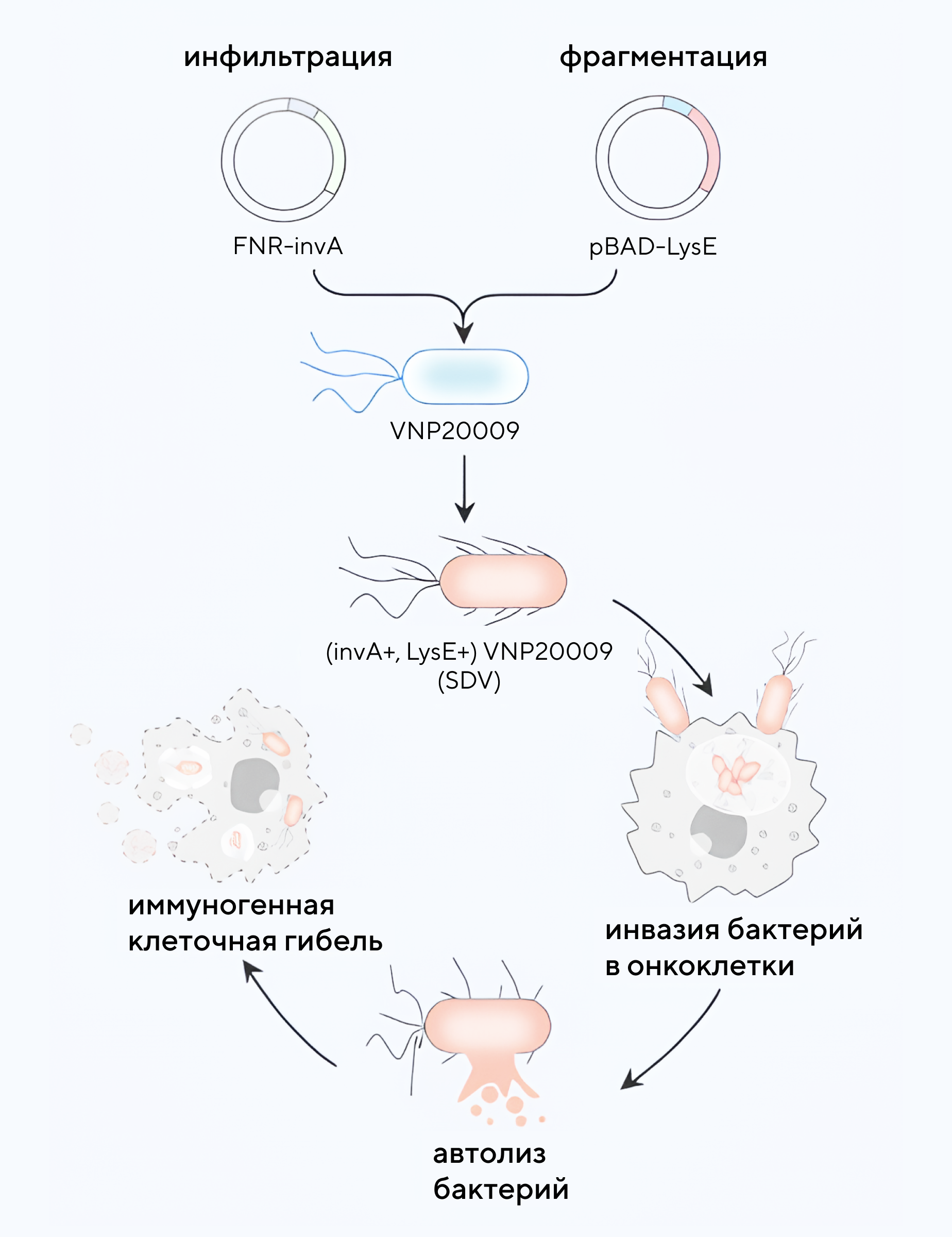
Механизм лечения: сначала клетки сальмонеллы трансформируют, нацеливая их на остаточные клетки глиобластомы, а затем вызывают их лизис и последующее разрушение онкоклеток. Источник: Nature Communications
Аутоиммунные заболевания
Белок — «предсказатель» течения рассеянного склероза
Лечение рассеянного склероза осложняется пока еще недостаточными методами ранней диагностики последствий этой болезни. В недавнем исследовании с помощью методов машинного обучения решили оценить вклад в развитие заболевания пяти миелоидных маркеров, выделенных из спинномозговой жидкости пациентов с рассеянным склерозом. Один из них — белок CHIT1 (chitotriosidase 1, или хитотриозидаза) — оказался надежным индикатором более быстрого развития инвалидности. Обычно этот белок экспрессируется клетками микроглии, расположенными в активных очагах поражения мозга при рассеянном склерозе. Оказалось, что экспрессия CHIT1 связана с переходом микроглиальных клеток к более активному состоянию, связанному с быстрым прогрессированием болезни. Этот вывод дает основания полагать, что CHIT1 может стать ранним маркером ускоренного развития и более ранней инвалидизации при рассеянном склерозе. — CHIT1 at diagnosis predicts faster disability progression and reflects early microglial activation in multiple sclerosis.
Структура человеческой хитотриозидазы 1 (CHIT1). Источник: SinoBiological
Хроматиновый атлас для визуализации разных типов ревматоидного артрита
Одно из отличительных проявлений ревматоидного артрита — воспаление синовиальных оболочек суставов. Ранее уже удалось выяснить, что воспалительный патогенез в суставах связан с периферическими Т-хелперами, однако эпигенетическая составляющая этого процесса все еще плохо изучена. Эпигенетическая регуляция включает все процессы, связанные с изменениями состояний хроматина и взаимодействиями ДНК, РНК и белков, при этом не затрагивая нуклеотидные последовательности. Исследуя состояния хроматина по всему геному, в новом исследовании удалось выделить 24 хроматиновых класса и связанные с ними факторы транскрипции, в том числе класс CD8+ клеток GZMK+ и класс фибробластов, связанный с AP-1. В результате ученые создали настоящий «хроматиновый атлас», который показывает связи между состояниями хроматина и фенотипами ревматоидного артрита. — The chromatin landscape of pathogenic transcriptional cell states in rheumatoid arthritis.
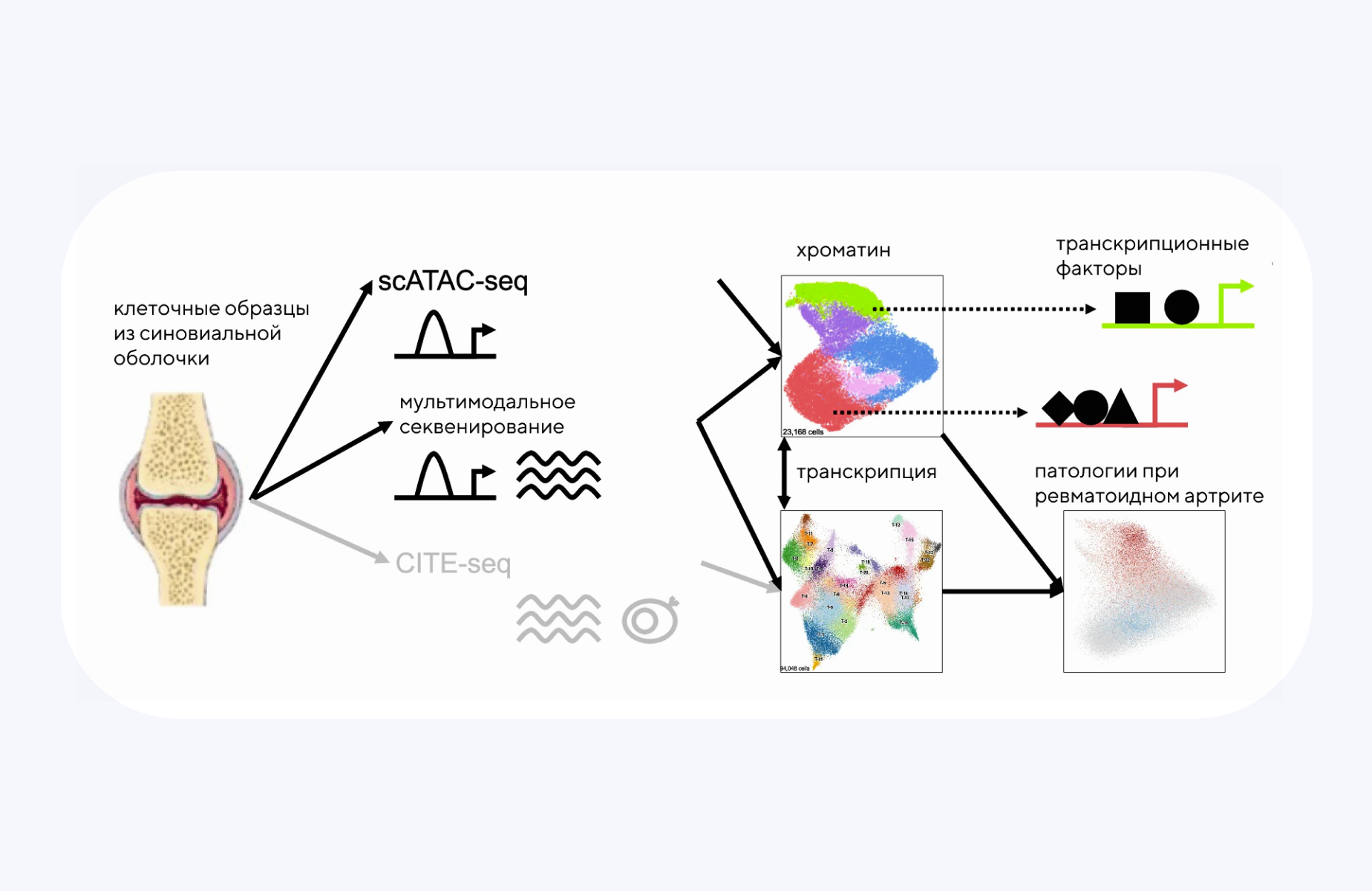
Источник: Nature
Communications
Для исследования взяли образцы клеток из синовиальной оболочки пациентов с ревматоидным и остеоартритом. Дальнейшие эксперименты проводили с унимодальным scATAC-seq и мультимодальным секвенированием; референсное исследование AMP-RA14 провели с помощью CITE-seq. В результате удалось определить классы хроматина для уни- и мультимодальных моделей и сравнить их с состояниями AMP-RA14. Как итог, исследователи выделили факторы транскрипции, которые, вероятно, регулируют описанные классы хроматина и связаны с патологическим воспалением при ревматоидном артрите.