
Научный дайджест #30: «троянские кони» против опухолевых клеток
Разработка методов иммунотерапии во многом стала революционной для лечения злокачественных заболеваний. Но, к сожалению, многие опухоли научились приобретать устойчивость к иммунотерапевтическим препаратам вроде анти-PD-1-антител. И здесь на помощь вполне может прийти своеобразный «троянский конь» — а именно инновационные конъюгаты эритроцитов с антителами (например, с теми самыми анти-PD-1). Это «секретное оружие» продлевает циркуляцию терапевтических молекул в крови, усиливая их накопление в опухолях и активируя Т-лимфоциты для атаки на опухолевые клетки. Подробнее об этой стратегии лечения, а также о других прорывах в молекулярной онкологии читайте в нашем новом дайджесте.
Эритроциты на страже иммунотерапии: как преодолеть резистентность
Иммунотерапия с использованием ингибиторов контрольных точек, таких как анти-PD-1-антитела, в свое время стала революцией в лечении солидных опухолей. Эта стратегия позволяет активировать иммунный ответ организма против злокачественных новообразований. Однако у этого способа лечения есть недостаток: у некоторых пациентов спустя время развивается резистентность. Причины могут быть разными — устойчивость к терапии может возникать из-за сниженного поглощения антител опухолевыми клетками, изменений в микроокружении и недостаточной активации Т-лимфоцитов. Все это приводит к рецидивам и прогрессированию заболевания.
Чтобы преодолеть эти барьеры, исследователи создали инновационные конъюгаты эритроцитов с анти-PD-1-антителами. Так, красные кровяные клетки служат своеобразным «троянским конем», накапливаясь в опухоли, где локально высвобождают антитела и усиливают их поглощение макрофагами и Т-клетками. В моделях резистентного рака молочной железы и меланомы такие конъюгаты значительно повысили противоопухолевый эффект, восстановив чувствительность к терапии без повышения системной токсичности. Это исследование открывает путь к развитию доступных и эффективных стратегий иммунотерапии для повышения эффективность лечения у пациентов с рецидивирующим раком. — Erythrocyte-antibody conjugates to overcome immunotherapy resistance.
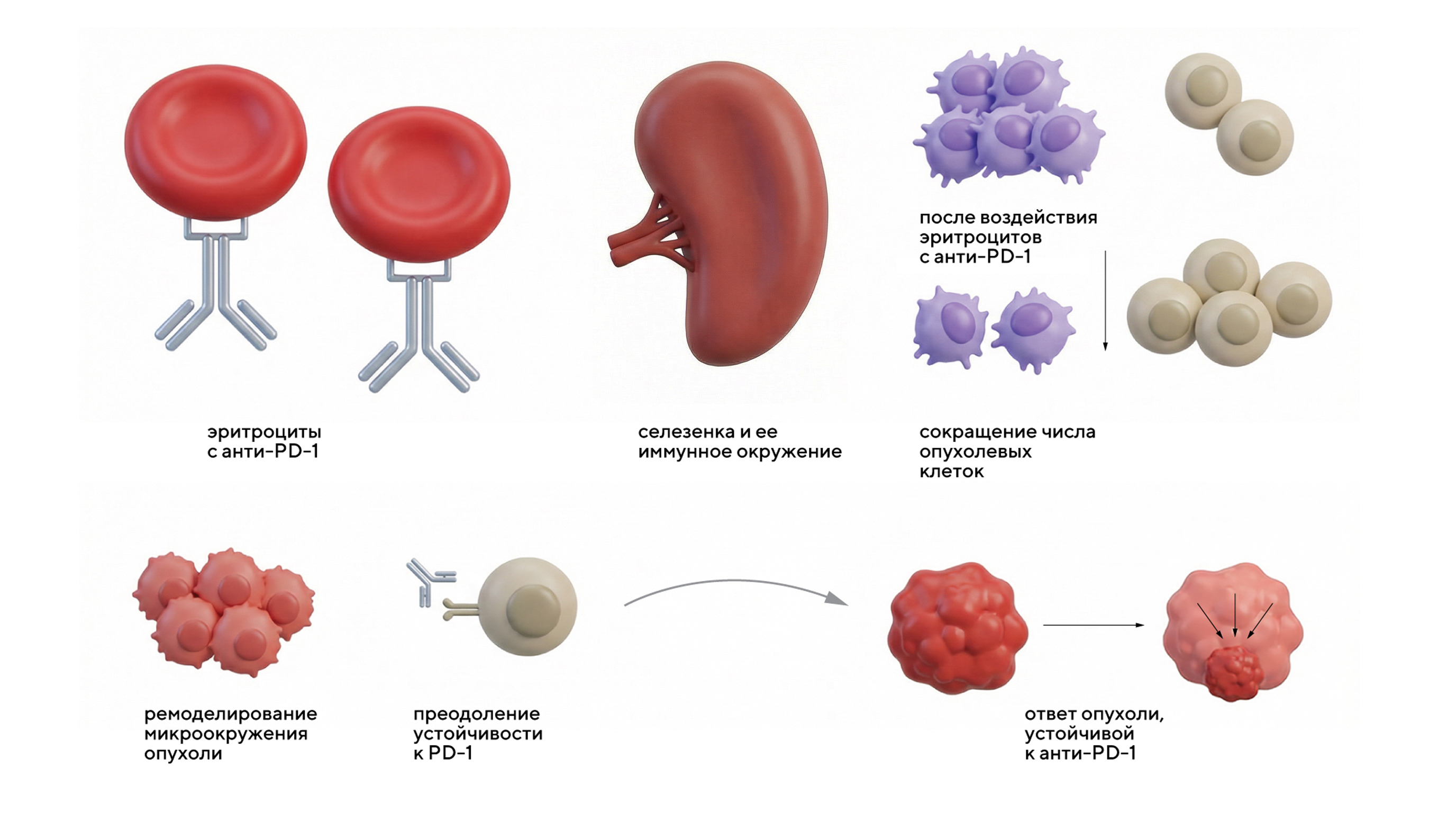
Схема эксперимента. В результате действия конъюгатов эритроцитов с анти-PD-1-антителами удалось повысить противоопухолевый эффект в моделях резистентного рака молочной железы и меланомы. Источник: адаптировано из Nature
NKG2A под прицелом: схема иммунотерапии с применением биспецификов
В норме NK-клетки и T-лимфоциты работают в роли ключевых эффекторов, связываясь с опухолевыми клетками и запуская процесс их уничтожения. Однако не все так радужно: в случае если в этих иммунных клетках повышается экспрессия гена, контролирующего синтез белка NKG2A, происходит связывание NKG2A с молекулой HLA-E в клетках опухолей. В результате происходит «торможение» иммунной реакции и опухоли словно ускользают из-под иммунного надзора.
Чтобы преодолеть этот порочный круг, исследователи идентифицировали два полностью человеческих моноклональных антитела против NKG2A, которые блокируют связывание с HLA-E. Благодаря модицифированным биспецифическим активаторам (BiNK, bispecific engagers), которые сочетали в себе анти-NKG2A и антитела против опухолевых маркеров вроде HER2 или EGFR, удалось продемонстрировать значительное подавление роста опухоли в мышиных моделях рака легких. Такое комбинированное воздействие может стать перспективным направлением для дальнейшей разработки иммунотерапевтических препаратов. — Discovery and preclinical evaluation of monoclonal antibodies and bispecific engagers targeting the NKG2A inhibitory receptor.
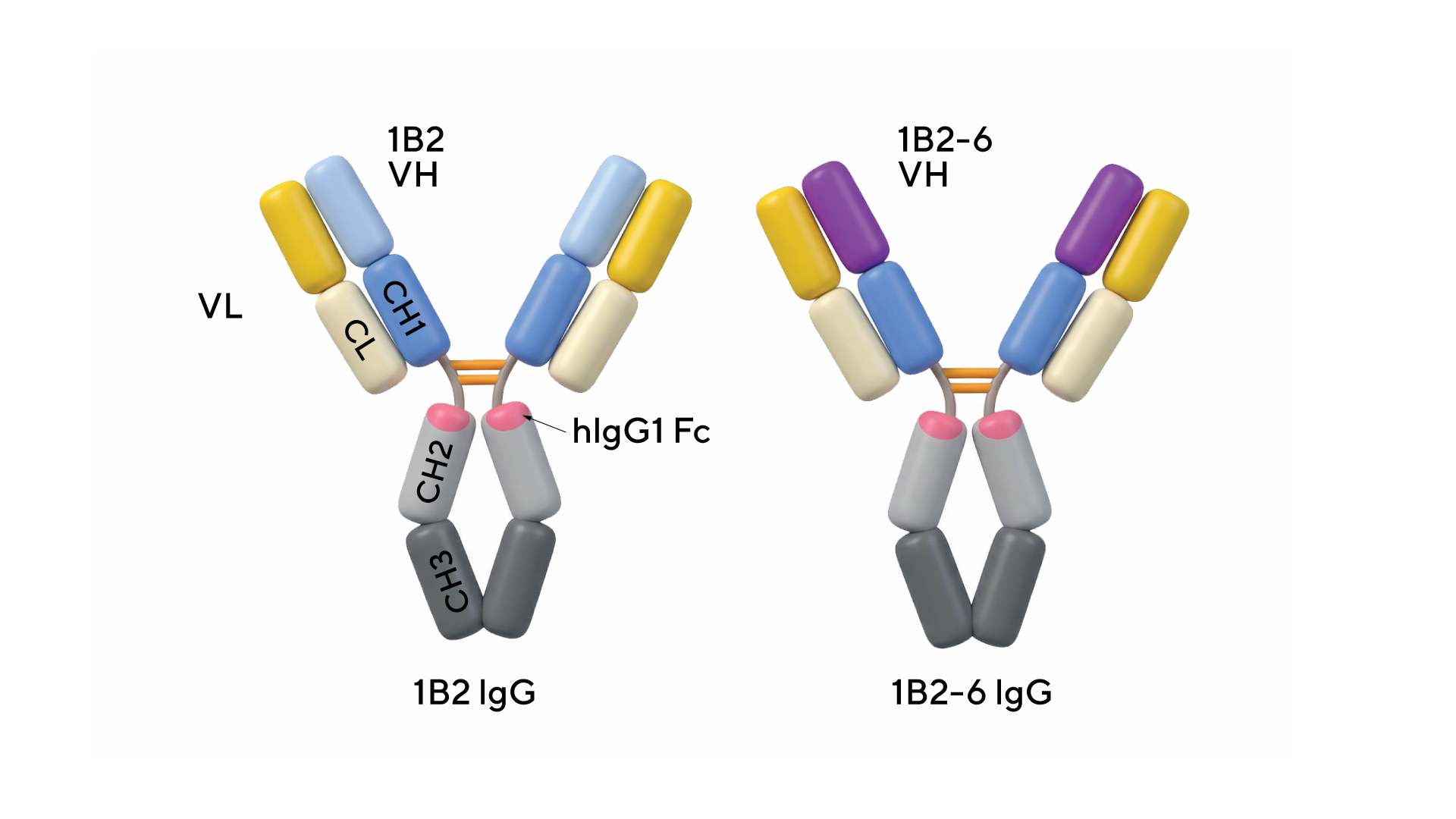
Схематическое изображение молекулы биспецифика с мутациями L234A, L235A и P329G, которые устраняют способность связывания с Fc-гамма-рецепторами. Источник: адаптировано из Science
Как «прокачать» иммунотерапию для борьбы с резистентными опухолями
Устойчивость опухолей к иммунотерапии — одна из главных проблем в лечении злокачественных новообразований. Несмотря на то что терапия с использованием ингибиторов иммунных контрольных точек в свое время произвела настоящую революцию в онкологии, многие виды опухолей не поддаются воздействию лекарственных препаратов или развивают резистентность, связанную с трансформирующим фактором роста β1 (TGFβ1). Однако в январе 2026 года были опубликованы результаты многоцентрового исследования фазы I (DRAGON trial, NCT04291079), в котором исследователи протестировали моноклональное антитело linavonkibart. Эта молекула селективно блокирует латентную форму TGFβ1 после проведенной ранее, но оказавшейся неэффективной анти-PD-1-терапии у пациентов с метастатическими солидными опухолями. Причем эти результаты удалось показать как в случае монотерапии, так и в комбинации с другим антителом — пембролизумабом. Этот подход может стать важным шагом в преодолении устойчивости к иммунотерапии, предлагая новый способ лечения для пациентов со злокачественными новообразованиями. — Linavonkibart and pembrolizumab in immune checkpoint blockade-resistant advanced solid tumors: a phase 1 trial.
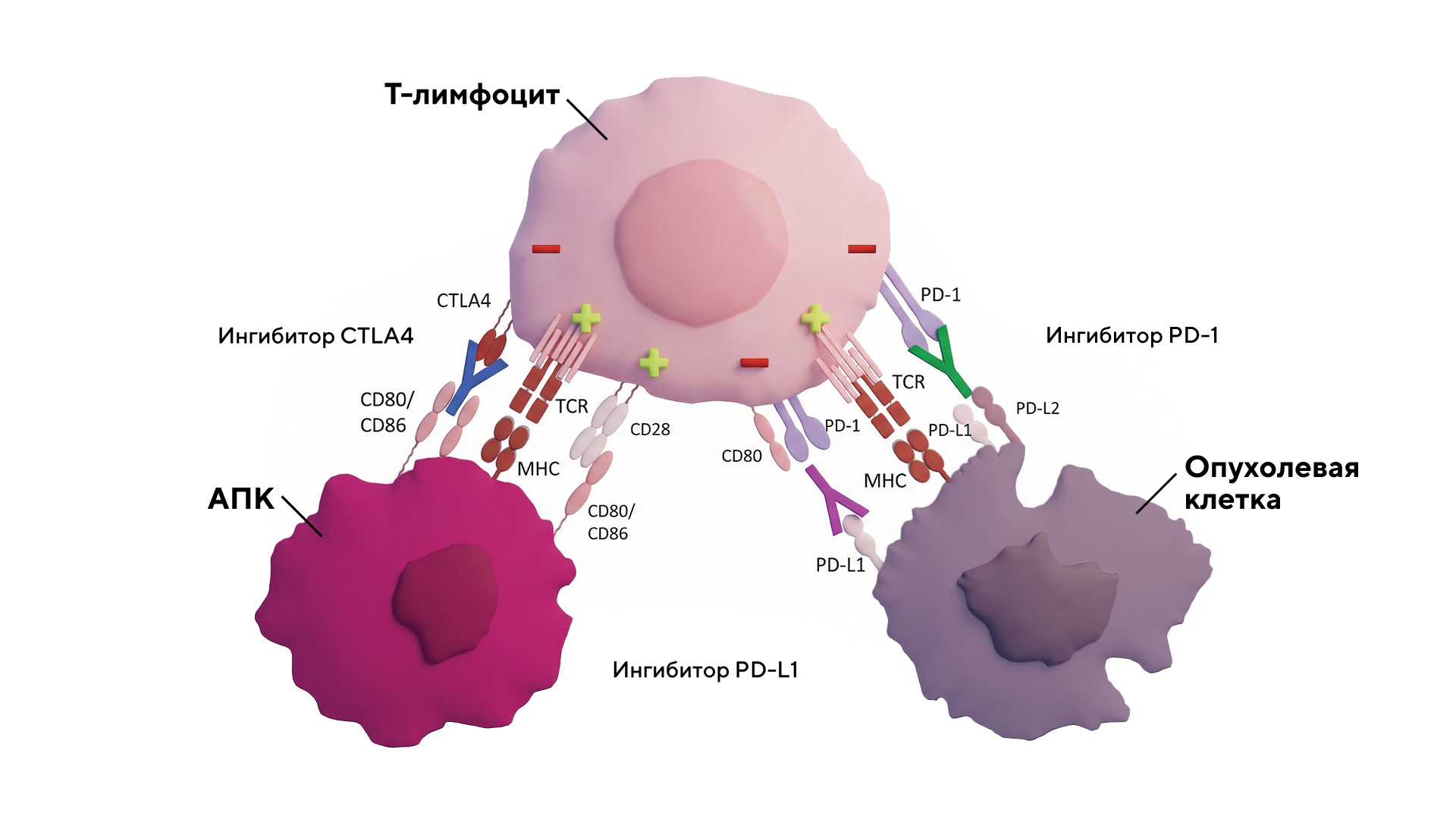
Молекулярные мишени ингибиторов контрольных точек иммунитета. Для преодоления резистентности к иммунотерапии с помощью анти-PD-1 можно использовать терапию с использованием антитела linavonkibart. Источник: адаптировано из Springer Nature
«Умные» нанокапсулы для точечного редактирования генов
В недавнем исследовании представили необычный способ генетического редактирования с помощью технологии CRISPR в виде концепции «умных» нанокапсул. Эти микроскопические носители, несущие в себе CRISPR-компоненты, после проникновения в организм высвобождаются только под действием внешнего лазера в зоне опухоли. Благодаря этому удается обеспечивать точную доставку системы без вреда для здоровых тканей. Конечно, пока что это только концепция, которой, если повезет, предстоит множество тестирований и проверок. Однако в случае, если эта технология получит «зеленый свет», это потенциально откроет путь для персонализированного и неинвазивного лечения злокачественных новообразований. — Perspective of smart nanocapsule swallowable laser-guided for integrated sensing and crispr-mediated cancer gene editing.
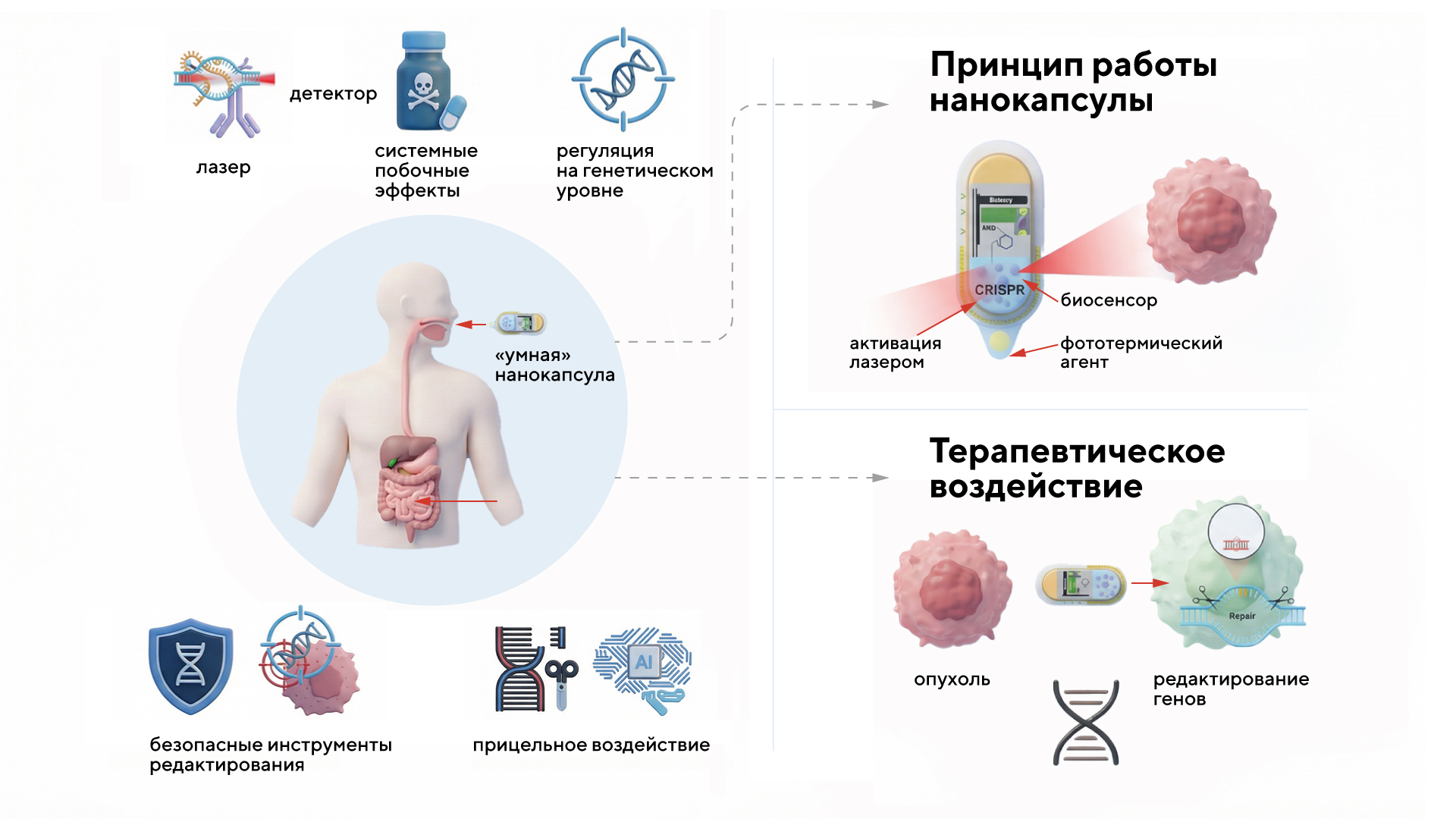
Краткий обзор принципа работы и терапевтического воздействия «умной» нанокапсулы. Разработка подобных противоопухолевых препаратов на основе CRISPR-технологии открывает потенциал для лечения злокачественных новообразований. Источник: адаптировано из Cancer Gene Therapy
SCYL2: как работает скрытый онкологический «переключатель»
Клатрин-ассоциированный белок SCYL2 — один из факторов внутриклеточного транспорта, который взаимодействует с эндосомами и влияет на сигнальные пути в опухолевых клетках. Недавно исследователи выявили, что SCYL2 способствует инактивации PTEN — ключевого супрессора опухолей — через посттрансляционные модификации. Это активирует путь PI3K/AKT, стимулируя рост и выживание опухолевых клеток. Эксперименты на моделях разных видов рака показали, что повышенная экспрессия SCYL2 усиливает сигнализацию AKT, способствуя канцерогенезу, в то время как его подавление снижает пролиферацию и метастазирование.
Эти результаты открывают перспективы применения SCYL2 как новой терапевтической мишени для ингибиторов PI3K/AKT в онкологии, потенциально повышая эффективность лечения солидных опухолей и снижая резистентность к существующим препаратам, таким как ингибиторы PTEN. — Clathrin-associated SCYL2 contributes to the activation of PI3K/AKT signaling and tumorigenesis through PTEN phosphorylation in adult T-cell leukemia/lymphoma.
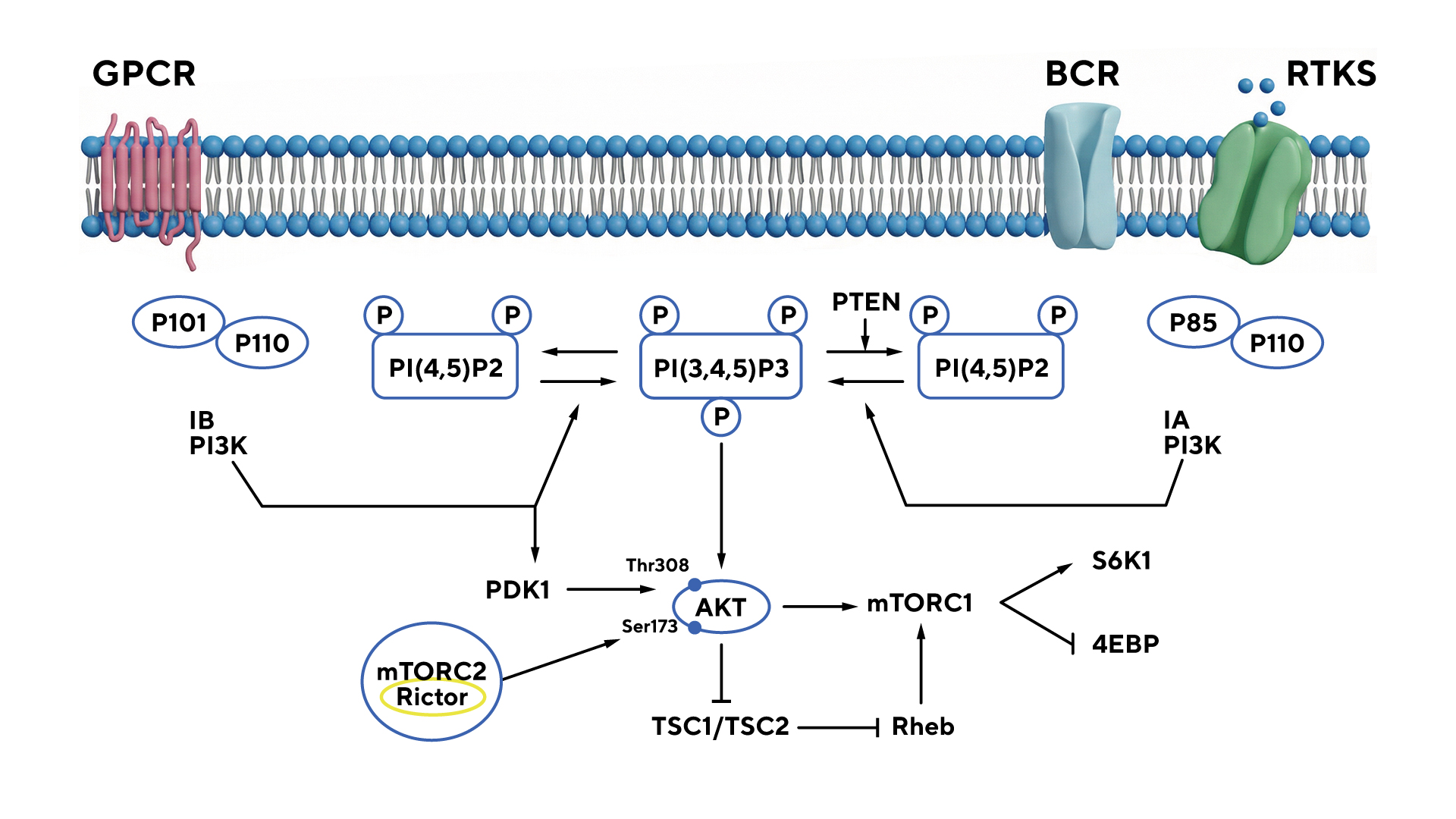
В фокусе исследования оказалось ингибирование сигнального пути PI3K/AKT, где белок PTEN действует как негативный регулятор. Источник: адаптировано из Cell Death&Disease