Научный дайджест #32: «размораживаем» опухоли за счет перепрограммирования микроокружения
Многие опухоли считаются «холодными» — в них практически не проникают лимфоциты, поэтому иммунотерапия при лечении подобных злокачественных новообразований оказывается практически бессильной. Однако не стоит думать, будто такие опухоли «безнадежно заморожены» — в недавнем исследовании ученые рассказали о разработке моноклонального антитела, которое позволяет перепрограммировать микроокружение опухоли, превращая ее из «холодной» в «горячую». О том, как преодолевать устойчивость в случае лечения «холодных» опухолей, а также о других новостях из мира молекулярной биологии читайте в нашем новом дайджесте.
Разработан новый коктейль антител для терапии рака молочной железы
Способы лечения тройного негативного рака молочной железы до сих пор ограничены в применении из-за высокой резистентности опухоли. Чтобы преодолеть это ограничение, в недавнем исследовании описали набор специфических мутантных белков, уникальных для опухолевых клеток, на которые можно воздействовать с помощью коктейля поликлональных антител. Эксперимент на мышиной клеточной линии EMT6 продемонстрировал, что из 12 мутировавших белков опухоли на связывание с антителами «откликнулись» 9 белков, причем без заметного взаимодействия с нормальными здоровыми тканями. Введение коктейля из 9 антител против таких белков мышам продемонстрировало замедление роста опухоли и улучшение выживаемости, особенно в сочетании с анти-PD-1-терапией. Перспективы этого открытия могут быть достаточно многообещающими, ведь опухолевые клетки значительной части пациенток с трижды негативным раком молочной железы содержат такие мутировавшие белки. — Novel antibody cocktail therapy targeting extracellular tumor-specific mutations to treat EMT6 cell line-derivedtriple-negative breast cancer.
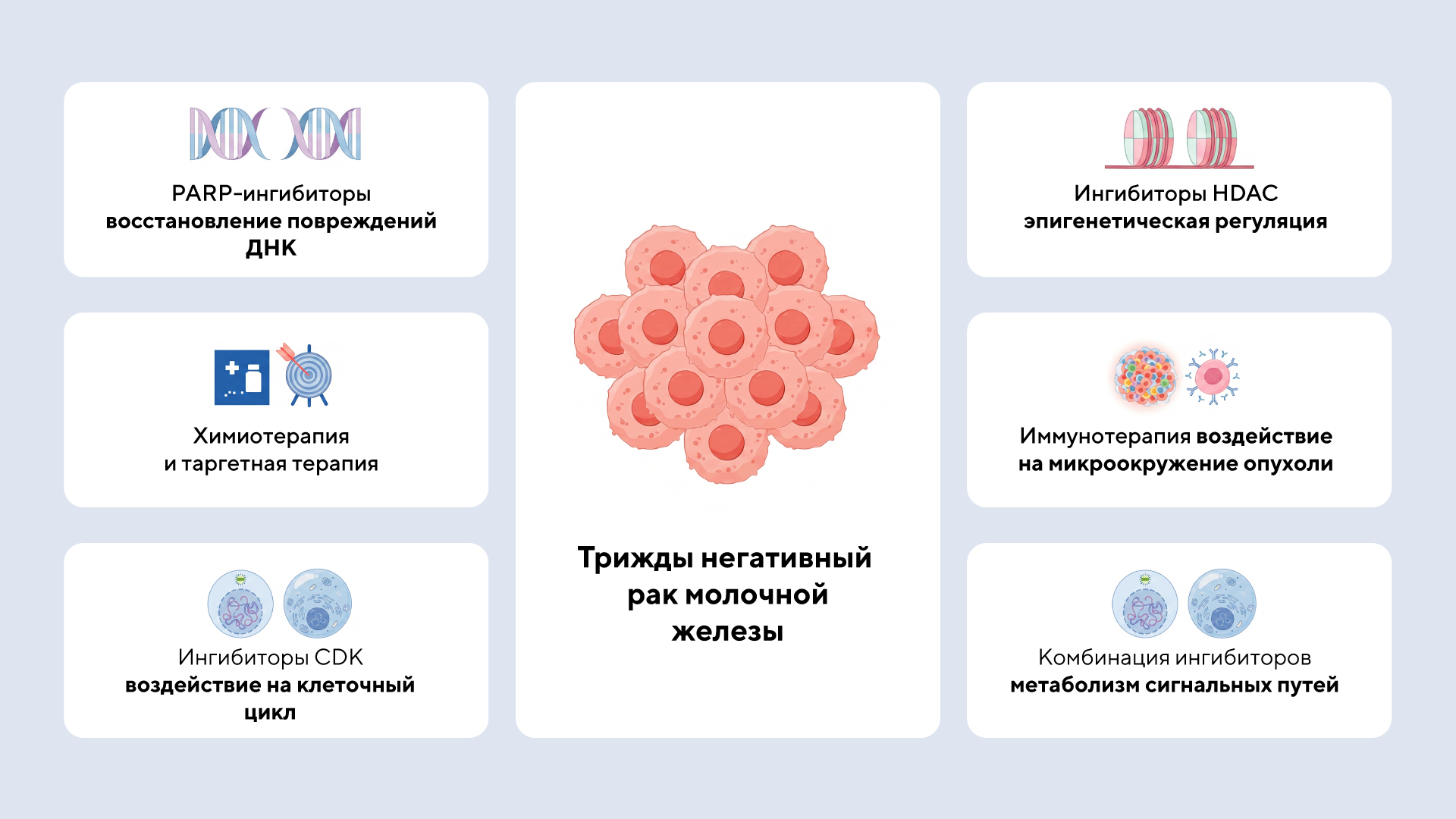
Схема различных вариантов терапевтических стратегий при трижды негативном раке молочной железы. Источник: MDPI
Как перепрограммировать микроокружение опухоли с помощью AXL
В онкологии существует понятие «холодных» опухолей — они представляют собой особый тип злокачественных новообразований, которые имеют низкую иммуногенность, содержат мало Т-лимфоцитов и окружены клетками, подавляющими иммунитет. В результате такие образования практически невидимы для иммунной системы и устойчивы к иммунотерапии с помощью ингибиторов чекпоинтов. Способность «взламывать» эту опухолевую блокаду могла бы стать перспективным способом для лечения «холодных» опухолей. И некоторые успехи в этом есть: так, например, в недавнем исследовании ученые описали стратегию перепрограммирования микроокружения опухоли через рецептор AXL. Биологи разработали антитело 6C5, направленное на один из эпитопов AXL, в результате чего микроокружение опухоли становится менее подавляющим для иммунных клеток. Комбинация этого антитела с двойной блокадой иммунных контрольных точек (анти-PD-1 в сочетании с анти-CTLA-4) приводила к мощной регрессии опухоли и формированию устойчивой иммунной памяти. Разработанный подход может повысить эффективность лечения опухолей, устойчивых к иммунотерапии. — Reprogramming the tumor microenvironment with antibody against membrane-proximal AXL to overcome immune checkpoint blockade resistance.
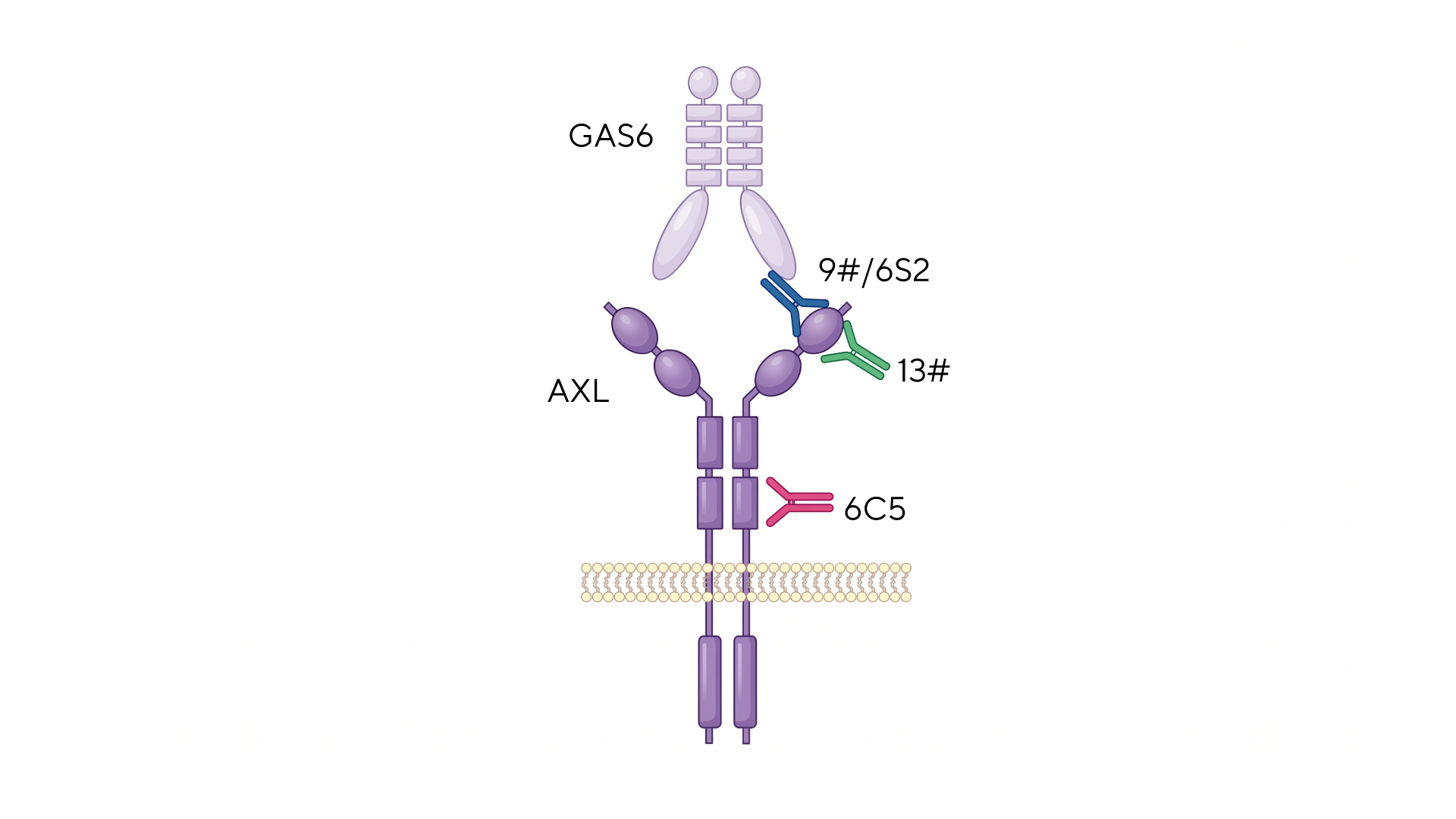
Схематическое изображение антител, связывающихся с различными эпитопами AXL. Источник: Signal Transduction and Targeted Therapy
Как аутоантиген влияет на развитие воспаления
В развитии многих аутоиммунных заболеваний участвуют аутоантитела против внутриклеточного Fc-рецептора TRIM21. Долгое время функции этого внутриклеточного рецептора связывали преимущественно с противовирусной защитой, однако новое исследование раскрывает неожиданную роль TRIM21 в формировании воспаления после гибели клеток. Так, удалось выяснить, что после некротической гибели клеток TRIM21 связывает антитела, которые оказываются внутри клетки, и формирует так называемые провоспалительные иммунные комплексы. Эти комплексы активируют сигнальные пути, ведущие к выбросу медиаторов воспаления и привлечению иммунных клеток. Таким образом, TRIM21 выступает своеобразным «мостиком» между процессами повреждения тканей и развитием иммунного ответа, что может быть важно при аутоиммунных и воспалительных заболеваниях. Это открывает новые перспективы в медицине и потенциально способно помочь в разработке таргетных методов терапии, направленных на снижение избыточного воспаления при аутоиммунных болезнях. — The autoantigen TRIM21 assembles proinflammatory immune complexes after lytic cell death.
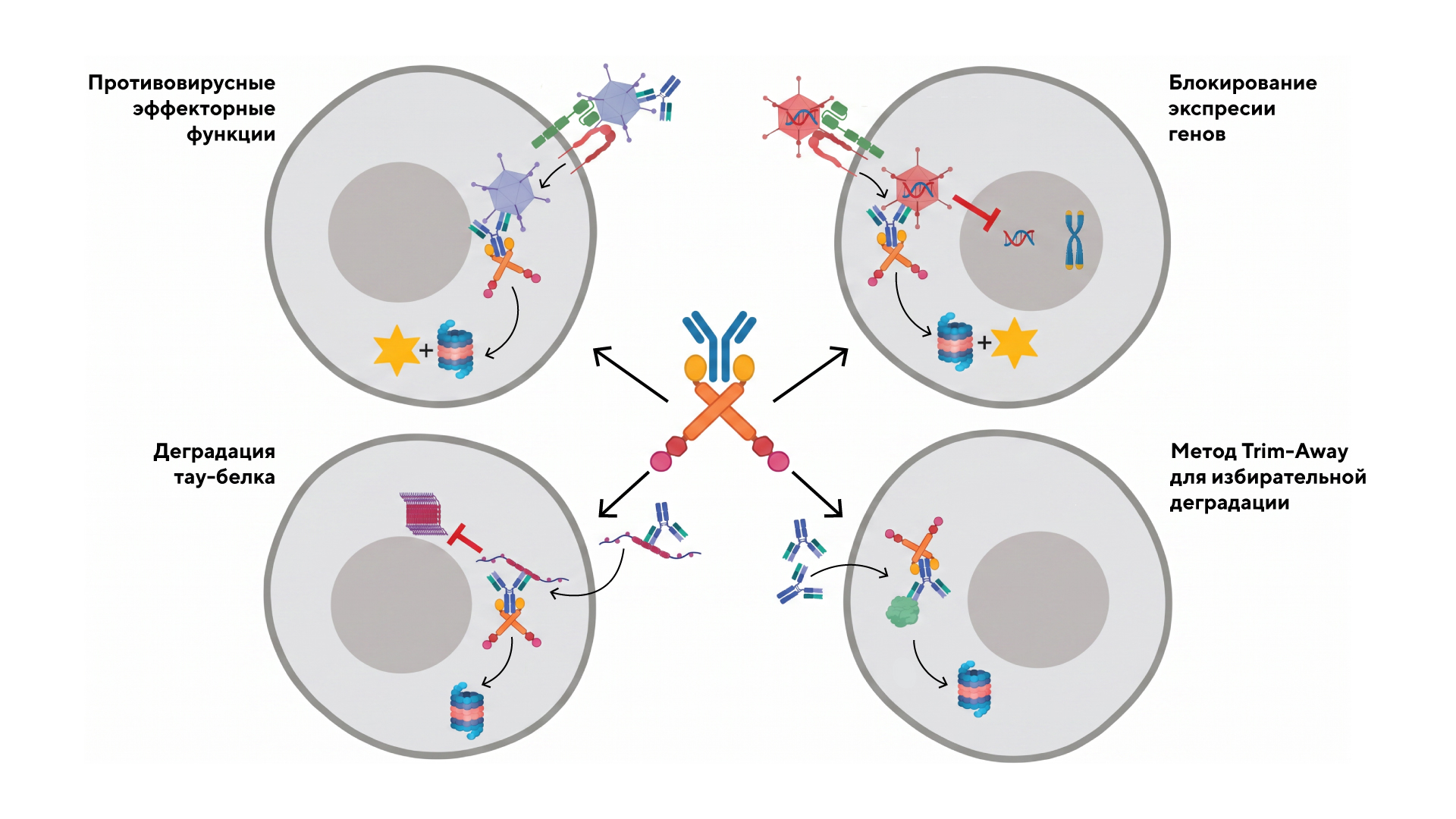
Роль TRIM21 в случае развития заболеваний и их лечения: TRIM21 обеспечивает двойной эффекторный и сигнальный ответы во время инфекции Ad5; блокирует экспрессию генов; вызывает разрушение тау-белка; обеспечивает протеасомную деградацию целевого белка (метод TRIM-Away). Источник: адаптировано из Frontiersin
Белок Pcbp1 как «энергетический страж» в иммунных клетках
В-лимфоциты — ключевые участники в развитии адаптивного иммунитета: именно с их помощью получается координировать гуморальный ответ за счет выработки антител в случае «атаки» на организм. В недавнем исследовании выяснилось, что одним из ключевых регуляторов выработки антител в В-лимфоцитах является белок Pcbp1. Дефицит Pcbp1 приводил к значительному снижению экспрессии иммуноглобулина М и к нарушению дифференцировки В-лимфоцитов зародышевых центров. Такой эффект происходил из-за нарушения целостности митохондрий в клетках. Получается, что белок Pcbp1 работает как важный молекулярный регулятор, что делает его одним из факторов, влияющих на адаптивный иммунитет. — RNA binding protein Pcbp1 maintains mitochondria integrity to promote antibody production and germinal center response.
Структура белка Pcbp1. Источник: «Википедия»
Как «удаление» Treg-клеток помогает NK-клеткам взять опухоли под контроль
Регуляторные Т-лимфоциты (Treg) — это особая популяция иммунных клеток, которые подавляют активность других лимфоцитов, в том числе цитотоксических CD8⁺ Т-клеток. В опухолях Treg могут создавать своеобразный «щит», мешающий иммунитету бороться со злокачественными новообразованиями. В недавнем исследовании обнаружился интересный эффект: селективное удаление Treg-клеток внутри опухоли запускает мощный противоопухолевый ответ со стороны NK-клеток (естественных киллеров). Оказалось, что без подавляющего влияния Treg-клеток NK-клетки активируются и начинают эффективно уничтожать опухолевые клетки, даже если те устойчивы к CD8⁺ Т-лимфоцитам. Этот механизм открывает потенциально перспективный путь для борьбы со злокачественными новообразованиями, которые не поддаются стандартным методам лечения. — Intratumoral Treg cell ablation elicits NK cell-mediated control of CD8 T cell-resistant tumors.
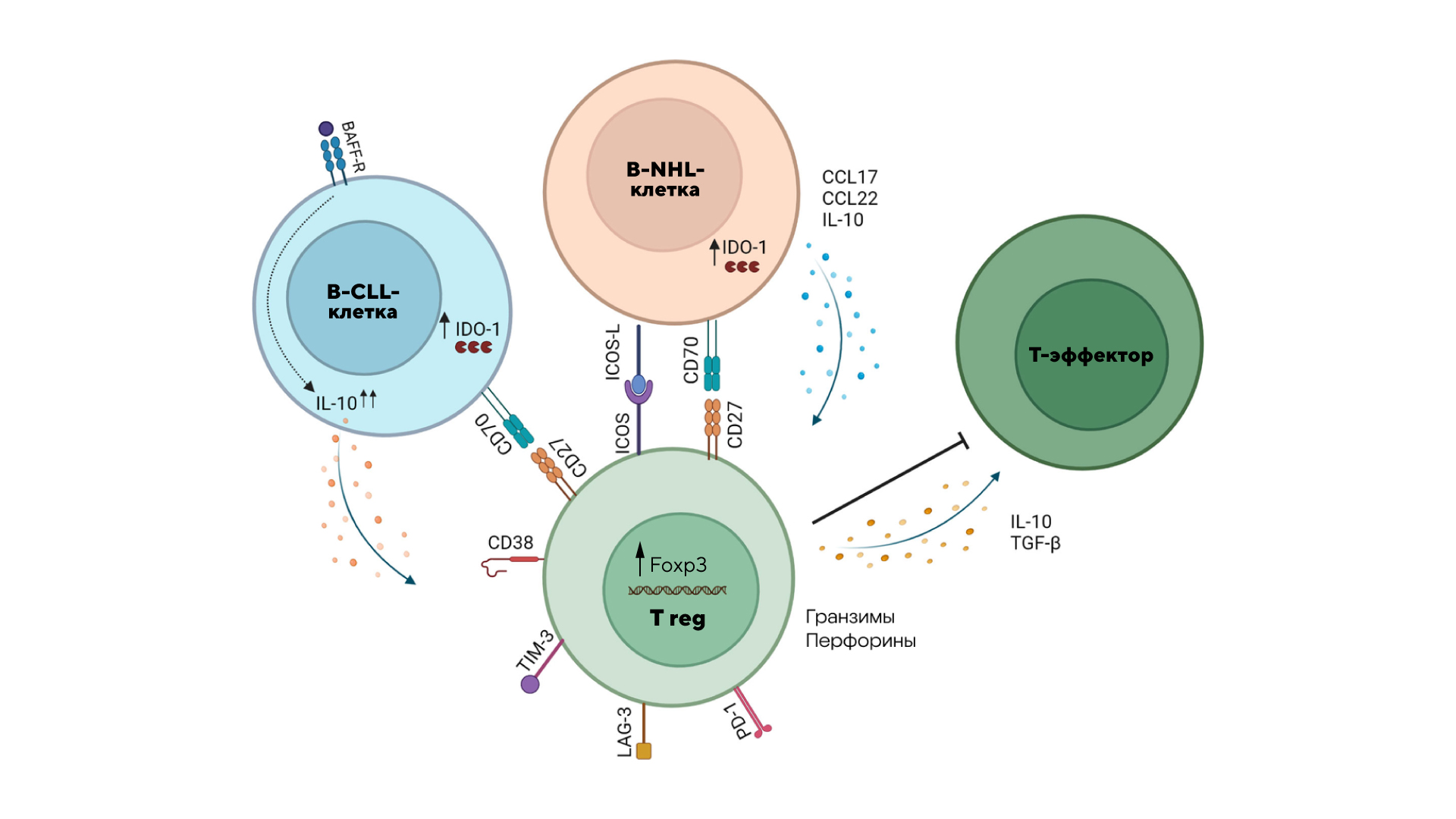
Механизмы индукции и действия Treg-лимфоцитов в микроокружении B-клеточной неходжкинской лимфомы (B-NHL). Лимфоциты B-NHL и клетки хронического лимфоцитарного лейкоза (CLL) могут индуцировать Treg-лимфоциты посредством прямого контакта с Т-лимфоцитами в микроокружении опухоли. В этих случаях Treg-клетки могут подавлять иммунный ответ посредством секреции IL-10 и TGF-β или путем уничтожения эффекторных Т-лимфоцитов посредством высвобождения гранзимов и перфоринов. Источник: адаптировано из Frontiers in Immunology