Адаптивный дизайн клинических исследований. Ускорить разработку препарата без потери качества данных
Рассказываем, зачем нужен адаптивный дизайн в клинических исследованиях (КИ) и как он помогает сделать препараты доступными для пациентов. Приготовьтесь, это настоящий лонгрид. Запаситесь терпением и чашечкой чая. Скучно не будет.
Сколько нужно времени, чтобы разработать лекарственный препарат? Дуксин Сан, декан Мичиганского университета, в своей аналитической статье говорит, что в среднем процесс занимает 10–15 лет1. При этом на создание лекарственного вещества уходит лишь треть времени и денег. Бо́льшая часть ресурсов ученых тратится на испытание препарата в клинических исследованиях2.
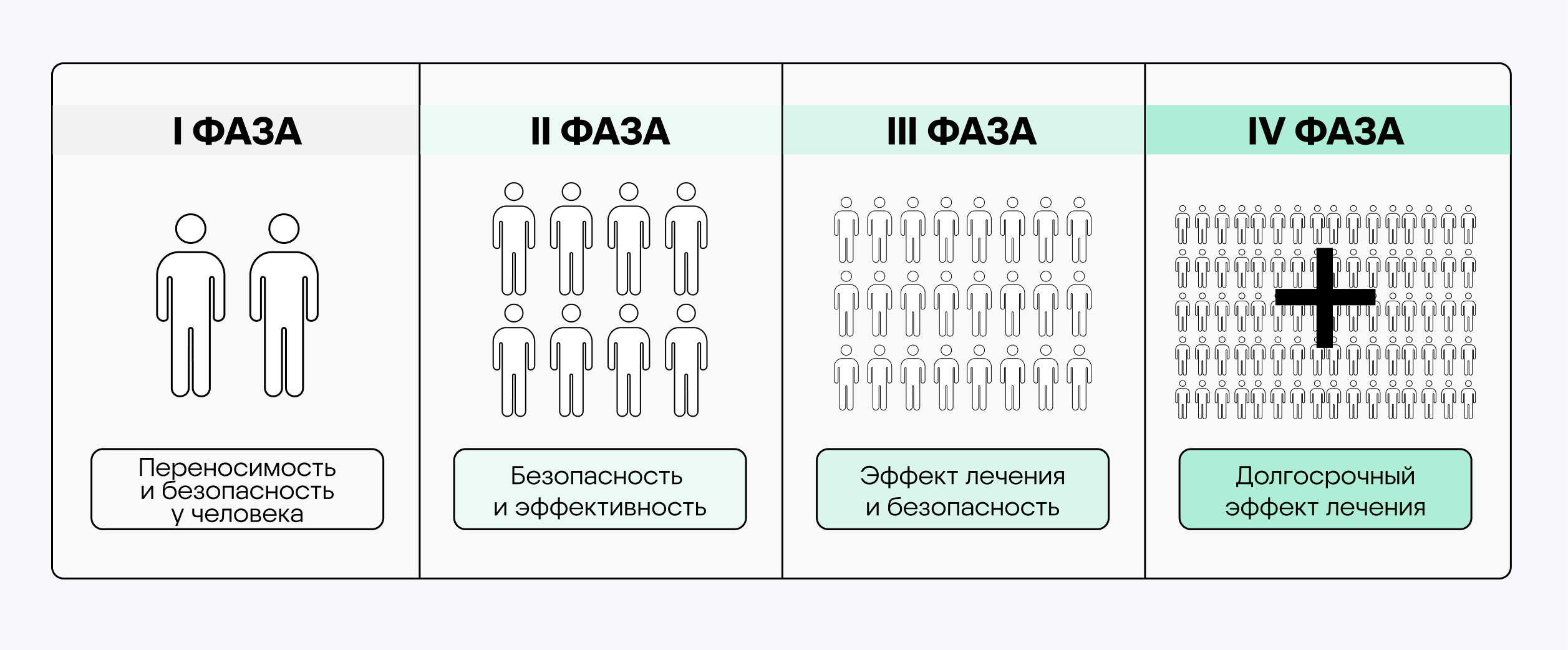
Чтобы понять, как препарат работает, насколько безопасно его применение у человека, какое его реальное влияние на заболевание, ученые обычно проводят серию последовательных клинических исследований различных фаз:
- Фаза I. Первое введение препарата небольшой группе здоровых добровольцев или пациентов для оценки его безопасности, определения дозировки и изучения фармакокинетики (как препарат ведет себя в организме).
- Фаза II. Исследование на пациентах для оценки безопасности препарата и проверки действия на заболевание.
- Фаза III. Масштабные исследования на большом количестве пациентов для подтверждения эффективности препарата, оценки побочных эффектов и сравнения с уже существующими методами лечения.
- Фаза IV (пострегистрационное исследование). Наблюдение за безопасностью и эффективностью препарата в реальной практике после его выхода на рынок. Не является обязательным для регистрации, но помогает врачам понять эффекты препарата при длительном применении, выявить редкие нежелательные явления и т. д.3
Чтобы провести качественное клиническое исследование, фармацевтические компании инвестируют огромные деньги и время. Из-за этого пациентам приходится годами ждать препараты, которые могли бы спасти им жизнь. В 2018 году управление по надзору за качеством пищевых продуктов и медикаментов США (FDA) рекомендовало исследователям и фармацевтическим компаниям использовать адаптивный дизайн для ускорения разработки препаратов и снижения их конечной стоимости4.
Дизайн классического клинического исследования
Дизайн клинического исследования — это детально разработанный план, который описывает, как будет проведено исследование: сколько в нем будет участников, как они будут отбираться, получать препарат, как будет измеряться эффект и т. д.5 Дизайн испытаний, проводимых в России, подробно описан в официальном документе — протоколе клинического исследования, который проверяется и согласовывается в этическом комитете и Министерстве здравоохранения6. В дальнейшем все исследователи проводят работу строго по протоколу, любое отклонение от него считается нарушением.
В классическом дизайне все параметры исследования определены до его начала7. Ученые рассчитывают, сколько пациентов должно участвовать, в какой дозе принимать препарат, как долго должно длиться исследование. При необходимости изменений их нужно согласовать с регулирующими органами, в России это этические комитеты и Министерство здравоохранения.
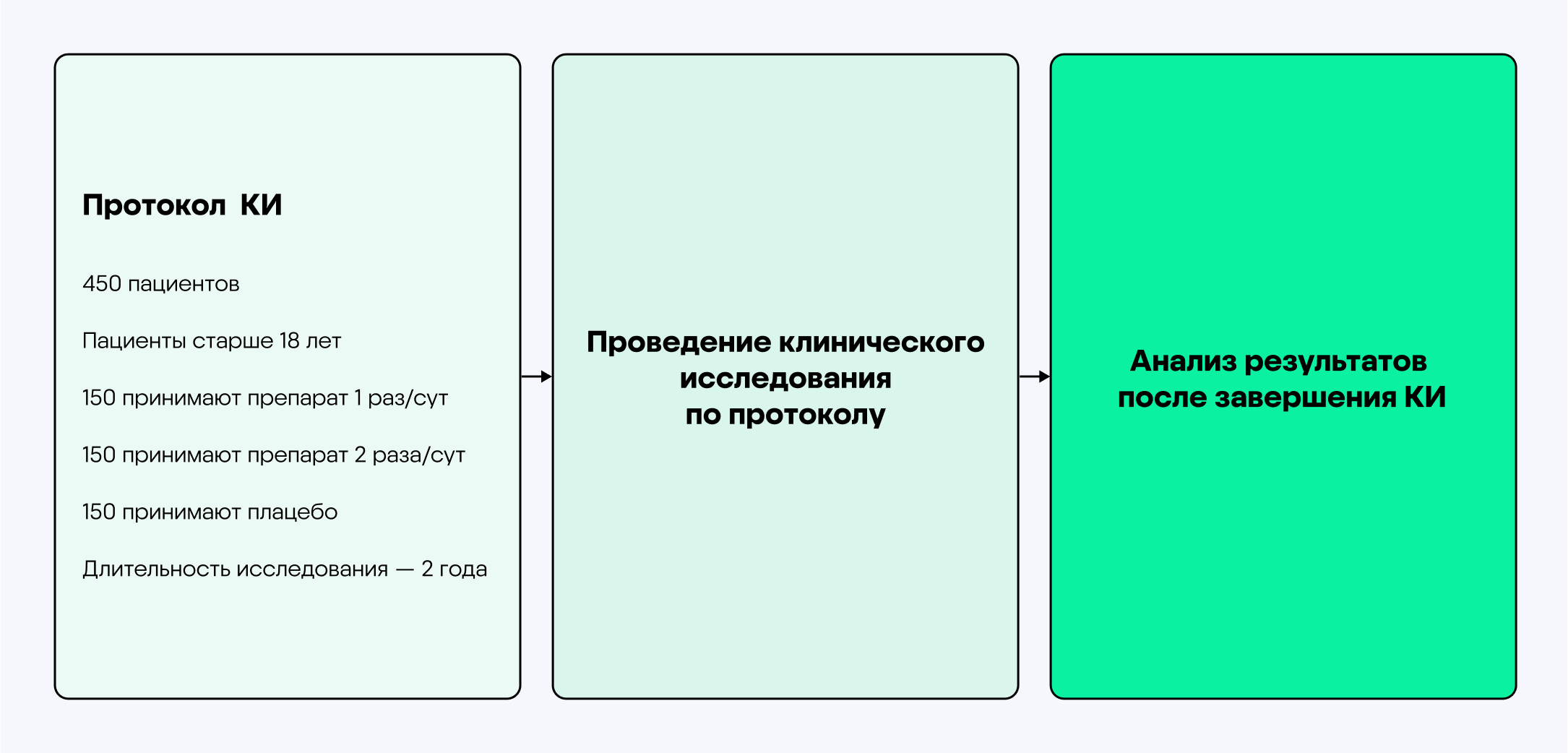
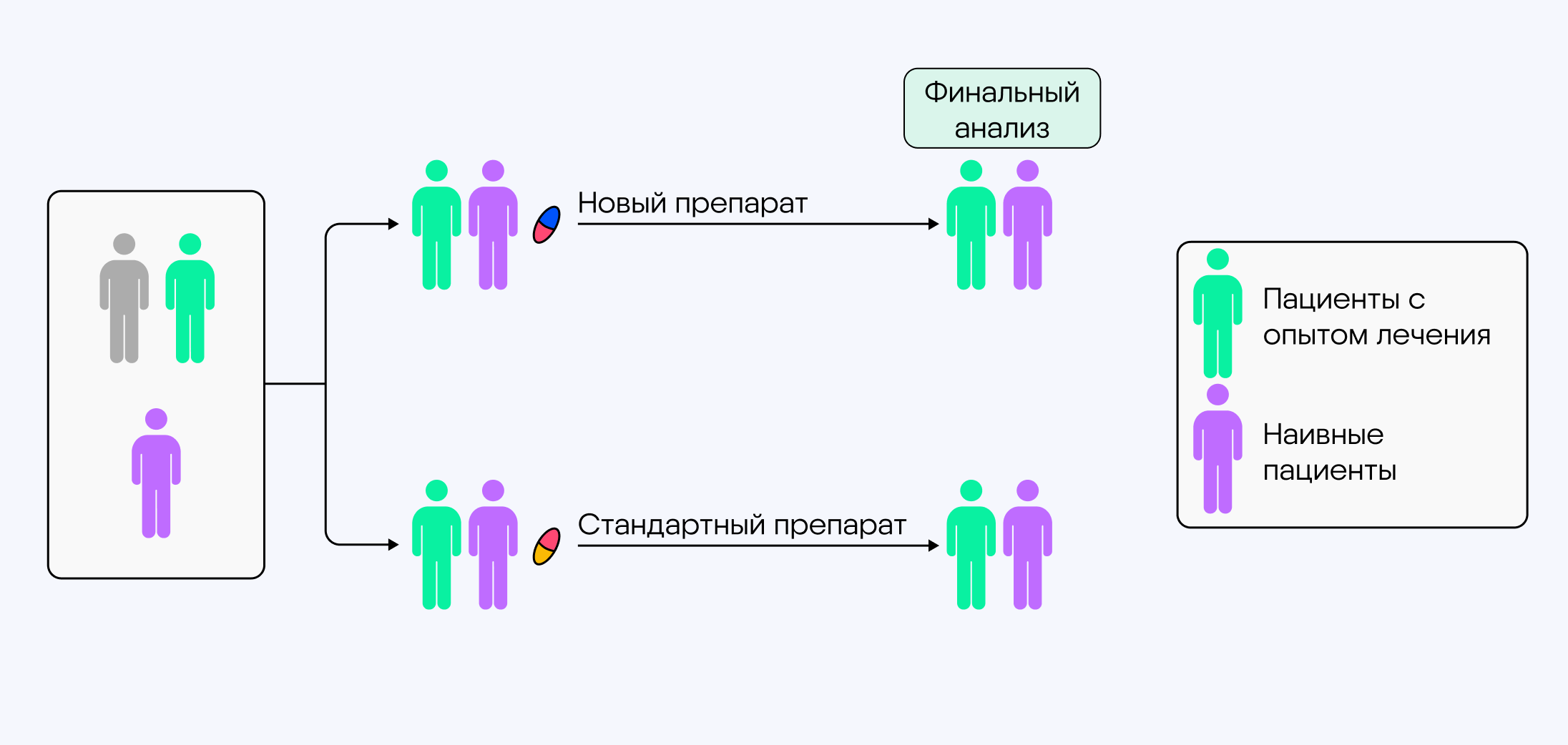
Рис. Схема традиционного дизайна клинического исследования7
Планирование классического клинического исследования можно сравнить с отправкой письма по почте. Вы пишете текст, кладете лист в конверт, пишете адрес, имя получателя, индекс. Вы все проверили и положили его в почтовый ящик. С этого момента уже ничего нельзя поменять, остается только ждать, что письмо дойдет по адресу и вы получите ответ. Но через неделю вы узнаёте, что ваш друг переехал из Москвы во Владивосток, просто забыл вам сказать об этом. И вам не остается ничего больше, как начать все заново: снова писать текст, клеить марки и отправлять по новому адресу.
Во время проведения клинического исследования нового препарата множество факторов будут влиять на его результаты. Уже после завершения многолетней работы может оказаться, что данные неубедительны из-за неправильно рассчитанного количества участников или из-за большого количества нежелательных эффектов, вызванных выбором слишком высокой дозировки.
Такие проблемы бывает сложно предсказать на этапе планирования. Их нельзя исправить во время клинического исследования, и единственное, что можно сделать, — начать его сначала, внеся изменения в дизайн.
Адаптивный дизайн — водить машину с открытыми глазами
Чтобы избежать непредсказуемости, можно заложить в протокол возможность изменения дизайна клинического исследования по ходу его проведения. Такой подход называется адаптивным дизайном.
Разработчики исследования на этапе планирования определяют, в какие моменты времени будут проводиться промежуточные анализы данных, на основе которых произойдут изменения дизайна — адаптации8.
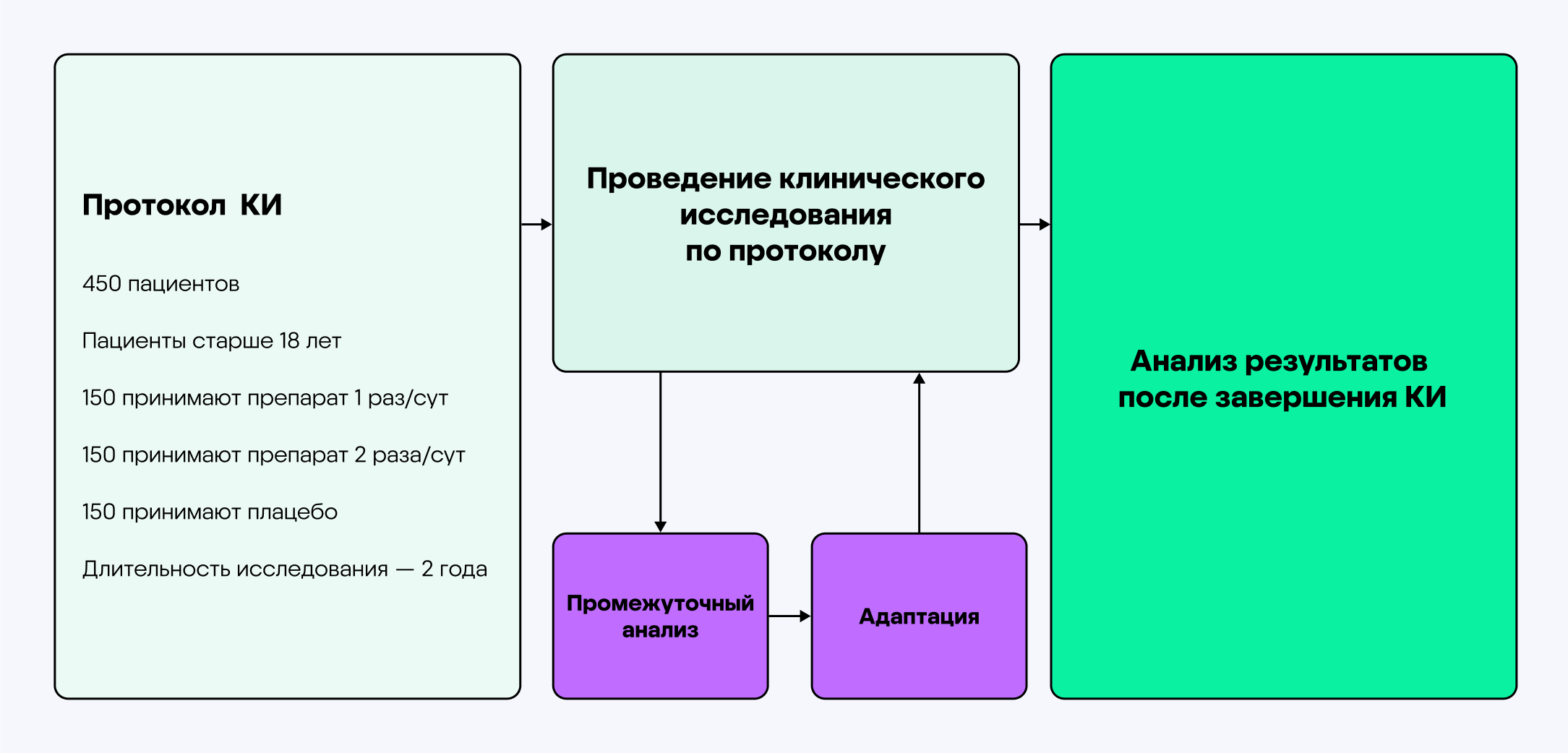
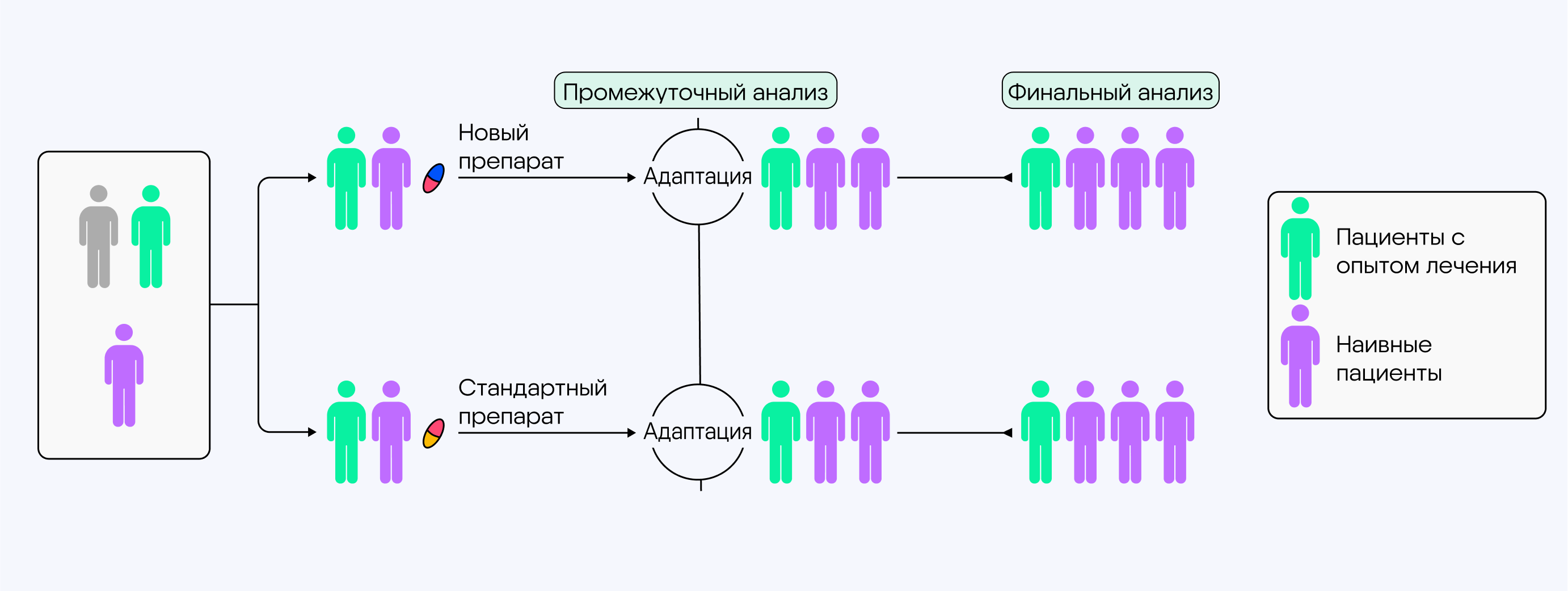
Рис. Схема адаптивного дизайна клинического исследования7
Все решения об изменениях принимаются не спонтанно, а заранее спрогнозированы и статистически рассчитаны на этапе планирования, поэтому гибкость таких исследований не нарушает достоверность будущих результатов. Давайте рассмотрим примеры исследований и возможности, которые дает адаптивный дизайн9.
Пример 1
Изменение распределения пациентов по группам
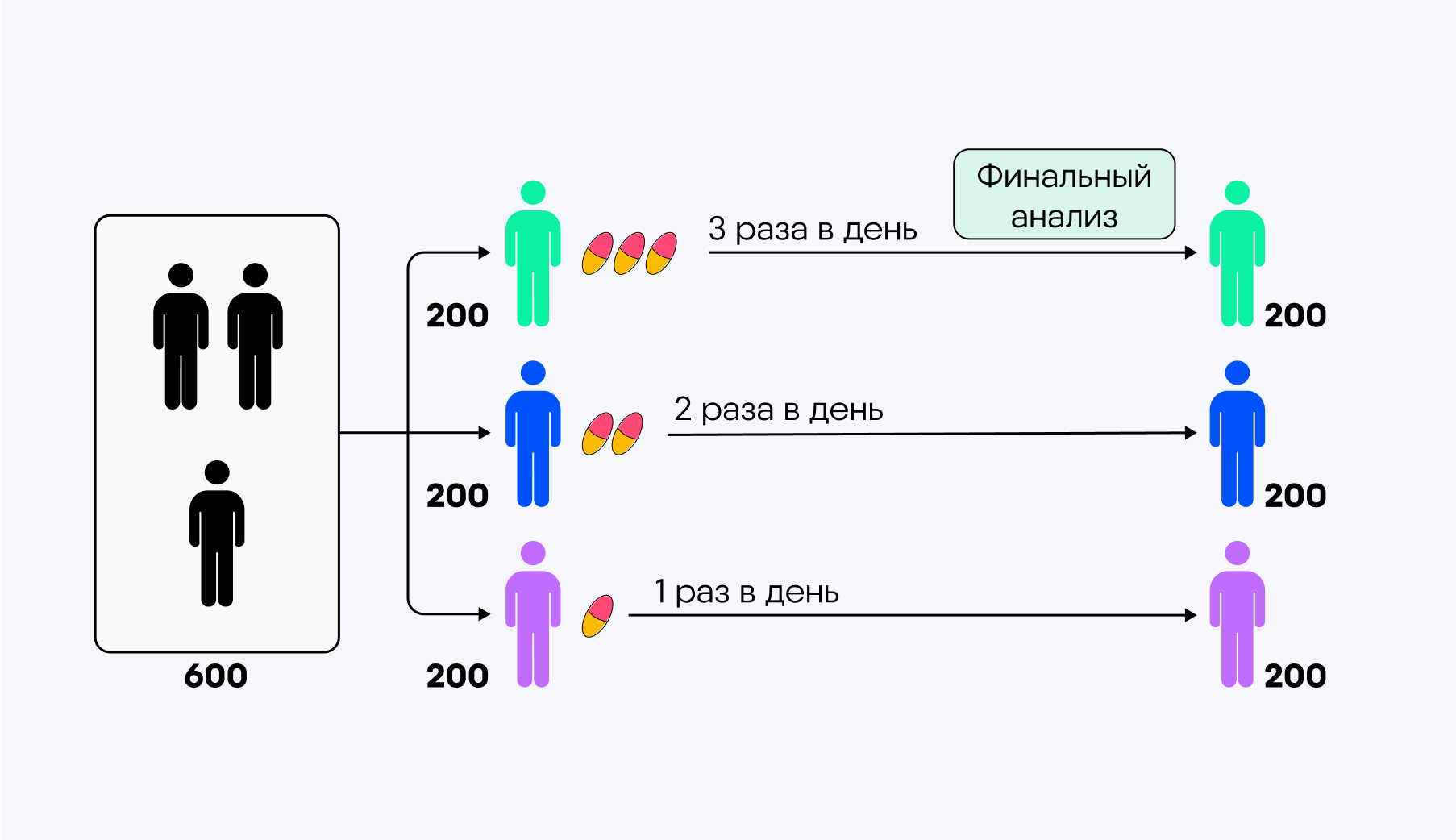
При планировании клинической разработки нового препарата для лечения злокачественного новообразования стало понятно, что у него узкий терапевтический диапазон. Это означает, что в маленькой дозе препарат неэффективен, а при небольшом повышении начинает вызывать тяжелые нежелательные реакции. Было решено протестировать разные дозировки у 600 пациентов, которых разделят (рандомизируют) на три группы в соотношении 1:1:1. В ходе исследования оказалось, что прием препарата три раза в день вызывает тяжелые побочные эффекты.
Классический дизайн
В отличие от исследований с адаптивным дизайном исследователи не предусматривают адаптации. Все 600 участников принимают запланированные дозы до конца исследования. В итоге пациенты из первой группы могут длительное время принимать излишнее количество препарата. Теоретически это может негативно влиять на состояние здоровья данной группы участников или искажать результаты исследования.
Адаптивный дизайн
Исследователи включают в протокол промежуточный анализ данных через три месяца после его начала. Этот анализ показывает, что прием препарата два раза в сутки обеспечивает оптимальное сочетание эффективности и безопасности, в то время как трехкратный прием приводит к значительному увеличению нежелательных эффектов. На основе этих данных исследователи принимают решение остановить набор участников в группу с трехкратным приемом и сосредоточиться на изучении второй группы.
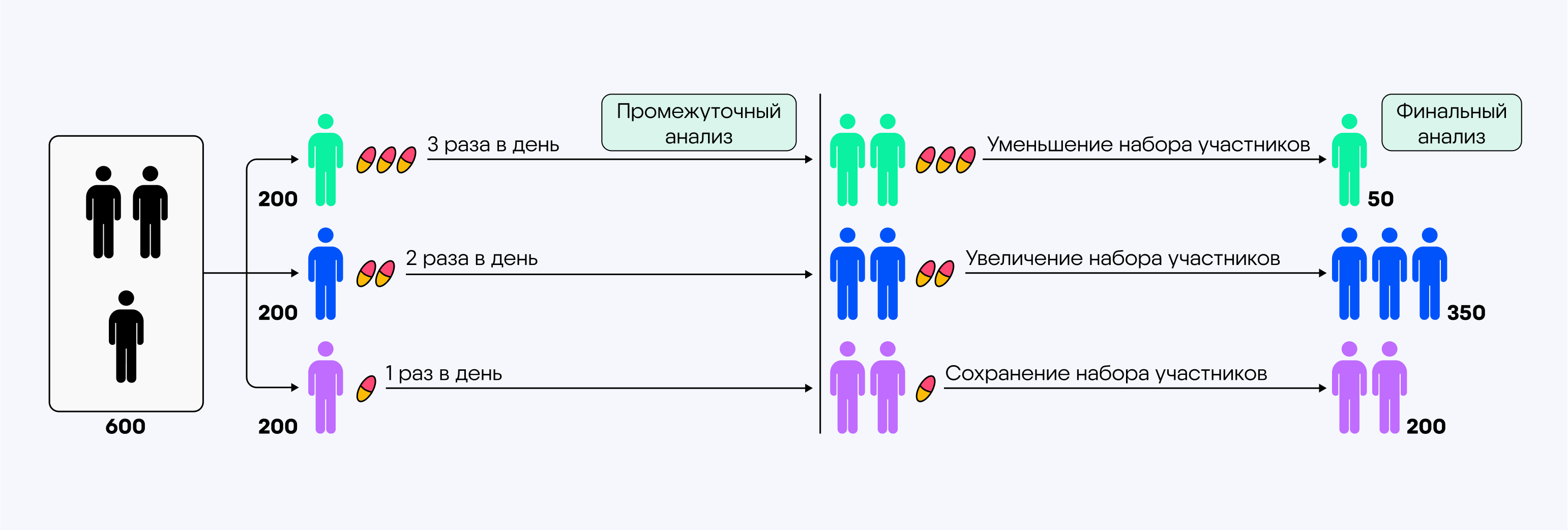
Благодаря адаптивному дизайну исследование может стать более гибким и эффективным. Сфокусировавшись на второй группе, исследователи могут быстрее собрать необходимые данные и снизить риски для участников, которые должны были получить высокую дозу.
Пример 2
Увеличение количества участников
Исследователи планируют исследование III фазы нового препарата для снижения риска инфаркта миокарда. На начальном этапе было решено, что для достижения статистически значимых результатов необходимо 200 участников. Однако со временем стало понятно, что такого числа недостаточно для демонстрации эффективности препарата по сравнению с плацебо.
Классический дизайн
Количество участников остается неизменным на протяжении всего исследования. После его завершения выясняется, что выбранного размера выборки недостаточно для подтверждения статистической мощности и, следовательно, для обеспечения достоверности результатов. Хотя врачи отметили улучшения у пациентов, статистические расчеты говорят о неэффективности препарата.
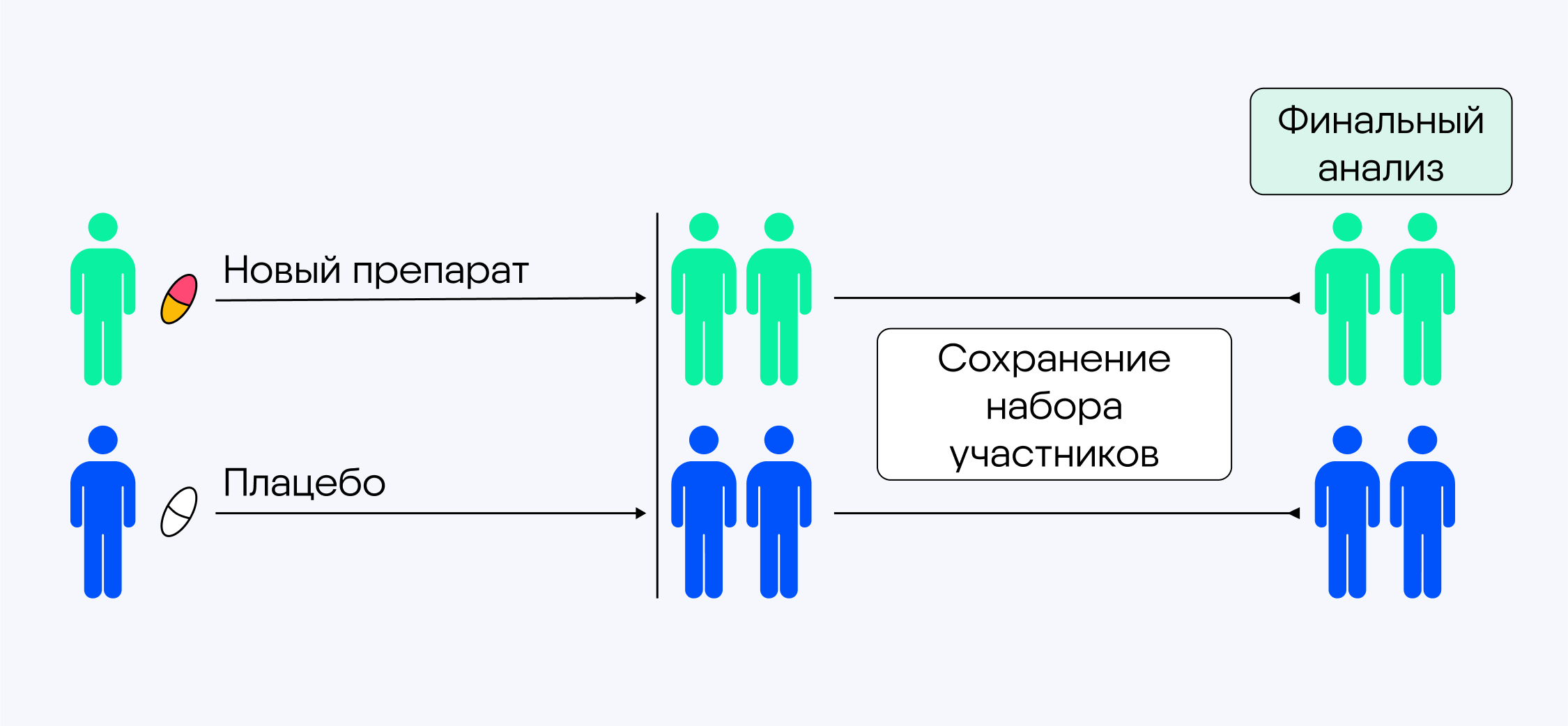
Адаптивный дизайн
Исследователи запланировали промежуточный анализ. Полученные данные говорили, что, хотя препарат эффективен, текущего количества участников недостаточно для подтверждения его преимуществ перед плацебо. Протокол исследования допускал в этом случае увеличение количества участников.
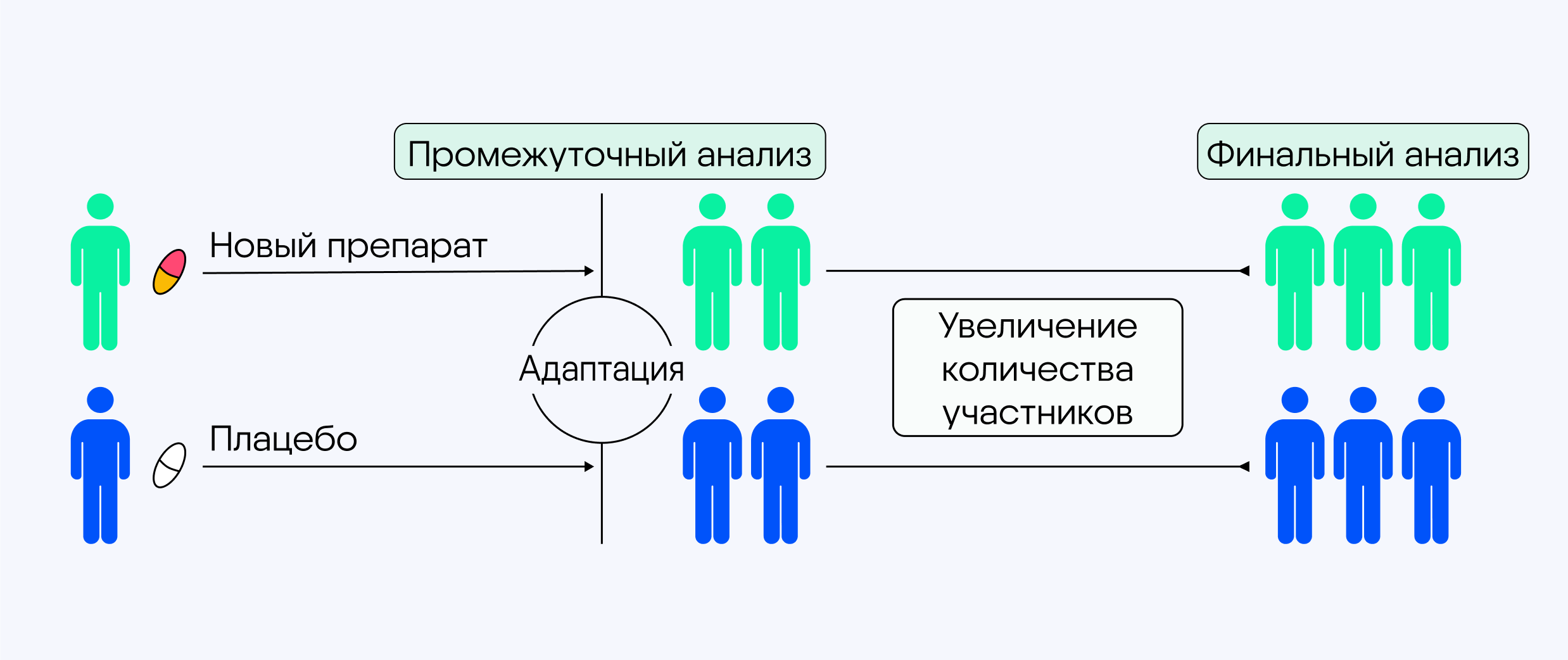
Исследователи скорректировали ход исследования, увеличив его статистическую мощность, и доказали эффективность нового препарата.
Пример 3
Обогащение групп
Ученые планируют клиническое исследование III фазы нового препарата для лечения злокачественного новообразования. Они решили разделить участников на две группы: одна получала новое лекарство, а другая — стандартное лечение. Участники были распределены таким образом, что в каждой группе было схожее количество тех, для кого это лечение было первым (наивные), и тех, кто уже принимал до этого химиотерапию. В ходе исследования оказалось, что новый препарат показывает особенно высокий результат в группе наивных пациентов.
Классический дизайн
Исследователи не меняли состав групп после начала испытания. Препарат показал незначительное увеличение продолжительности жизни по сравнению со стандартным лечением. Количество наивных пациентов оказалось недостаточным, чтобы подтвердить высокую эффективность в этой группе.
Адаптивный дизайн
После получения промежуточных данных исследователи изменили критерии включения, увеличив количество наивных пациентов в исследовании. К моменту завершения испытания было установлено, что новый препарат значительно увеличивает продолжительность жизни наивных пациентов по сравнению со стандартной терапией. Это открытие помогло изменить подходы к лечению заболевания.
Бесшовные исследования
Исследование нового препарата на людях обычно проходит поэтапно. Сначала ученые проверяют его безопасность на здоровых добровольцах или пациентах в исследованиях фазы I, затем на небольшой выборке пациентов в фазе II, а уже после этого — на большом количестве пациентов в фазе III. В классическом варианте данные, полученные в одном исследовании, используются для планирования последующих, что увеличивает время разработки.
Бесшовные исследования представляют собой пример адаптивного дизайна. В них пациенты беспрепятственно переходят из ранней фазы в позднюю, что ускоряет получение окончательных выводов о эффективности и безопасности препарата9.
Отдел клинических разработок компании BIOCAD применяет адаптивный подход при планировании клинических исследований.
«Одной из первых наших оригинальных разработок стал препарат для лечения рассеянного склероза, в котором нуждались тысячи пациентов в России. Без лекарственных препаратов заболевание прогрессирует, что может привести к инвалидности в относительно короткие сроки. Для ускорения клинических испытаний мы объединили вторую и третью фазы. Несмотря на кажущуюся простоту, разработка адаптивного дизайна является сложной задачей. Это потребовало от нас проведения тщательных статистических расчетов и обоснования целесообразности такого подхода перед Министерством здравоохранения.
В итоге в исследование в кратчайшие сроки было включено 399 пациентов, что позволило значительно ускорить процесс клинических испытаний и в конечном итоге сделать препарат доступным для пациентов».
Планирование клинических исследований
Разработка дизайна исследования — один из сложнейших этапов разработки препарата. Нужно учесть все возможные риски, сделать процесс безопасным для пациентов, обеспечить непредвзятую оценку нового препарата. В BIOCAD этим занимается Департамент клинической разработки.
«Наша главная задача — сделать так, чтобы исследование прошло без нареканий. Мы готовим пакет документов для Министерства здравоохранения, отвечаем на их запросы, готовим отчеты после завершения испытаний.
Для выполнения такой работы необходимо общее понимание медицинских вопросов, статистики, регуляторики. Нужно уметь быстро прорабатывать большое количество медицинской литературы и искать нестандартные решения. Большинство людей, которые приходят работать медицинскими экспертами, — это врачи, имеющие опыт научной работы, участия в клинических исследованиях со стороны медицинского учреждения. Так или иначе, можно сказать, что новые сотрудники часто не имеют непосредственного опыта планирования больших клинических исследований на момент начала работы. Для успеха нужно хотеть развиваться и получать новые навыки. Необходимо плотно и быстро ознакомиться с общими принципами клинической разработки, со статистикой, с международным опытом разработки препаратов.
Сейчас в компании в приоритете международная клиническая разработка. Приходится изучать требования и законы других стран, особенности проведения в них клинических исследований. И это очень интересно! Кроме того, сейчас в большинстве исследований мы стараемся применять элементы адаптивного дизайна, что ускоряет процесс разработки новых препаратов».
Использование адаптивного дизайна в клинических исследованиях сокращает время на разработку препарата, снижает риски для участников, повышает достоверность результатов7. Однако, чтобы применить его на практике, требуется большая предварительная работа, знания в статистике, оценка рисков, согласование с регуляторными органами. И мы в BIOCAD делаем это, чтобы наши препараты начали работать для пациентов как можно скорее.
