Сворачиваем и разворачиваем белки: за что вручили Нобелевскую премию по химии — 2024
Множество процессов в нашем организме — от переваривания пищи до деления клеток — происходят благодаря белкам. То, какую именно работу будет выполнять белок, определяет его структура. Если научиться собирать белки с заданной структурой, можно решать биологические задачи — например, как свернуть терапевтический белок для его связывания с конкретной мишенью в организме. О том, какие перспективы открывает проектирование белков «под заказ», в чем проблема сворачивания белков и за что вручили Нобелевскую премию по химии в 2024 году, обсудили на Guest Club в Санкт-Петербурге.
Нобелевскую премию по химии часто вручают не за чисто химические исследования, а за открытия, тесно связанные с биологией и медициной. В разные годы премией награждали за разработку методов CRISPR/Cas9 и фагового дисплея, а также за открытие деградации белков с помощью убиквитина и исследование механизма транскрипции у эукариот. Однако лауреатами премии 2024 года стали даже не биологи, а айтишники — Дэвид Бейкер из США, Демис Хассабис и Джон Джампер из Великобритании. Награду присудили за компьютерный дизайн белков и предсказание их трехмерной структуры. О перспективах развития вычислительной биологии, проблемах фолдинга белка и дизайне молекул поговорили на открытом обсуждении Нобелевки с вице-президентом по R&D BIOCAD Павлом Яковлевым и главным редактором портала «Биомолекула», старшим научным сотрудником ИБХ РАН Антоном Чугуновым. Модератором дискуссии выступила Анна Владимирова, директор Департамента научного развития компании BIOCAD.
Белки с разных сторон: за что вручили Нобелевскую премию
Одну часть Нобелевской премии по химии 2024 года вручили американскому биохимику Дэвиду Бейкеру «за дизайн новых белков». Вторую — английским исследователям Демису Хассабису и Джону Джамперу из компании Google DeepMind — «за предсказание 3D-структуры белка». Оба достижения тесно связаны между собой, несмотря на противоположные подходы: Дэвид Бейкер создал алгоритм Rosetta, который по 3D-структуре белка может спроектировать нужную аминокислотную последовательность, а Хассабис и Джампер разработали нейросеть AlphaFold, которая, наоборот, на основе последовательности предсказывает строение белка. Но общий вывод один — премию вручили за решение физической задачи (связь последовательности и структуры белка) нефизическими методами (статистическими или машинным обучением).
Проблема фолдинга: зачем сворачивать белки
В молекулярной биофизике существует понятие «фолдинг белка» (folding — сворачивание, укладка). Белки — биополимеры, которые свернуты в сложную трехмерную структуру. Информация о том, как именно им удается принять ту или иную конформацию, заложена в аминокислотной последовательности — это открыли еще в 1961 году.
Сворачивание (фолдинг) белка — это протяженный по времени процесс превращения цепочки аминокислот в пространственную белковую структуру. А то, чем занимается команда DeepMind, — это protein structure prediction, то есть предсказание по аминокислотной последовательности только финальной структуры, без учета всего промежуточного процесса.
Однако проблему фолдинга белка решили лишь отчасти. За что же тогда дали Нобелевскую премию в 2024 году? Прорыв Дэвида Бейкера и его команды заключался в разработке программы Rosetta, которая позволяет моделировать структуру белков, пусть даже это срабатывает не всегда и только для небольших белков. Команда Бейкера не углублялась в физику, не стремилась минимизировать потенциальную энергию, а просто подобрала похожие белки, порезала их на кусочки и научила программу сопоставлять эти фрагменты.
Rosetta и AlphaFold: дизайн vs структура
Rosetta — программа, которая помогает создавать белки с заранее выбранными функциями. Принцип работы Rosetta, разработанной в Институте белкового дизайна под руководством Дэвида Бейкера, основан на предложении возможных вариантов укладки белка. Если сильно упрощать, то Rosetta «режет» белок на множество фрагментов, ищет в базе данных похожие фрагменты с известной структурой и собирает из кусочков белок с заданными свойствами.
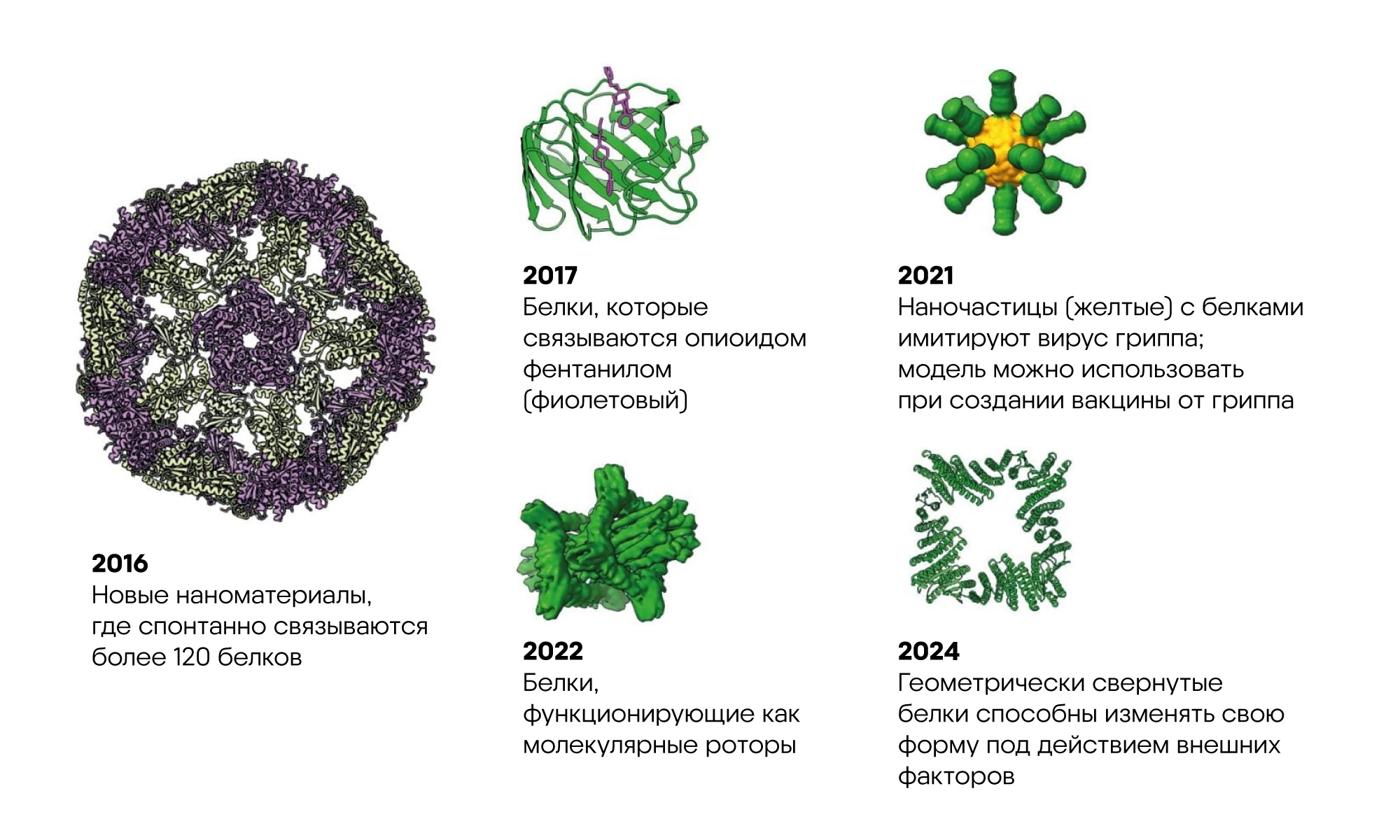
Белки, разработанные с использованием программы Rosetta
AlphaFold — нейросеть для предсказания 3D-структуры белка по аминокислотной последовательности. В ее основе — алгоритм, обученный на базе данных белковых структур. Успех компании DeepMind — в подключении метагеномики на службу предсказания белков.
По сути, AlphaFold просчитывает огромное количество всех уже секвенированных последовательностей (а их в нейросеть загружено более 2,5 млрд), для того чтобы выбрать оптимальные 3D-структуры.
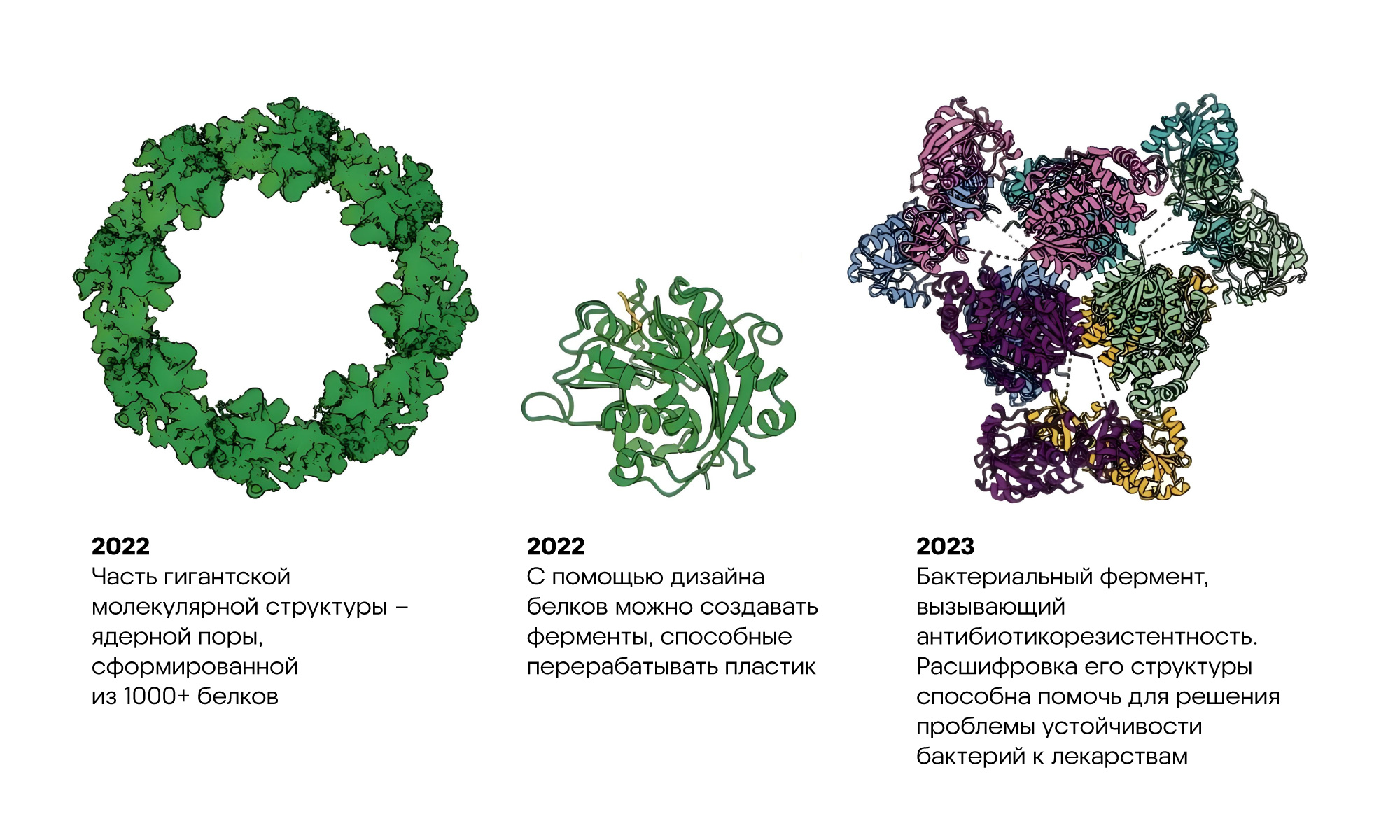
Структуры белков, предсказанные с помощью AlphaFold
Оба подхода — и Бейкера, и Джампера с Хассабисом — роднит то, что они не пытались воспроизвести физику поведения белковых молекул, а пошли другим путем, от наблюдений. Поэтому разработки компании DeepMind — это естественное продолжение проекта Бейкера, который он начал задолго до AlphaFold.
Быстрое предсказание структуры белка раскрывает большие перспективы для медицины, чтобы собирать белки с нужными свойствами. Объясним на примере. Японская компания Chugai Pharmaceutical Co. разработала биспецифическое антитело эмицизумаб против гемофилии А. У людей с этой болезнью нарушен процесс свертываемости крови из-за отсутствия одного из компонентов — фактора VIIIа (FVIIIа). Свертываемость — многоступенчатый процесс, и в норме FVIII связывает между собой два других фактора — FIXа и FX. Чтобы «подружить» между собой FIXа и FX у людей с гемофилией, в Chugai разработали «мостик» — биспецифическое антитело, которое работает как FVIIIа. Связать каждый из двух белков не так сложно, а вот правильно их приблизить — это задача нетривиальная. В этом помогли как раз знания о структуре белка. Но нельзя сказать, что это было просто: пришлось повторить процедуру подбора нужных белковых кусочков и внесения в них мутаций более 1 200 раз, а ушло на это 16 лет!
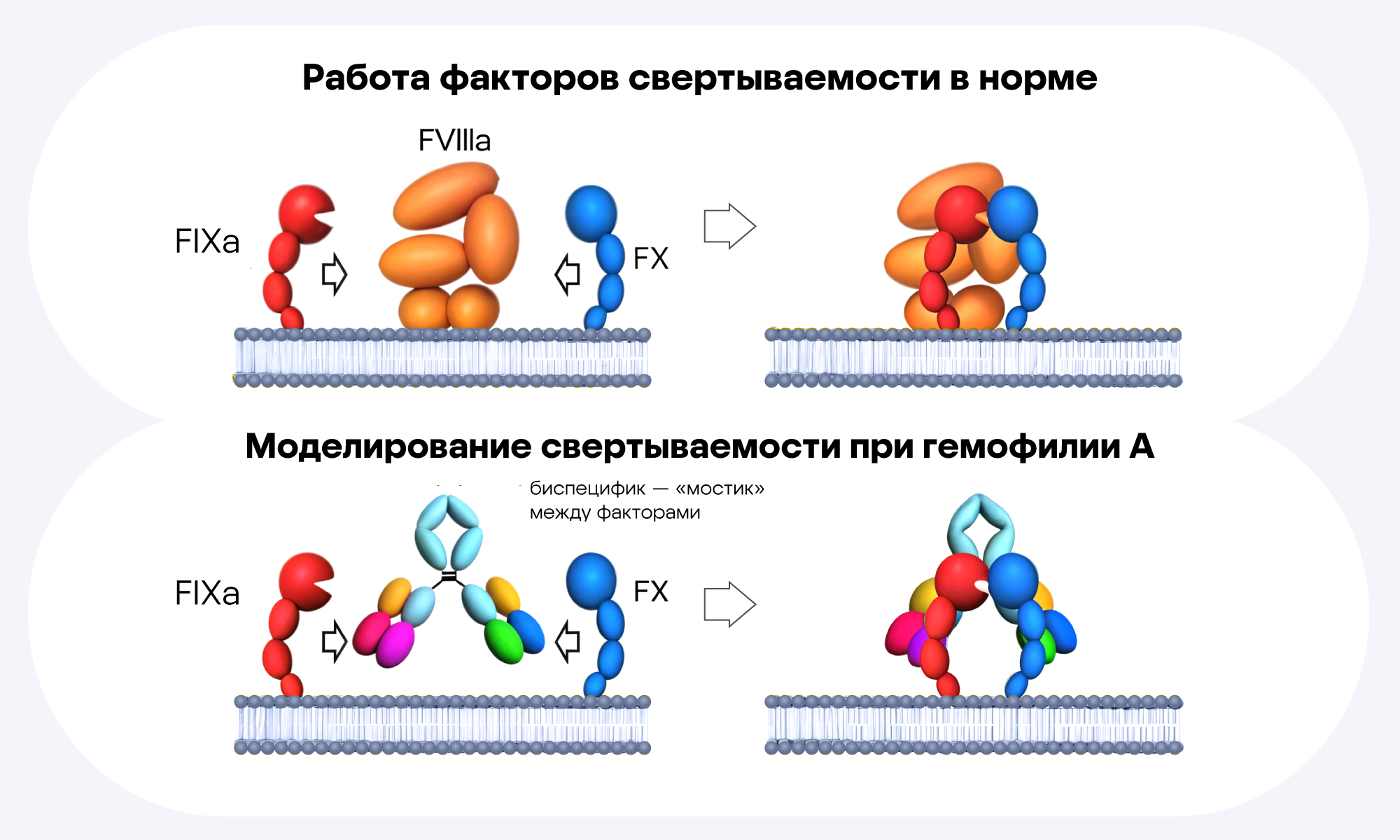
Чтобы связать факторы IX и X, разработали биспецифическое антитело: эпитоп на одной «руке» узнает FIXa, а эпитоп на другой — FX. Источник: адаптировано из ASCLS
Первый белковый дизайн
Если ориентироваться на присуждение Нобелевской премии Дэвиду Бейкеру, то именно его следует назвать первым «белковым дизайнером». Действительно, в 2003 году его команда опубликовала дизайн нового белка Top7, структура и последовательность которого не содержались ни в одной из существующих баз данных. Однако Бейкера вряд ли можно считать первопроходцем, создавшим дизайн нового белка. Еще в 1997 году появился белок 1FSD — 1st Full Sequence Design. Его создатели — два исследователя, которые взяли структурный белковый мотив zinc finger и создали точно такой же белок, но с совершенно иной аминокислотной последовательностью.
Белковый дизайн помогает нам создавать белки, которых не существует в природе, под свои задачи.

Тот самый первый задизайненный белок 1FSD
Однако формально и этот белок нельзя считать первым. Еще в 1992 году структурщики из Пущино сделали первый белковый дизайн альбебетина. Они решили использовать не природную структуру, а сконструировали ген и синтезировали белок «на глаз» — и у них получилось. По крайней мере, если сравнивать модель из Пущино и модель от AlphaFold, они примерно совпадают.

Так вот, с помощью современной версии AlphaFold такие задачи решить невозможно: из-за слишком высокой вариабельности структур у японской компании Chugai или из-за уникальности разрабатываемого белка, не имеющего природных аналогов.
Кто не получил Нобелевку?
Если судить по лауреатам Нобелевской премии 2024 года, то и в химии, и в физике победителями стали люди, далекие от этих наук. Среди тех, кто премию пока не получал, — Уильям Йоргенсен, пионер в области вычислительной химии, который придумал силовое поле OPLS и внес наибольший вклад в теорию возмущений свободной энергии. Оба этих результата активно используют каждый день биоинформатики в Департаменте вычислительной биологии BIOCAD: они позволяют предсказывать, на что повлияет та или иная мутация в белке. Йоргенсена включают в список потенциальных лауреатов премии еще с конца 1990-х, но награду он до сих пор так и не получил. Возможно, это связано с тем, что Нобелевскую премию дают за результат, а не за способ его достижения.
Для предсказания пространственной структуры белка ab initio используют метод силовых полей, основанный на расчете энергии. OPLS — не единственное силовое поле, которое позволяет имитировать сворачивание белка. Например, в Rosetta используется поле REF2015
Черри-пикинг для создания репутации
Если оценивать хронологию после дизайна первого белка командой Дэвида Бейкера в 2003 году, кажется, что все научные лаборатории уже давно должны заниматься дизайном белков исключительно с помощью вычислительных методов. Однако этого не происходит, и белки создают по старинке. Почему же лаборатории и фармкомпании продолжают тратить огромное количество денег, вместо того чтобы просто запустить компьютерную программу? Причина в том, что Дэвид Бейкер публикует отнюдь не все свои результаты.
В Git есть команда git cherry-pick — это когда мы вносим выборочные изменения в текущую ветку проекта. Что-то вроде черри-пикинга, или выборочного представления фактов, делает и команда Бейкера — они публикуют только то, что хорошо получилось. На самом же деле на работу по дизайну белков тратится огромное количество ресурсов, но успех приходит далеко не всегда.
Однако, несмотря на неудачи в вопросе решения фолдинга белка, и Rosetta, и AlphaFold открывают огромные перспективы для развития науки и технологий. Возможно, спустя время дизайн терапевтических молекул и предсказание связывания лекарств с мишенями будут решаться не человеком, а машинами.