
Мифы о раке. Часть II: разбираемся в нюансах терапии
Онкологические заболевания являются одной из лидирующих причин смерти в мире — так, по данным Всемирной организации здравоохранения, в 2022 году на планете было зарегистрировано 20 млн новых случаев возникновения злокачественных новообразований. Сложность лечения этой группы болезней в том, что на сегодняшний день нет средств, которые бы со стопроцентной вероятностью избавляли бы людей от онкологических заболеваний. Одним из перспективных способов борьбы со злокачественными новообразованиями считается иммунотерапия. Разработкой инновационных препаратов на основе терапевтических антител, способных помогать иммунитету бороться с болезнью, занимаются в том числе и в компании BIOCAD. Но этим в компании не ограничиваются и занимаются модернизацией тактик лекарственной помощи, включая сопроводительное лечение при химиотерапии.
Чтобы развеять возможные мифы о перспективах лечения рака, мы решили ответить на самые популярные вопросы наших читателей. В первой части статьи мы уже рассказали о предпосылках возникновения онкологических заболеваний и особенностях инновационной терапии. Во второй части статьи предлагаем разобраться с вопросами диагностики и с перспективами лечения злокачественных новообразований.
Снижают ли ПИТРС, например Ивлизи®, риск развития злокачественного заболевания?
Так ли это? Неизвестно.
Что известно? Подробных исследований, которые явно подтверждают взаимосвязь между частотой возникновения злокачественного новообразования и приемом препаратов, изменяющих течение рассеянного склероза, не проводилось. Однако такие препараты действительно влияют на работу иммунной системы и способны опосредованно выключать или удалять неправильно работающие клетки, которые потенциально могут переродиться в опухолевые. Если оценивать взаимосвязь между злокачественными новообразованиями и ПИТРС по исследованиям, которые проводили для некоторых препаратов, можно заключить: как правило, они не влияют на развитие заболевания.
При проведении клинических исследований Ивлизи® (МНН дивозилимаб) также не был обнаружен риск развития злокачественных новообразований во время терапии этим препаратом. Однако тем людям, у которых в настоящий момент или в прошлом диагностировано онкологическое заболевание, врач может отложить лечение с помощью Ивлизи®.
Чтобы лучше разобраться в том, откуда могла возникнуть мысль о возможной связи между применением ПИТРС и подавлением злокачественного новообразования, давайте посмотрим на механизм действия антитела против CD20. Именно эта молекула стала основой препарата Ивлизи® для терапии рассеянного склероза. Молекула CD20 очень часто встречается на поверхности патогенных клеток, которые появляются в организме не только при рассеянном склерозе, но и при В-клеточных неходжкинских лимфомах, хроническом лимфолейкозе, системной красной волчанке, сахарном диабете 1-го типа. Принцип действия Ивлизи® основан на связывании этого антитела с белком CD20 на поверхности В-лимфоцитов, которые отвечают за развитие рассеянного склероза. Однако анти-CD20 также потенциально могут запускать и другие иммунологические реакции, например, делая В-клеточную лимфому более уязвимой для лечения. Возможно, это и стало причиной возникновения идеи о том, что препараты, изменяющие течение рассеянного склероза, могут также угнетать процессы опухолевого патогенеза.
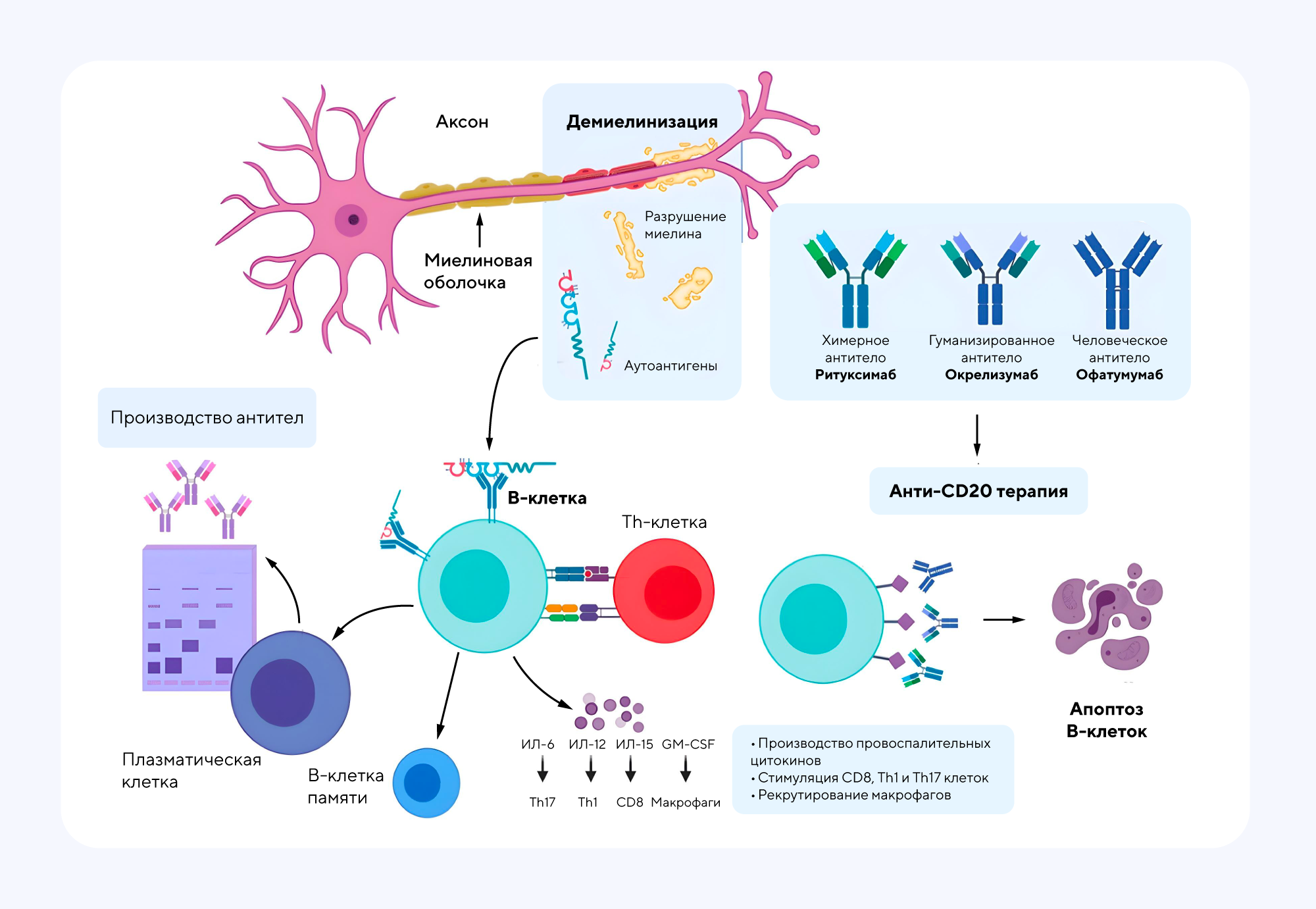
Против CD20 разработаны несколько антител, в том числе ритуксимаб (противоопухолевое и иммуномодулирующее средство), окрелизумаб (препарат для лечения рассеянного склероза) и офатумумаб (препарат для лечения хронического лимфоцитарного лейкоза). Источник: адаптировано на основе MDPI
Правда ли, что витамины группы В провоцируют рост опухоли?
Так ли это? Отчасти да.
Как на самом деле? Обычно витамины ассоциируются с чем-то однозначно положительным и уж точно безвредным. Но в случае если речь идет об онкологических заболеваниях, прием витаминов важно обсуждать с лечащим врачом. Дело в том, что за последние несколько лет накопились данные, которые косвенно подтверждают взаимосвязь между приемом конкретных групп витаминов и увеличением риска развития некоторых видов злокачественных новообразований. В их числе — витамины группы В, в частности фолиевая кислота (В9), метилкобаламин (В12), тиамин (В1), пиридоксин (В6). Причина, по которой следует ограничить их прием, в том, что витамины группы В — впрочем как и любые другие жизненно необходимые для клетки элементы, — помимо других своих функций, также способны активировать рост клеток. Проблемой может стать то, что запускается рост любых клеток — и нормальных, и поломанных, а значит, витамины группы В могут быть невольными «сподвижниками» разрастания опухоли. Поэтому принимать эти витамины не рекомендуется на протяжении цикла химиотерапии, чтобы снизить риски возникновения рецидива. Впрочем, убедительных и надежных доказательств, которые явно подтверждают связь между витаминами и осложнениями онкологических процессов, пока что нет — и в каждом случае решение о назначении тех или иных биологических добавок принимается лечащим врачом.
Запрещены ли при раке массажи, баня и загорание?
Так ли это? Не совсем.
Как на самом деле? Обычно при любых разновидностях злокачественных новообразований, особенно с метастазированием, не рекомендуется ходить в баню и на массаж без предварительной консультации с лечащим врачом. Это ограничение связано с тем, что такие процедуры ускоряют кровообращение, что повышает риск увеличения уже существующей опухоли и может способствовать ее метастазированию. Однако однозначный запрет на массаж и посещение бани уже несколько устарел. В некоторых случаях и после согласования с лечащим врачом общеукрепляющий массаж, наоборот, назначают, чтобы расслабить мышцы и снять боли в разных частях тела. Так, анализ результатов исследований среди онкопациентов показал скорее положительное влияние массажа для облегчения состояния.
Похожая история была и с запретом на бани и сауны: до недавнего времени существовал строгий запрет на их посещение у людей с онкологическими заболеваниями, в том числе в период ремиссии. Считалось, что высокая температура однозначно плохо влияет на опухоли, способствуя распространению раковых клеток. Однако сейчас, наоборот, накопились подтверждения того, что температура выше 40 градусов повышает чувствительность опухолей, делая их более уязвимыми для лечения. На этом свойстве основан подход HIPEC — гипертермической интраперитонеальной терапии, которую применяют для лечения органов брюшной полости.
А вот с загаром все сложнее. Ультрафиолетовое излучение — один из самых мощных травмирующих факторов, которые могут повредить ДНК и привести к образованию мутаций. Нахождения под прямыми солнечными лучами следует избегать даже здоровым людям, не говоря уже о пациентах с диагностированным онкологическим заболеванием. Особенно актуально это в период проведения химиотерапии, которая и так повышает чувствительность кожи.
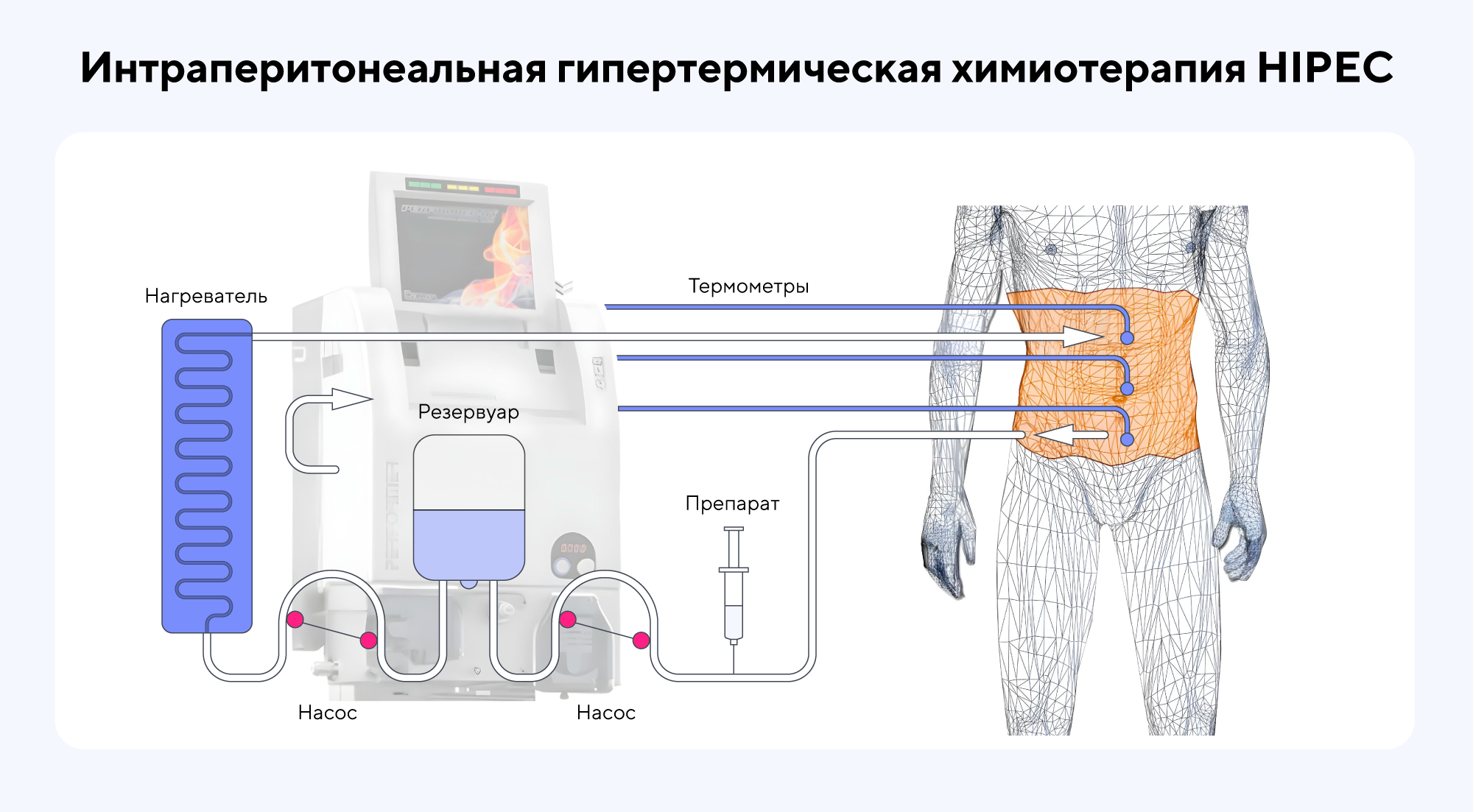
Терапию HIPEC проводят, в частности, для лечения злокачественных опухолей ЖКТ: тонкой и толстой кишки, прямой кишки, опухолей брюшины, желудка и т. д. Для этого в брюшную полость вводят раствор противоопухолевого препарата, который имеет температуру 42–43°С. Через определенное время препарат обратно аспирируют («забирают» при помощи вакуума)
Может ли метотрексат спровоцировать образование меланомы?
Так ли это? В абсолютном отношении — скорее нет.
Как на самом деле? Метотрексат — препарат из группы цитостатиков, который подавляет иммунную систему. Благодаря этому свойству его используют для лечения аутоиммунных заболеваний, например при псориазе или ревматоидном артрите. Но этим показания к применению метотрексата не ограничиваются: из-за своей способности тормозить клеточное деление к этому препарату чувствительны быстро делящиеся онкологические клетки. Поэтому метотрексат также применяют при терапии острого лимфобластного лейкоза, неходжкинских лимфом и других видов злокачественных новообразований трофобластических опухолей, раке шейки матки и раке пищевода.
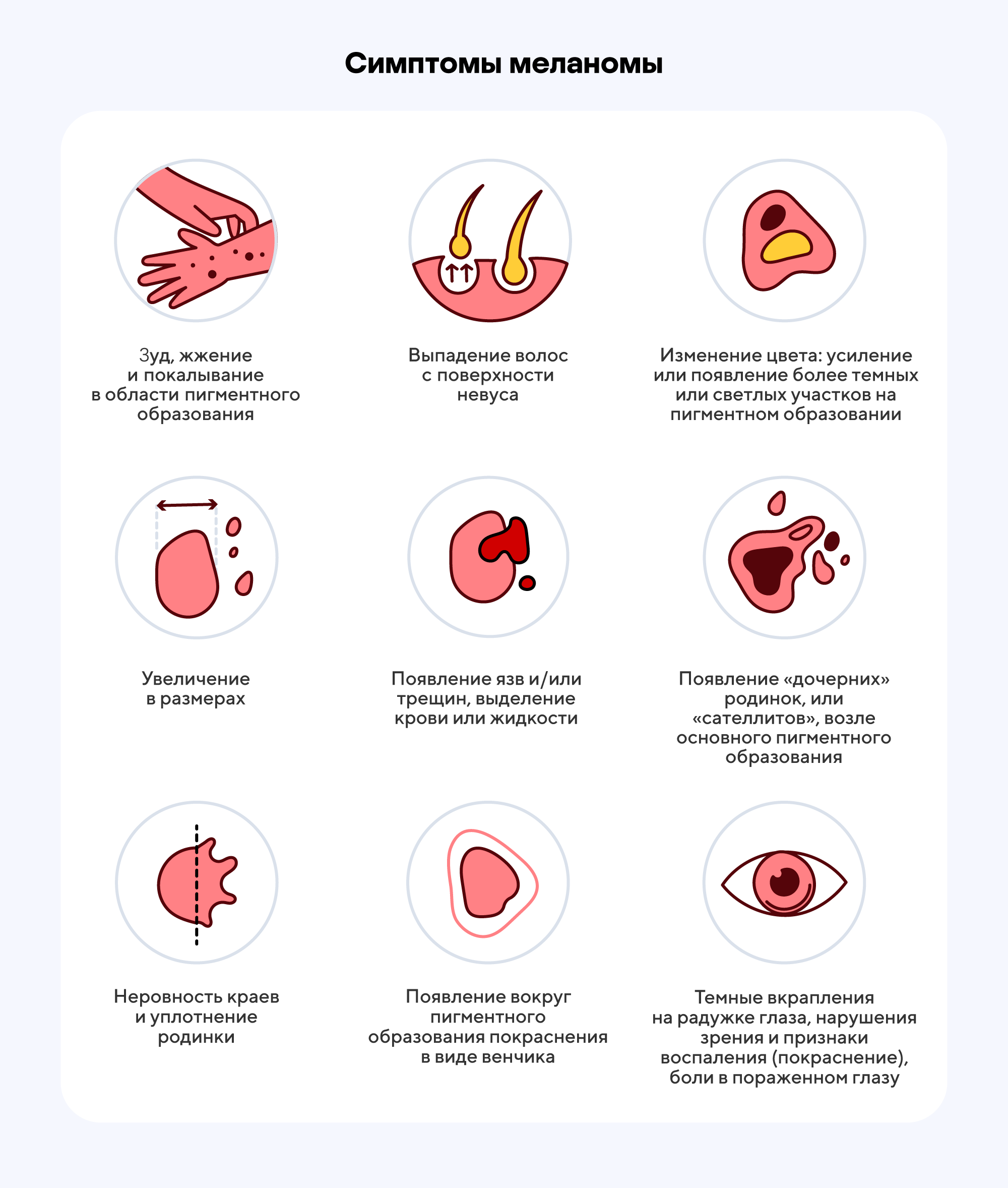
Однако в последнее время накопились свидетельства того, что метотрексат может быть косвенным виновником, повышающим риск развития меланомы. Возможно, в определенной степени это происходит из-за роли «двойного агента», ведь метотрексат и подавляет клеточное деление, и отчасти угнетает иммунную систему. Выводы об этом сделали по результатам 17 исследований, из которых 12 включали 16 642 случая меланомы: у участников, принимающих метотрексат, был выявлен небольшой риск развития рака кожи. При этом авторы уже другого исследования, в котором изучали эту же взаимосвязь, подчеркивают, что не стоит демонизировать метотрексат. Возможно, полученные результаты обусловлены ошибкой в статистическом анализе. Абсолютный риск развития меланомы после приема метотрексата по-прежнему очень мал. Также может быть, что эти результаты связаны не с самим приемом препарата, а всего лишь отражают общий рост заболеваемости меланомой на уровне популяции — не будем забывать, что развитие злокачественных новообразований связано с действием множества факторов. Но в любом случае прием метотрексата или любого другого иммуносупрессивного препарата должен происходить под контролем лечащего врача.
Можно ли диагностировать онкологическое заболевание, если нет симптомов?
Так ли это? Отчасти да.
Как на самом деле? Часто онкологические заболевания протекают без симптомов, особенно на ранних стадиях. Для ранней диагностики широко применяют различные анализы на онкомаркеры. Обычно лаборатории предлагают услуги по анализу крови для выявления широкого спектра онкомаркеров. Однако не стоит слепо доверять результатам таких проверок — уровень онкомаркеров может повышаться из-за самых разных причин, необязательно связанных с развитием злокачественного новообразования. Результаты анализов совместно с данными других диагностических исследований должен интерпретировать лечащий врач. Целесообразность сдачи онкомаркеров определяется числом пациентов, которых можно спасти с помощью этого анализа. К сожалению, ни один из маркеров не продемонстрировал в этом отношении значимых результатов.
В случае если человек абсолютно здоров, у него нет генетической предрасположенности и каких-либо беспокоящих симптомов, то для женщин нет необходимости сдавать анализы на онкомаркеры. Для мужчин в возрасте от 55 до 69 лет имеет смысл не чаще одного раза в год сдавать анализ на ПСА (простатспецифический антиген) с целью скрининга рака предстательной железы.
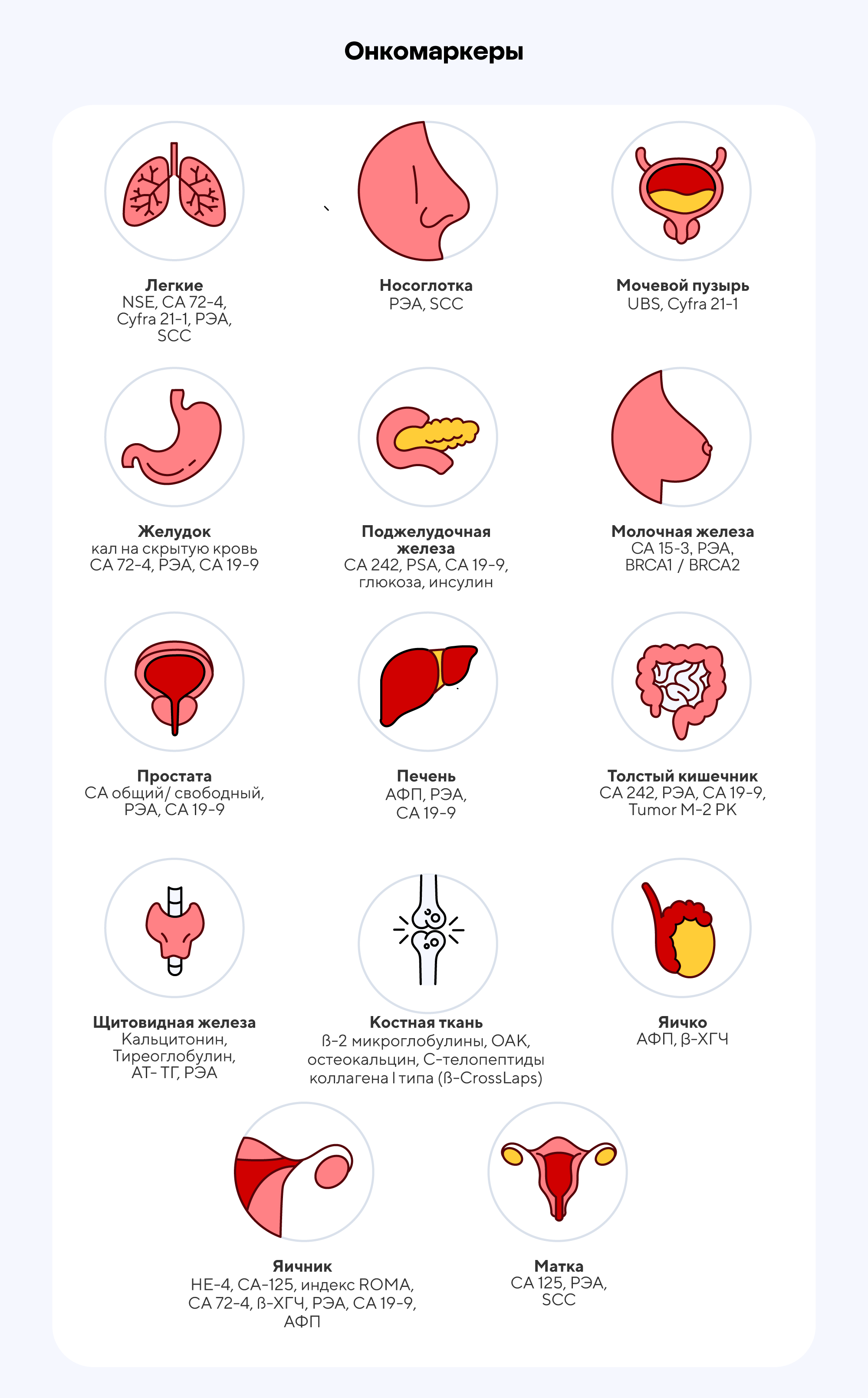
У каждого конкретного вида опухоли есть свой набор онкомаркеров, позволяющих оценивать динамику заболевания
Если говорить о проведении онкоскринингов, то доказанная польза в настоящий момент существует для нескольких видов рака: толстой кишки, легкого, молочной железы и меланомы. Разберемся по порядку.
Будут ли в ближайшее время доступны онковакцины?
Так ли это? Пока что неизвестно.
Как на самом деле? Первые разработки берут свое начало еще с конца 19-го века. На сегодняшний день, пожалуй, наиболее известной можно назвать вакцину против вируса папилломы человека. Инфицирование определенными штаммами данного вируса считается одной из наиболее распространенных причин, которые провоцируют рак шейки матки. Поэтому вакцинация от этого вируса считается одним из наиболее надежных способов профилактики.
Толчком для развития более современных версий вакцин от онкологических заболеваний стало создание РНК-вакцин против COVID-19, разработанных компаниями Moderna и BioNTech/Pfizer. На сегодняшний день вакцины могут быть на основе как белков или их фрагментов, так и кодирующих их нуклеиновых кислот, вирусов или даже целых клеток, например дендритных. Однако, несмотря на развитие этого направления, пока что рано говорить о конкретных сроках доступности вакцин от рака для пациентов.
На сегодняшний день ведутся клинические исследования для более 100 неоантигенных онковакцин, в первую очередь против меланомы и рака легкого. Например, в числе интересных разработок можно назвать мРНК-вакцину от компании BioNTech для лечения рака поджелудочной железы — несмотря на небольшую выборку пациентов, перспективы для ее применения могут быть вполне хорошими, но нужно еще время.
Одна из главных трудностей при создании таких вакцин — их персонализированность, то есть «настройка» на опухолевые неоантигены одного конкретного пациента. Для этого необходимо взять образец опухоли (биопсию) и провести трудоемкий анализ этих самых неоантигенов, после чего создать РНК, кодирующую нужные последовательности, и упаковать ее в специальную оболочку для введения в организм человека.
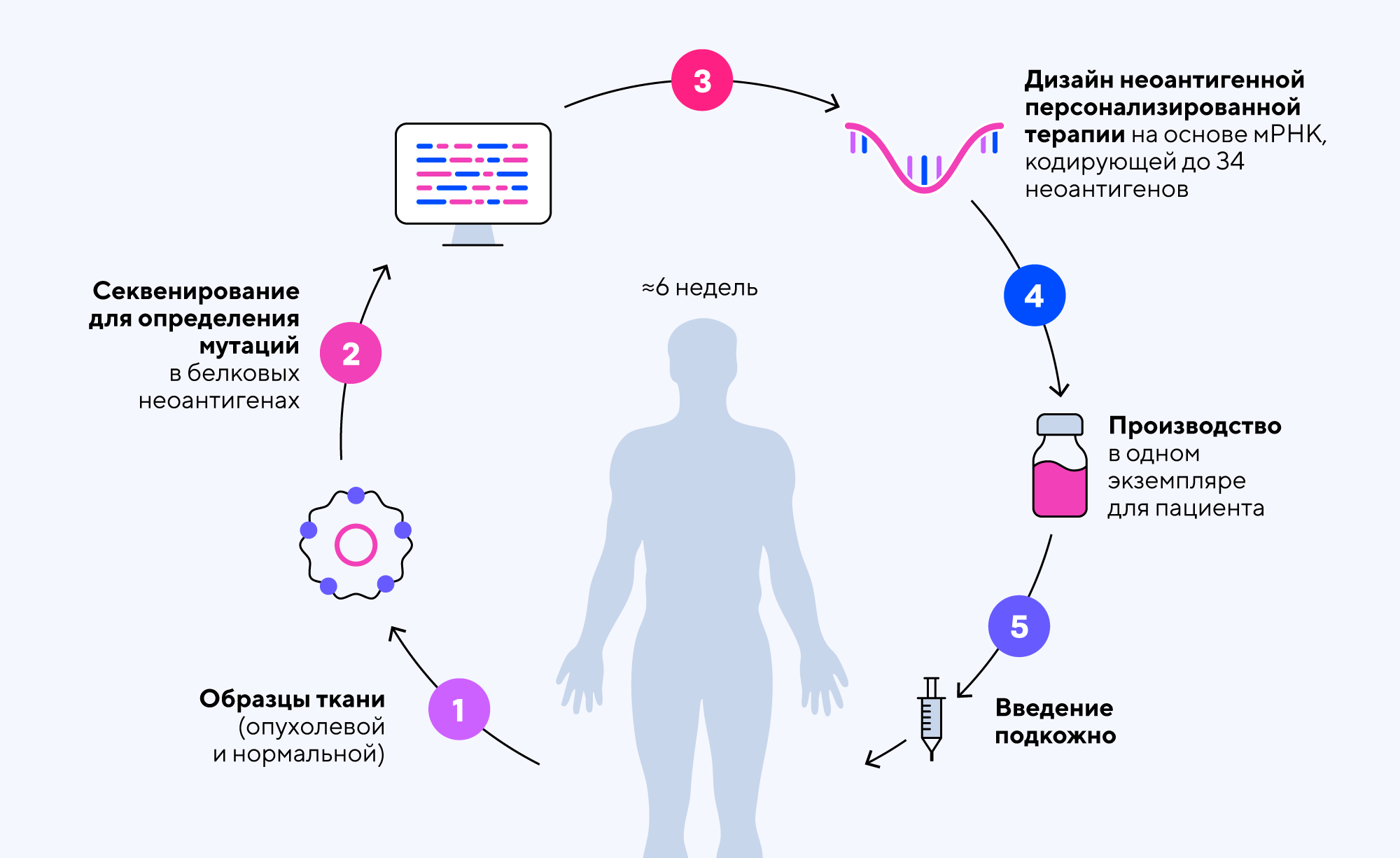
Схема изготовления персонализированной неоантигенной вакцины
Из недавних заявлений также можно отметить разработку НМИЦ радиологии Минздрава России совместно с Институтом молекулярной биологии имени В. А. Энгельгардта, которые в конце 2024 года начали (но уже, кажется, приостановили) набор добровольцев для изучения своей онколитической вакцины. Поэтому пока что рано говорить о конкретных сроках доступности вакцин от рака для пациентов. Несмотря на это, неоантигенный подход к разработке вакцин остается довольно многообещающим и привлекательным.
Правда ли, что у людей с рассеянным склерозом не может быть рака?
Так ли это? Нет.
Как на самом деле? У пациентов с аутоиммунными заболеваниями, в том числе с рассеянным склерозом, которые получают терапию иммуносупрессантами, по статистике, отмечается повышение риска развития онкологических заболеваний. Это работает и в обратную сторону — некоторые злокачественные новообразования также могут спровоцировать аутоиммунные нарушения в организме. В частности, достоверно подтверждена взаимосвязь между наличием у человека аутоиммунного заболевания и развитие рака мочевого пузыря и тела матки.
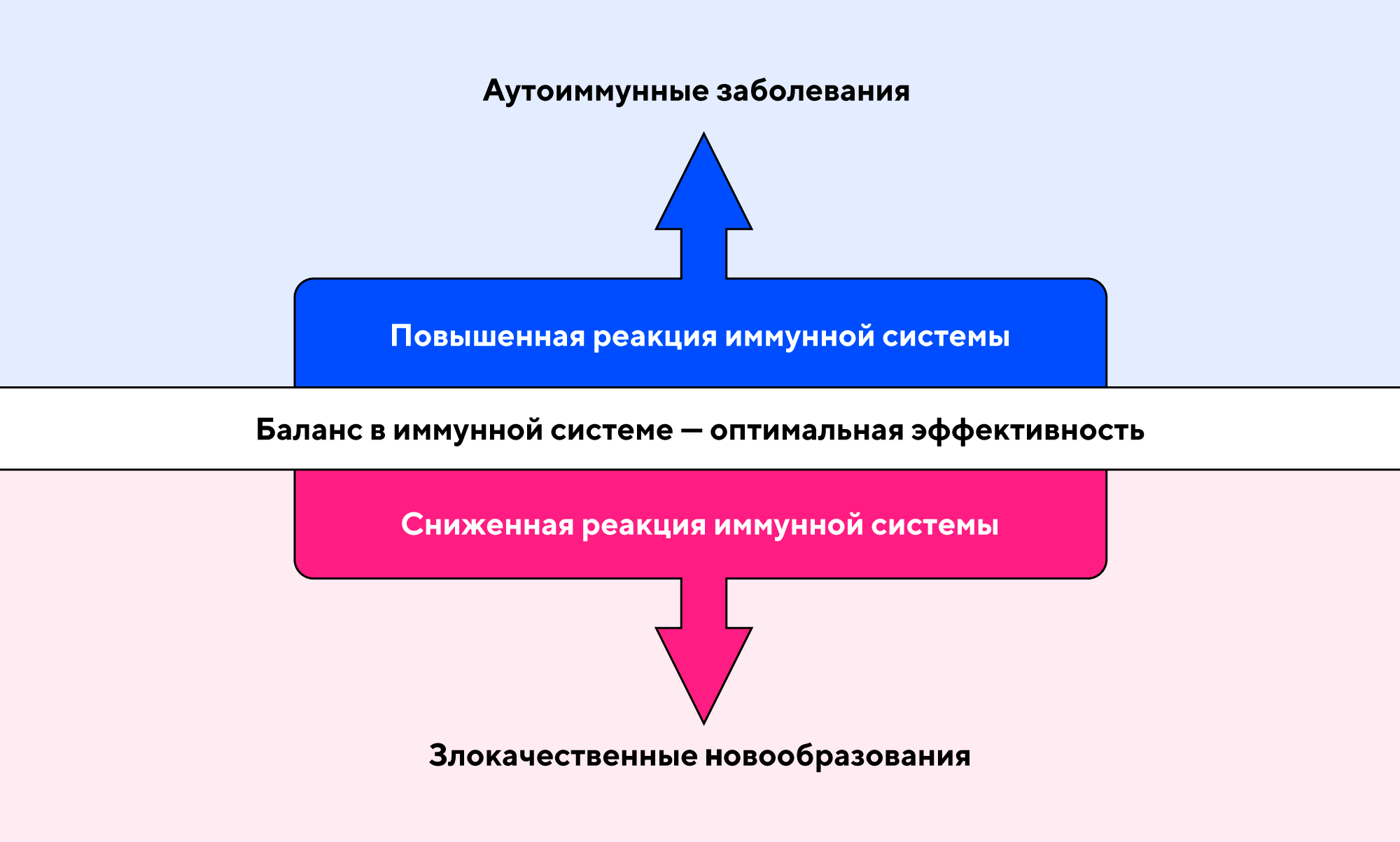
Аутоиммунные и онкологические заболевания связаны с нарушениями «настроек» иммунной системы, но с разных сторон: первые — из-за повышенной реакции, вторые — из-за ухода клеток от иммунного надзора. Несмотря на это, многочисленные исследования показывают взаимосвязь между раком и последующим развитием аутоиммунных заболеваний
Пищевод Барретта — это не онкология?
Так ли это? Нет, но есть нюансы.
Как на самом деле? Пищевод Барретта — это отдельное заболевание, при котором патологически изменяется слизистая оболочка пищевода. Обычно такое состояние вызывается внешними факторами и сопутствующими причинами, среди которых — осложнение уже имеющейся у человека гастроэзофагеальной рефлюксной болезни (ГЭРБ), которое может происходить при нарушении рекомендованной диеты, а также под влиянием курения и приема алкоголя. Коварность пищевода Барретта в том, что при этом заболевании происходит перерождение клеток слизистой, и в конечном итоге, без надлежащего лечения, это может приводить к развитию злокачественного новообразования.
Проводят ли какие-либо исследования в области лечения рака поджелудочной железы?
Так ли это? Да, но есть сложности.
Как на самом деле? Для лечения рака поджелудочной железы в настоящий момент проводится множество исследований, а само это показание считается приоритетным для изучения. Так, по данным ClincalTrials.gov, ресурса, где обязательно регистрируются все проводимые в США клинические испытания, по запросу «рак поджелудочной» отображается 4 632 клинических исследования. Однако пока что существуют определенные сложности в разработке препаратов для лечения этой болезни, в частности — трудность в доставке терапевтического средства к месту назначения из-за состава микроокружения и стромы опухоли.
Возможно ли создать на базе BIOCAD аналог препарата Абраксан?
Так ли это? Теоретически возможно, но в настоящее время разработки полного аналога Абраксана на базе BIOCAD не ведутся.
Как на самом деле? Действительно, препарат Абраксан показал свою эффективность в лечении рака поджелудочной железы, как и в случае других онкологических заболеваний. Абраксан представляет собой паклитаксел — цитотоксический противоопухолевый препарат из класса таксанов, стабилизированный белком альбумином. Принцип его действия основан на том, что опухолевые клетки потребляют альбумин из микроокружения опухоли, и альбумин, достигая этого микроокружения, является своеобразным переносчиком для паклитаксела.
В BIOCAD осуществляется производство препарата Таксакад®, который представляет собой паклитаксел. Но разрабатывать паклитаксел, стабилизированный альбумином, на данный момент мы не планируем.
Существует ли «паразитарный след» в онкологии?
Так ли это? Для отдельных разновидностей онкологических заболеваний — да, может быть.
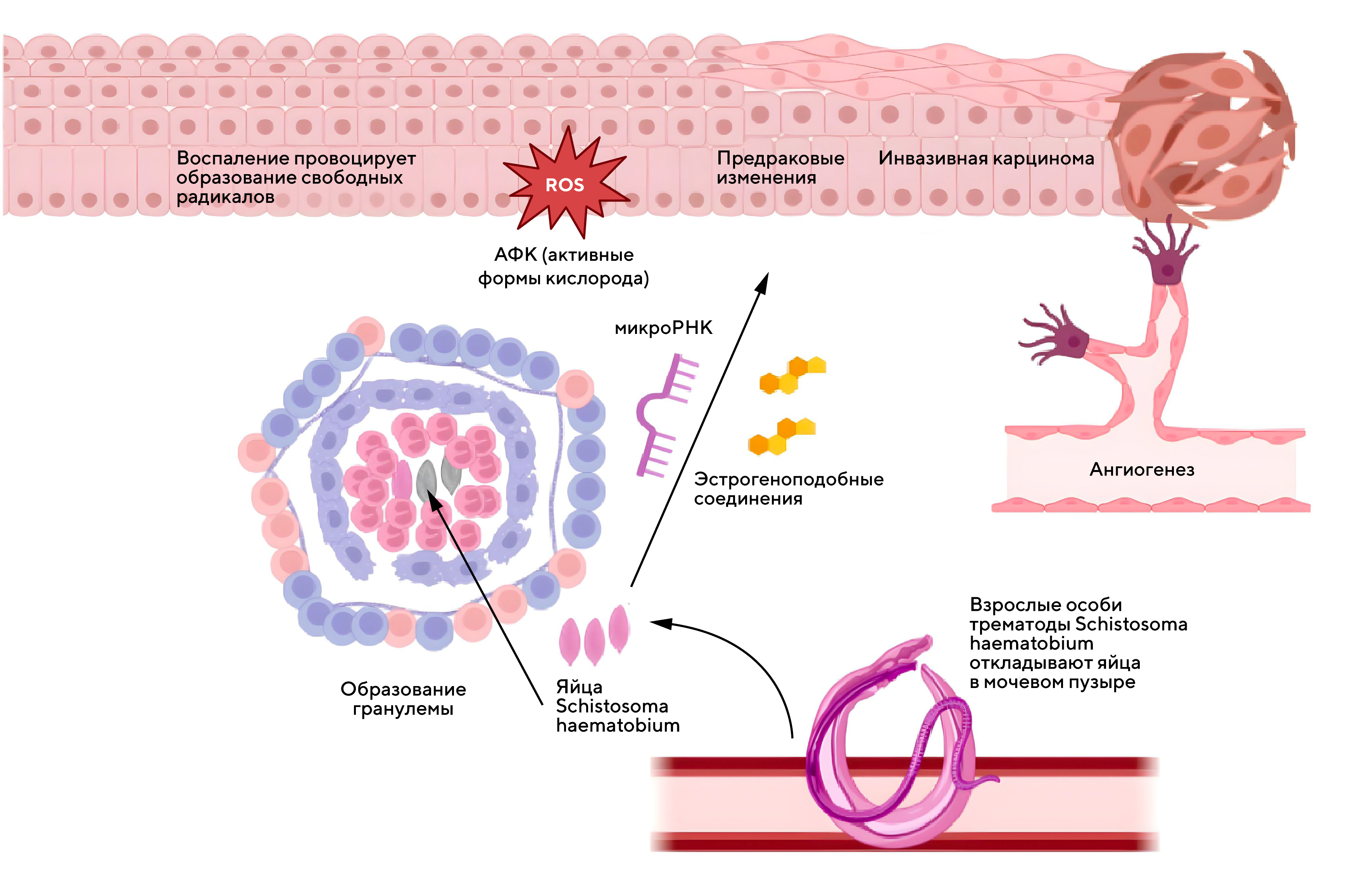
Как на самом деле? Этиология злокачественных новообразований различна и опосредована множеством факторов, в числе которых может быть и так называемое паразитарное происхождение болезни. Например, трематода Schistosoma haematobium, которая известна благодаря своей способности вызывать инфекционное заболевание шистосомоз, также увеличивает риск развития рака мочевого пузыря. Заражение этим паразитом может происходить во время плавания или при переходе вброд в пресной воде, населенной трематодами S. haematobium. Яйца паразита, как правило, оседают в мочевом пузыре. В случае если инфекция сохраняется на протяжении длительного времени без лечения, в организме развивается воспалительная реакция, вслед за которой образуются язвы и рубцевание. Хроническое раздражение и другие сопутствующие симптомы, вызванные шистосомозом, считаются предрасполагающими для развития рака мочевого пузыря.
Правда ли, что химиотерапия не «чистит» лимфу, поэтому лимфоузлы удаляют?
Так ли это? Нет.
Как на самом деле? Химиотерапия не несет в себе функцию очищения организма. Да и сам по себе эффект химиотерапии не имеет направленности или избирательности, а действует по всему организму, преимущественно поражая наиболее быстро делящиеся клетки — ими, как правило, являются опухолевые клетки. Поэтому говорить о «чистке лимфы» с помощью химиотерапии некорректно. Лимфоузлы же действительно в некоторых случаях удаляют, чтобы воспрепятствовать дальнейшему проникновению и распространению злокачественных клеток по организму.
Онкологическое заболевание — не показание к суррогатному материнству?
Так ли это? Неизвестно.
Что известно? Влияние беременности на течение онкологических процессов — очень сложный и многогранный вопрос. Так, эстрогены — стероидные женские половые гормоны, уровень которых повышается во время беременности, могут быть связаны с повышением риска развития рака молочной железы. Однако есть и другие любопытные данные — например, описан протективный эффект более ранней беременности в возрасте 20–30 лет на развитие рака молочной железы в более взрослом возрасте. Но, несмотря на это, течение беременности, сопряженной с онкологическим заболеванием — индивидуальный процесс, который во многом определяется типом злокачественного новообразования и его чувствительностью к половым гормонам. Поэтому в каждом конкретном случае важно консультироваться с лечащим врачом, который должен оценивать потенциальный риск, связанный с беременностью, на течение опухолевого процесса.
Может ли эстроген вызывать онкологические заболевания?
Так ли это? Точные причины возникновения рака неизвестны.
Что известно? Крупные исследования, посвященные раку молочной железы, показали: применение гормональных контрацептивов повышает риск развития этого злокачественного новообразования при использовании прогестеронсодержащих препаратов, но риск не увеличивается в случае приема только эстрогенсодержащих препаратов. Эстроген, таким образом, через стимуляцию эффекта прогестерона увеличивает риск развития рака молочной железы у женщин в менопаузе. Для реализации онкогенного эффекта гормонов, по всей видимости, нужны какие-либо предрасполагающие факторы. Адъювантную гормонотерапию, действительно, назначают в течение некоторого времени после основного курса лечения рака молочной железы. Сроки терапии определены проведенными клиническими исследованиями.
Можно ли каким-то образом поддержать и восстановить слизистую желудка во время и после химиотерапии?
Так ли это? Да.
Как это сделать? Для профилактики эрозивного или язвенного поражения желудка во время агрессивной химиотерапии применяются препараты, понижающие кислотность желудка — блокаторы гистаминовых рецепторов или блокаторы протонной помпы. Эти препараты должен назначать врач-химиотерапевт при необходимости после обследования пациента. Если симптомы поражения слизистой желудка сохраняются после завершения курса химиотерапии, необходимо провести дополнительные обследования, например гастроскопию, pН-метрию, анализ на Helicobacter. Это поможет лечащему врачу выработать тактику лечения для каждого конкретного случая.