Как работает препарат Трибувиа®: разбираемся, в чем уникальность
В 2024 году BIOCAD получил регистрационное удостоверение на первый в классе препарат для терапии болезни Бехтерева — Трибувиа®. В ноябре 2023 года ведущий научный журнал Nature Medicine* опубликовал статью о научном открытии, которое лежит в основе препарата. Мы перевели и переработали текст статьи и в этом материале рассказали, в чем уникальность механизма действия препарата. Приготовьтесь, текст будет непростым.
Направленный подход против иммунных ошибок
На протяжении более ста лет болезнь Бехтерева, или анкилозирующий спондилит, лечили с помощью поддерживающей терапии, основная цель которой заключалась в снятии симптомов и улучшении качества жизни пациентов. Со временем методы лечения совершенствовались, и в арсенале врачей появлялись более эффективные лекарственные средства, которые могли приостановить воспалительные процессы, хотя не воздействовали на причину заболевания. Наконец, недавним прорывом стал новый метод таргетной терапии, направленный на первопричину болезни и способный нейтрализовать вышедшие из-под контроля Т-клетки. О том, как это работает, какие сложности сопровождали раннюю разработку антитела против анкилозирующего спондилита и какие перспективы открываются благодаря этому проекту, читайте в статье.
Почему возникает болезнь «неподвижного позвоночника»
Болезнь Бехтерева, или анкилозирующий спондилит, — аутоиммунное заболевание, при котором собственные Т-клетки атакуют суставы. Хроническое воспаление затрагивает осевой скелет, постепенно вызывая сращивание суставов — анкилоз. Из-за этого наиболее характерным симптомом болезни считается «неподвижный позвоночник».
Механизм развития анкилозирующего спондилита стал известен благодаря исследованиям в области иммунологии, а конкретно — изучению роли Т-лимфоцитов в развитии различных аутоиммунных состояний. В норме эти клетки патрулируют организм на предмет возможных поломок или «непрошеных гостей». Для идентификации неполадок Т-клетки используют особые рецепторы на своей поверхности — TCR (T-cell receptor). С помощью TCR Т-клетки взаимодействуют с поверхностью всех клеток организма, вернее, с главным комплексом гистосовместимости I типа, MHC-I (major histocompatibility complex). Но если внутрь клетки пробрался неизвестный инфекционный агент или же с ее собственным белком произошла какая-то поломка, то об этом будет известно с помощью «выставления» образцов на поверхности. Этот процесс называется презентацией антигена. В этом случае Т-клетки после связывания с MHC в зависимости от своего типа (CD4+ или CD8+) либо призывают на помощь другие иммунные клетки, способные справиться со сломанной клеткой, либо самостоятельно уничтожают ее. В случае анкилозирующего спондилита основную роль играет второй тип — цитотоксические СD8+ Т-клетки, способные убивать «неправильные» клетки.
Итак, в узнавании зараженных или поломанных клеток ключевую роль играет Т-клеточный рецептор, TCR. В организме существует огромное разнообразие Т-клеток с различными TCR на своей поверхности, которые способны с высочайшей точностью распознавать самые разные мишени, но все эти рецепторы имеют сходное строение. TCR состоит из двух субъединиц — альфа- и бета-цепей, в которых выделяют разные сегменты: V (variable), D (diversity), J (joining) и C (constant). Из них три региона — V, D и J — являются вариабельными, то есть собираются в цепи TCR случайным образом. Благодаря этой случайной мозаике в организме формируется невероятное разнообразие TCR, способных распознавать огромное количество мишеней. Одним из генов, которые вносят свой вклад в генетическое разнообразие TCR, является ген TRBV9, который кодирует один из V-участков бета-цепи. Именно эта последовательность станет ключевым элементом в рассказе о лечении анкилозирующего спондилита.
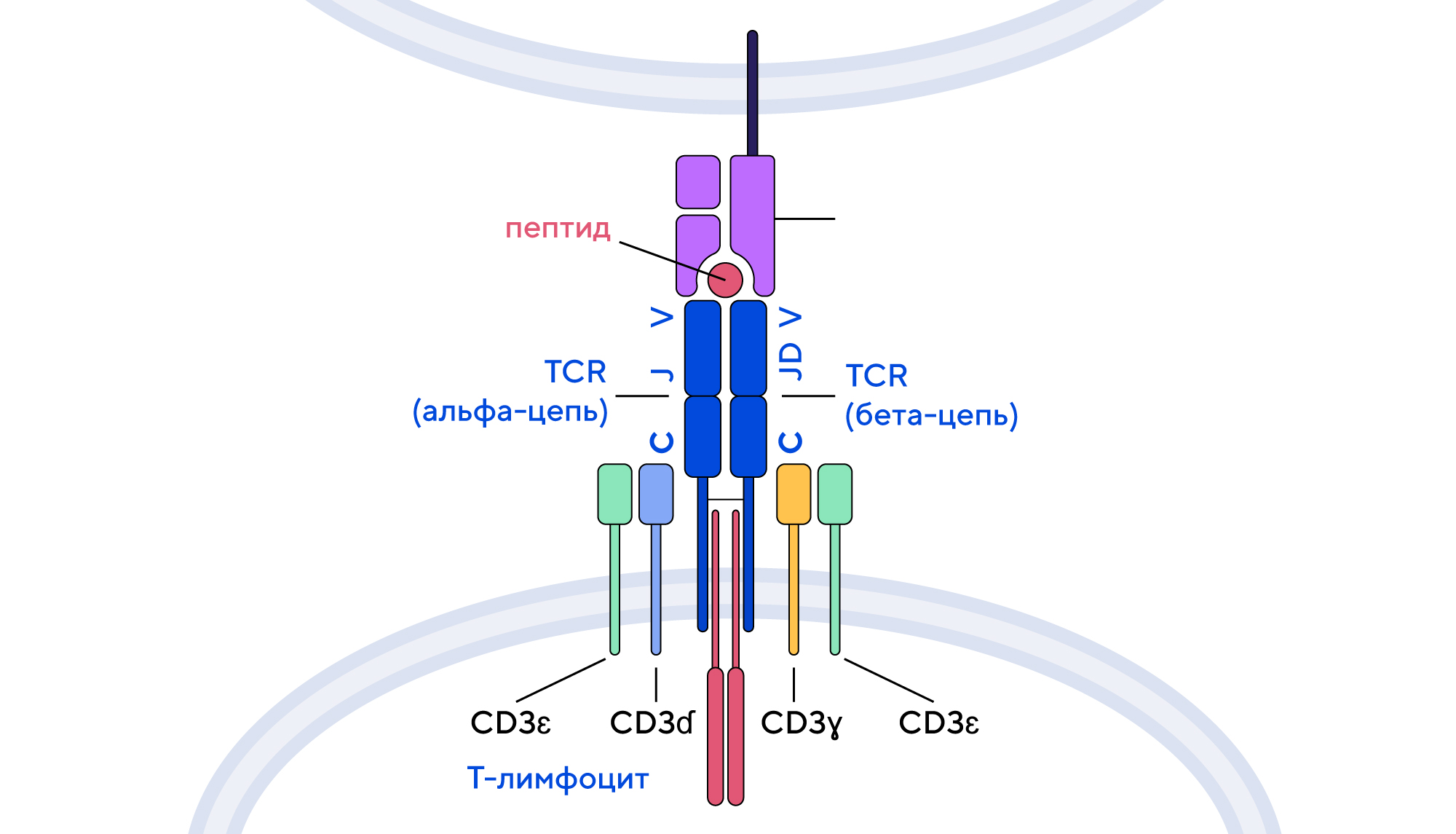
Распознавание пептида в комплексе с MHC на поверхности клетки и его связывание с клеточным рецептором на поверхности Т-лимфоцита
Это основной механизм, способный запустить Т-клеточный адаптивный иммунитет против инфицированных, опухолевых или поломанных клеток. Состав VDJ-участка на бета-цепи формируется случайным образом, когда в цепь попадает один из 52 возможных вариантов V-участков, один из двух возможных D-участков и один из 13 возможных J-сегментов. В случае анкилозирующего спондилита ключевой является последовательность TRBV9 в V-участке девятого семейства вариабельного домена бета-цепи.
Огромное разнообразие Т-клеточных рецепторов, которые формируются благодаря случайной генерации V(D)J-доменов, — это колоссальное преимущество, которое помогает нашему организму генерировать защиту против самых разных вирусов или поломанных клеток. Однако за этими случайными сборками ТCR может скрываться проблема — например, иногда при случайном сочетании доменов появляются такие рецепторы, которые будут принимать собственные клетки организма за чужеродные. Конечно, природа позаботилась о том, чтобы минимизировать эту вероятность. Для этого в организме настроены несколько уровней проверки. Так, каждая новая Т-клетка перед началом работы проходит обучение на толерантность к собственным тканям. Если этот экзамен будет провален и TCR свяжется с собственным МНС на поверхности нормальной клетки, эта Т-клетка будет уничтожена. Такой процесс отбора называют негативной селекцией. Но даже если аутореактивной Т-клетке, реагирующей на собственные здоровые белки, удалось каким-то образом преодолеть первый барьер защиты, то в большинстве случаев ее все равно заметят особые Т-регуляторные клетки — они обнаружат и подавят повышенную активность Т-клетки. Однако иногда этого не происходит, и в организме оказываются вышедшие из-под контроля Т-клетки, которые реагируют даже на небольшие концентрации собственных пептидов, вызывая воспаление. В таком случае говорят о развитии аутоиммунного состояния.
При анкилозирующем спондилите важную роль играет фактор гистосовместимости HLA-B27. Еще в 1970-е годы выяснилось, что у многих пациентов с анкилозирующим спондилитом (более 90%), с псориатическим артритом (до 50%) и другими аутоиммунными заболеваниями присутствует ген HLA-B27. Нормальные клетки могут презентировать фрагменты своих белков на поверхности в комплексе с HLA-B27. Если у человека происходит иммунологический сбой при сборке вариабельной части TCR, то Т-клетки могут неадекватно реагировать на HLA-B27 в комплексе с нормальным фрагментом белка и, принимая его за микробный пептид, атаковать нормальную клетку. В результате повреждения клеток и тканей развиваются симптомы заболевания, в частности анкилозирующего спондилита.
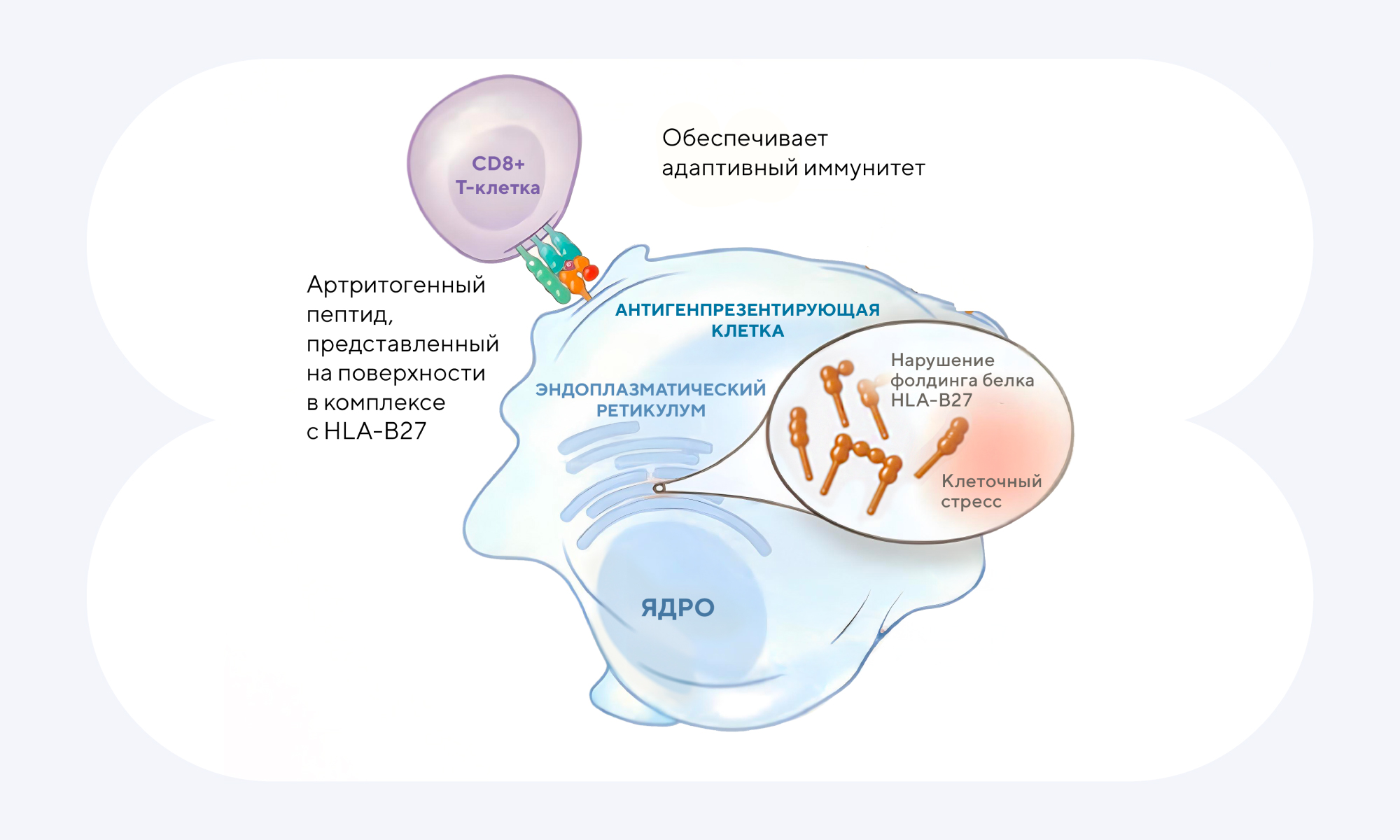
HLA-B27: механизм активации аутореактивных CD8+ Т-клеток и связь с анкилозирующим спондилитом
Существует несколько теорий о том, какую именно роль играет HLA-B27 в развитии анкилозирующего спондилита. Так, к неправильной реакции аутореактивных Т-клеток могут приводить неправильная сборка белка или клеточный стресс, в частности, связанный с эндоплазматическим ретикулумом, где происходит активный синтез белков. При сочетании нескольких факторов Т-клетки начинают распознавать собственные клетки организма с HLA-B27 и пептидом на поверхности как чужеродные, атакуя их.
Теперь соединим вместе все эти факты о TCR, HLA-B27 и последовательности TRBV9. Расшифровка структуры обеих цепей патогенного TCR и накопленные ранее знания о механизме развития аутоиммунной реакции показали: анкилозирующий спондилит развивается в случае, когда вышедшие из-под контроля Т-клетки с вариабельным фрагментом TRBV9 в своем рецепторе некорректно распознают нормальные клетки, несущие на своей поверхности HLA-B27. В результате происходит активация TRBV9+ Т-лимфоцитов и повреждение тканей. Если избавиться от аутореактивных Т-клеток, можно остановить болезнь.
Как бороться с аутореактивными Т-клетками
Недавно был предложен новый метод лечения анкилозирующего спондилита, который позволяет прицельно воздействовать на первопричину болезни — аутореактивные Т-клетки с определенным участком рецептора TRBV9. В результате сотрудничества между РНИМУ им. Н. И. Пирогова и BIOCAD удалось разработать терапевтическое моноклональное антитело BCD-180, которое способно распознавать и уничтожать Т-лимфоциты, имеющие в рецепторе фрагмент TRBV9, не затрагивая остальные клетки организма.
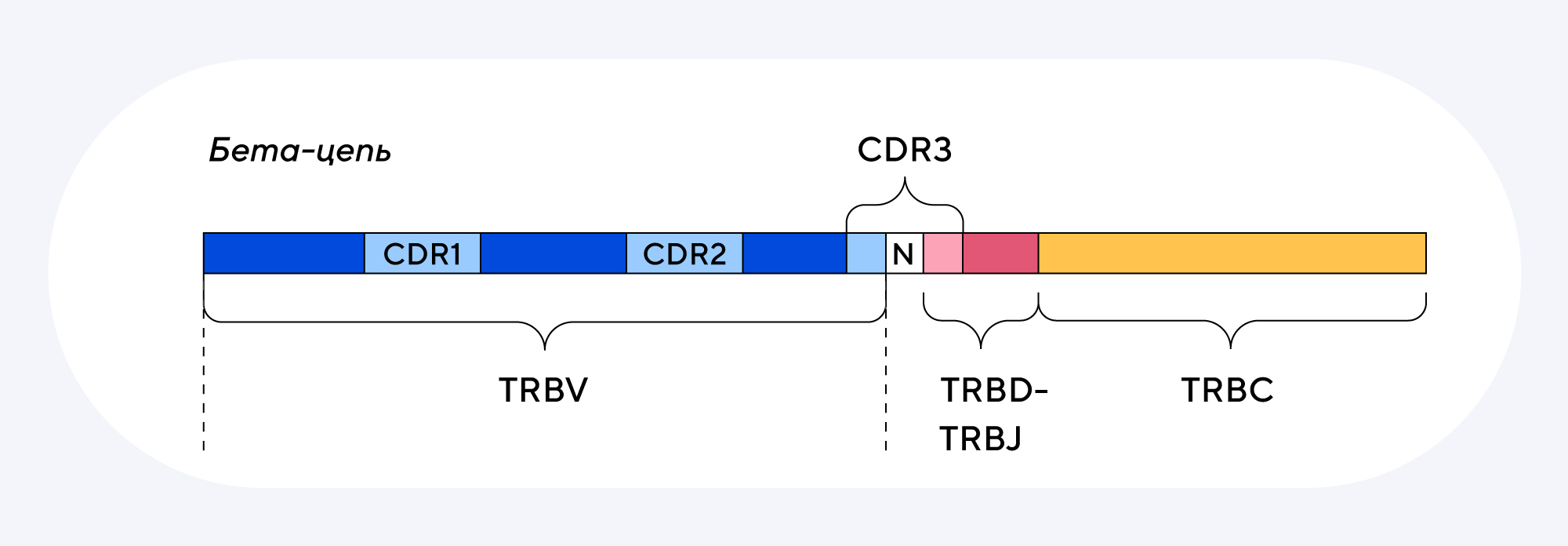
Молекула BCD-180 нацелена против участка TRBV9 — это регион V (variable) 9-го типа вариабельного домена бета-цепи Т-клеточного рецептора
Важная особенность моноклонального антитела BCD-180 — его усиленная эффекторная функция, то есть способность эффективно привлекать другие клетки иммунной системы для уничтожения мишени. Влиять на эффекторные функции можно разными способами, в том числе за счет внесения конкретных мутаций, усиливающих силу действия антитела. Однако при разработке молекулы BCD-180 использовали другой способ модификации. Для усиления активации иммунных клеток изменили углеводную часть антитела, а конкретно — удалили остаток фукозы.
Результаты промежуточных данных клинических исследований показывают, что после введения BCD-180 уровень аутореактивных Т-лимфоцитов падает почти до нуля. При этом высокая эффективность устранения таргетных клеток — это не единственное преимущество нового моноклонального антитела. Так, удалось показать, что после терапии BCD-180 из Т-клеточного репертуара специфичным образом удаляются только те Т-лимфоциты, которые несут в своих TCR-регион TRBV9, остальные продолжают выполнять свои защитные функции. Благодаря такой специфичности терапия с помощью BCD-180 имеет благоприятный профиль безопасности.
Здесь хочется отметить, что TRBV9 несут на себе не только аутореактивные, но и вполне здоровые Т-клетки. Но при терапии BCD-180 уничтожаются вообще все клетки с регионом TRBV9 — и вышедшие из-под контроля, и нормальные. Однако это не приводит к значимой иммуносупрессии. Дело в том, что Т-клетки с TRBV9 составляют лишь небольшую часть популяции, менее 5% от общего числа клеток. Поэтому, даже если под воздействием BCD-180 погибнут полезные Т-лимфоциты, это не приведет к снижению иммунной защиты: среди огромного разнообразия иммунных клеток найдутся другие, способные бороться с патогенами1.
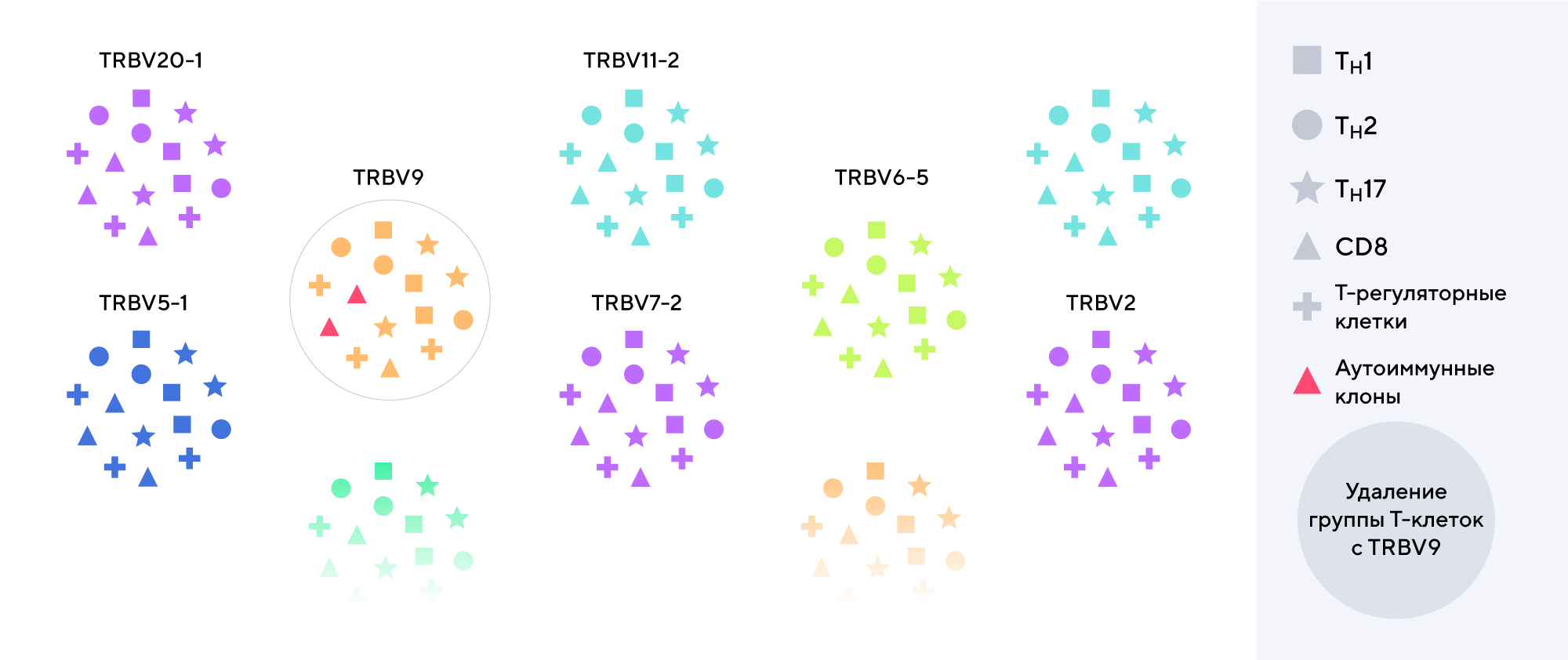
Терапия BCD-180 уничтожает все клоны Т-клеток с TRBV9 — и аутоиммунные, и здоровые. Однако это не оказывает системного влияния на общий Т-клеточный иммунитет2. Поэтому удаление из популяции Т-клеток с сегментом TRBV9 не подавляет иммунные реакции, связанные с различными видами Т-лимфоцитов
В чем сложность разработки BCD-180
Основное преимущество лечения анкилозирующего спондилита с помощью BCD-180 — в его таргетном действии, направленном против первопричины заболевания. В этом, пожалуй, и заключалась главная сложность: для разработки моноклонального антитела против такой уникальной и специфичной мишени, как TRBV9, требовалось очень тщательное моделирование мишени с учетом ее природной структуры. Также на этапе ранней разработки необходимо учитывать множество технических нюансов, чтобы не допустить ошибок при наработке и очистке антигена для дальнейшего получения молекулы. Однако все эти усилия нацелены на достижение сложной цели: создать моноклональное антитело, способное очень точно узнавать и уничтожать узкую и специфичную группу конкретных клеток.
Сложности с получением моноклонального антитела BCD-180 во многом были связаны со структурой мишени — антигена с регионом TRBV9. Важно было получить природную форму этой мишени, то есть последовательность в составе TCR. Как правило, работа с препаратами против Т-клеточных рецепторов — сложный процесс, так как TCR представляют из себя сложный комплекс из множества белков. Для правильного распознавания мишени антителом необходимо четко смоделировать и собрать этот белковый комплекс. Здесь на помощь приходят методы компьютерного моделирования in silico, а также адаптированные схемы очистки и пробоподготовки. Однако все эти сложности помогают решить важную задачу — разработать эффекторное моноклональное антитело, способное точечно связываться с конкретным участком в Т-лимфоцитах.
Какие перспективы открывает терапия с помощью BCD-180
Одним из главных достижений нового подхода к терапии, кроме, разумеется, самой разработки молекулы, направленной на первопричину болезни, стало то, что удалось собрать воедино все известные факты о причинах и механизмах ряда аутоиммунных заболеваний. Вспомним, что связь между HLA-B27 и развитием артритов была известна еще с 1970-х годов, а первые данные о последовательности TRBV9 и ее связи с развитием анкилозирующего спондилита появились в конце 1990-х. Однако именно в этой работе впервые удалось сложить вместе кусочки мозаики и увидеть полную картину развития и способа лечения болезни.
Успешное создание моноклонального антитела BCD-180 позволило продемонстрировать, что против болезней, связанных с T-клеточными рецепторами, вполне можно бороться. И если раньше разработка молекул, связывающихся со специфичными участками в конкретном рецепторе, практически не велась, то сейчас удалось показать: несмотря на все сложности, возможно создавать уникальные препараты против конкретных TCR.
В будущем терапию против TRBV9 можно расширить и на другие аутоиммунные заболевания, связанные с HLA-B27. А уже созданное моноклональное антитело BCD-180 можно использовать не только для терапии анкилозирующего спондилита, но и для подготовки других антигенов для лечения различных болезней.